
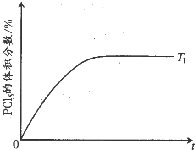
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl5)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
分析 (1)0~150s内的平均反应速率v(PCl5)=$\frac{\frac{△n}{V}}{△t}$,该段时间内v(PCl3)=v(PCl5);
(2)开始时c(PCl3)=$\frac{2.0mol}{2.0L}$=1.0mol/L、c(Cl2)=$\frac{1.0mol}{2.0L}$=0.5mol/L,平衡时c(PCl5)=$\frac{0.40mol}{2.0L}$=0.2mol/L,
PCl3(g)+Cl2(g)?PCl5(g)△H=-93.0kJ•mol-1,
开始(mol/L)1.0 0.5 0
反应(mol/L)0.2 0.2 0.2
平衡(mol/L)0.8 0.3 0.2
化学平衡常数K=$\frac{c(PC{l}_{5})}{c(PC{l}_{3}).c(C{l}_{2})}$;
(3)250s时生成n(PCl5)=0.40mol,根据五氯化磷和反应热之间的关系式计算放出热量;
(4)a.反应前后气体总质量不变、容器体积不变,根据ρ=$\frac{m}{V}$计算;
b.所有的化学反应只要升高温度正逆反应速率都增大;
c.350s 时,向该密闭容器中充入氮气,参加反应的各气体浓度不变,化学平衡不移动;
d.相同条件下,若起始向该密闭容器中充入1.0molPCl3和0.2molCl2,与原反应相比,相当于减小压强平衡向气体体积增大的方向移动;
(5)该反应的正反应是放热反应,升高温度化学反应速率加快,反应达到平衡时间缩短,但平衡逆向移动,达到平衡时五氯化磷体积分数降低.
解答 解:(1)0~150s内的平均反应速率v(PCl5)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.36-0}{2}}{150}$mol.L-1•s-1=1.2×10-3或0.0012
mol.L-1•s-1,该段时间内v(PCl3)=v(PCl5)=1.2×10-3或0.0012mol.L-1•s-1,
故答案为:1.2×10-3或0.0012;
(2)开始时c(PCl3)=$\frac{2.0mol}{2.0L}$=1.0mol/L、c(Cl2)=$\frac{1.0mol}{2.0L}$=0.5mol/L,平衡时c(PCl5)=$\frac{0.40mol}{2.0L}$=0.2mol/L,
PCl3(g)+Cl2(g)?PCl5(g)△H=-93.0kJ•mol-1,
开始(mol/L)1.0 0.5 0
反应(mol/L)0.2 0.2 0.2
平衡(mol/L)0.8 0.3 0.2
化学平衡常数K=$\frac{c(PC{l}_{5})}{c(PC{l}_{3}).c(C{l}_{2})}$=$\frac{0.2}{0.8×0.3}$=$\frac{5}{6}$,
故答案为:$\frac{5}{6}$;
(3)生成1mol五氯化磷放出93.0kJ热量,250s时生成n(PCl5)=0.40mol放出热量=0.40mol×93.0kJ/mol=37.2kJ,故答案为:37.2;
(4)a.反应前后气体总质量不变、容器体积不变,根据ρ=$\frac{m}{V}$知,无论反应是否达到平衡状态密度始终不变,故a正确;
b.所有的化学反应只要升高温度正逆反应速率都增大,所以该反应升高温度正逆反应速率都增大,故b正确;
c.350s 时,向该密闭容器中充入氮气,参加反应的各气体分压不变、浓度不变,则化学平衡不移动,故c错误;
d.相同条件下,若起始向该密闭容器中充入1.0molPCl3和0.2molCl2,与原反应相比,相当于减小压强平衡向气体体积增大的方向移动,则生成五氯化磷物质的量小于原来一半,故d正确;
故选abd;
(5)该反应的正反应是放热反应,升高温度化学反应速率加快,反应达到平衡时间缩短,但平衡逆向移动,达到平衡时五氯化磷体积分数降低,所以其图象为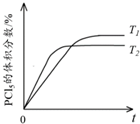 ,
,
故答案为: .
.
点评 本题考查化学平衡计算,为高频考点,侧重考查学生分析计算能力,注意“三段式”在化学平衡计算中的灵活运用,注意(4)中c选项充入氮气不影响平衡移动,为易错点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
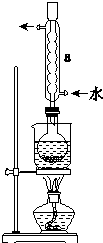 Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
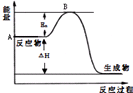 2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将待测液NaOH溶液取到锥形瓶后,露置空气中较长时间,以酚酞为指示剂测定 | |
| B. | 以甲基橙为指示剂,当甲基橙变红时停止滴定 | |
| C. | 移液管用蒸馏水冲洗后直接移取待测液 | |
| D. | 滴定终点读数时俯视 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
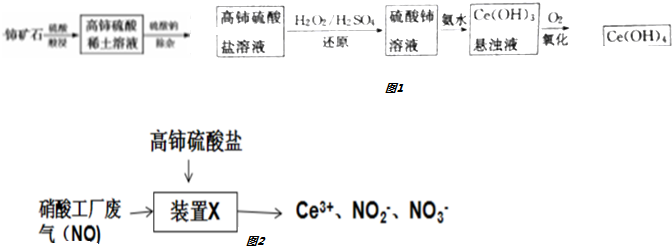
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
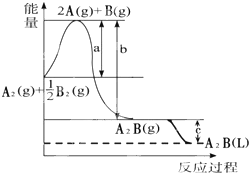 已知:A2(g)+$\frac{1}{2}$B2(g)═A2B(g),反应过程中能量变化如图,问:
已知:A2(g)+$\frac{1}{2}$B2(g)═A2B(g),反应过程中能量变化如图,问:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
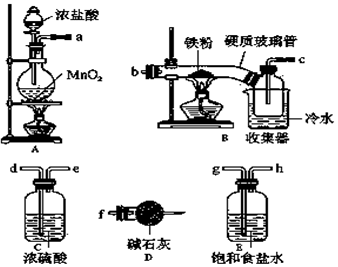
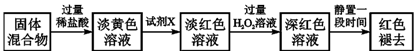
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
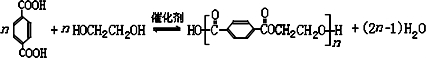
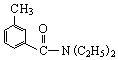 ; DEET在一定条件下,可通过下面的路线来合成:
; DEET在一定条件下,可通过下面的路线来合成: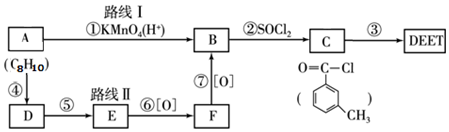
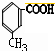 .
.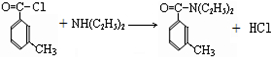 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 | |
| B. | 25℃时,在等体积、等浓度的硝酸中加入氨水,溶液的导电性增强 | |
| C. | 25℃时,0.1mol/L的硫化氢溶液与等浓度的硫化钠溶液的导电能力相当 | |
| D. | 25℃时,将等体积PH=1的盐酸和水混合,混合后溶液的PH=1.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com