
���� ���ɷ���ʽ��֪����Ӧǰ�����������������仯���ݴ˼��������������
�ڱ�״���£�����Ħ������M=Vm���ѣ��ݴ˼����������Ħ�����������������ݷ���ʽ��������ʵ���XY2���ټ���XY2��Ħ��������
�۸���XY2�����У���X��Y����Ԫ�ص�����֮��Ϊ3��16���Լ�XY2��Ħ����������X��Y�����ԭ�����������ж�Ԫ�����ͣ�
��� �⣺�ٱ����һ������Һ̬������XY2����һ����O2��ǡ����ȫȼ�գ��ɷ���ʽ��֪����Ӧǰ�����������������仯����Ӧ�������������Ĺ�ϵʽΪ1��1���ʷ�Ӧǰ���������Ϊ��V��O2��=672mL��
�ʴ�Ϊ��672��
�ڱ�״���£�����Ħ������M=Vm���ѣ����巴Ӧ���������Ħ������=22.4L/mol��2.56g/L=57.344g/mol��
672mL�����������ʵ���=$\frac{0.672L}{22.4L/mol}$=0.03mol��n��O2��=0.03mol����n��XY2��=0.01mol��
m��XY2��=m��������壩-m��O2��=0.03mol��57.344g/mol-0.03mol��32g/mol=0.76g
�ʻ�����XY2��Ħ������M��XY2��=$\frac{0.76g}{0.01mol}$=76g/mol��
�ʴ�Ϊ��76g/mol��
��XY2������X��Y��Ԫ�ص�������Ϊ3��16��
��1molXY2�к���X������Ϊ��76g��$\frac{3}{3+16}$=12g��Y������Ϊ��76g-12g=64g��
1molXY2���X1mol��Y2mol��
����X�����ԭ������Ϊ12��Y�����ԭ������Ϊ32����֪ԭ�Ӻ�������������������ͬ��
��XΪCԪ�أ�YΪSԪ�أ�
�ʴ�Ϊ��C��S��
���� ���⿼���˻���ﷴӦ�ļ��㣬��Ŀ�Ѷ��еȣ�ע����ݷ���ʽ������������������������������Ħ���������ܶȵĹ�ϵΪ���ؼ�������������ѧ���ķ�����������ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ�����N2��CO������������ΪNA | |
| B�� | 1.7 g H2O2�к��еĵ�����Ϊ0.9NA | |
| C�� | ��״���£�22.4L��������NA�����ʷ��� | |
| D�� | 1mol•L-1NaCl��Һ����NA��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 950mL ����ƿ | B�� | 500mL����ƿ | ||
| C�� | 1000mL ����ƿ | D�� | �����������ƿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪2NO2��g���TN2O4��g����H��298K��=-52.7kJ•mol-1��ij����С��Ϊ��̽���¶Ⱥ�ѹǿ�Ի�ѧƽ���Ӱ�죬������������ʵ�飺
��֪2NO2��g���TN2O4��g����H��298K��=-52.7kJ•mol-1��ij����С��Ϊ��̽���¶Ⱥ�ѹǿ�Ի�ѧƽ���Ӱ�죬������������ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ���� | B�� | ����ͭ��Һ | C�� | ����������Һ | D�� | ˮ�ܽ��/gA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 +2Na��
+2Na�� +H2��
+H2��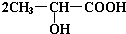 +Na2CO3��
+Na2CO3��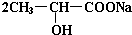 +H2O+CO2����
+H2O+CO2����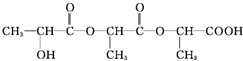

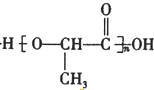
 $��_{��}^{Ũ����}$CH2=CHCOOH+H2O��
$��_{��}^{Ũ����}$CH2=CHCOOH+H2O���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com