
【题目】下列气体只能使用排水集气法收集的是
A. NO B. NH3 C. Cl2 D. NO2
科目:高中化学 来源: 题型:
【题目】A、B、C是三种元素的原子,质子数都小于18。A原子与B原子的最外层电子数都是6,A原子与C原子的核外电子层数都为3, C原子的质子数比A少4。回答下列问题:
(1)A、B、C的元素名称分别为________、________、________;
(2)A的离子结构示意图为________;
(3)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1mol AB42-的质量为104g,则元素B的该核素中的中子数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁:另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的物质的量浓度为
A. ![]() molL﹣1 B.
molL﹣1 B. ![]() molL﹣1
molL﹣1
C. ![]() molL﹣1 D.
molL﹣1 D. ![]() molL﹣1
molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,铁的氧化物、卤化物以及硫酸盐均为重要化合物。
(1)氧化铁为红棕色粉末,该物质难溶于水,易溶于盐酸中,请写出该物质与盐酸反应的离子方程式______________________________。
(2)铁在氯气中剧烈燃烧,产生红棕色的烟,将燃烧所得的三氯化铁溶于水,所得溶液的质量分数为16.25%,其密度为6.0g· mL-1,则该溶液中氯离子的物质的量浓度为________________;将上述所配制的溶液稀释为0.15mol/L 的稀溶液480mL,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管之外,还需要________________;量取该溶液的体积是_______________mL;在配制过程中如果定容时俯视刻度线,会造成所配溶液浓度________(填“偏高”、“偏低”或“无影响”)。
(3)将饱和FeCl3溶液滴入沸腾的蒸馏水中,可以制得Fe(OH)3胶体,请写出该过程的化学反应方程式_______________________,以下关丁Fe(OH)3胶体的说法中不正确的有_____________(填序号。
A. Fe(OH)3胶体是一种红褐色、澄清、透明的混合物
B. Fe(OH)3胶体中分散质的微粒直径在10-9m~10-7m 之间
C.用渗析法鉴别Fe(OH)3胶体和FeCl3 溶液,用丁达尔效应分离Fe(OH)3胶体和FeCl3 溶液
D.取少量Fe(OH)3胶体置于试管中,向试管中逐滴滴加稀硫酸,可看到先产生红褐色沉淀,随后沉淀溶解,最终得到黄色的溶液
E.将其装入U 形管内,用石墨作电极,接通直流电,通电一段时间后发现靠近正极区附近的颜色逐渐变深
(4)在硫酸铁溶液中,逐滴加入等浓度的氢氧化钡溶液,其溶液的导电性随氢氧化钡溶液体积增加而变化的图象是(_______)

查看答案和解析>>
科目:高中化学 来源: 题型:
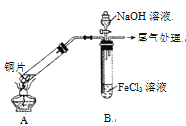
【题目】某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如右图所示(夹持仪器已略去)。
(1)实验前,应先检查装置的 ;实验中产生的尾气应通入 溶液进行处理。
(2)实验过程中需要配制100 mL l mo1·L-1 FeCl3溶液,所需要的玻璃仪器有:烧杯、量筒、玻璃棒、 ;实际配制过程中,常先将FeCl3固体完全溶于适量稀盐酸中,再加水稀释,此特殊操作的目的是____。
(3)该小组同学向5 mL l mo1·L-1 FeCl3溶液中通入足量的SO2,溶液最终呈浅绿色,写出其反应的离子方程式 。再打开分液漏斗活塞,逐滴加入煮沸冷却后的NaOH稀溶液,则试管B中产生的实验现象是 。
(4)该小组同学在(3)中实验时,发现溶液变为浅绿色需要较长时间,在此期间同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔效应,最终溶液呈浅绿色。
【查阅资料】Fe(HSO3)2+在溶液中呈红棕色且具有较强的还原性,能被Fe3+氧化为SO42-。则Fe(HSO3)2+与Fe3+在溶液中反应的离子方程式是 。
(5)若实验中用5 mL一定浓度的浓H2SO4与适量Cu片充分反应,实验结束后,测得产生SO2的体积在标准状况下为672 mL,向已冷却的A试管溶液中加入4 mo1·L-1的NaOH溶液30 mL时,恰好使Cu2+完全沉淀。则所用浓H2SO4浓度为____。(忽略过程中溶液的体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂和还原剂的物质的量之比最大的是().
A. 铜和稀硝酸 3Cu+8HNO3(稀)=2NO↑+3Cu(NO3)2+4H2O
B. 氯气和氨气 3Cl2+8NH3=N2+6NH4C1
C. 氢气和氧化铁 3H2+Fe2O3![]() 2Fe+3H2O
2Fe+3H2O
D. 二氧化锰和盐酸 MnO2+4HC1(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com