
【题目】已知短周期主族元素A、B、C、D、E的原子序数依次增加,五种元素中C的原子半径最大,B与E同主族,D的氧化物既能与酸反应也能与碱反应,E的氧化物是形成酸雨的主要原因,A与E形成的化合物是下水道中具有特殊气味的气体。下列说法正确的是
A. 1molA2B2中所含的共用电子对数目为3NA
B. A2E水溶液的电离方程式为A2E![]() 2A++E2-
2A++E2-
C. 最高价氧化物对应的水化物的酸性:D>E
D. 简单氢化物的热稳定性:B>E,是因为B的氢化物分子间含有氢键
科目:高中化学 来源: 题型:
【题目】实验室利用废弃旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验过程如图所示:

下列叙述错误的是( )
A. “溶解”操作中可用酸性条件下不断鼓入O2代替H2O2
B. 铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的H2O2
C. 与加入锌粉反应的离子为Cu2+、H+
D. “过滤”操作后,将滤液蒸干、高温灼烧即可制取纯净的ZnO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,改变0.1mol/L弱酸RCOOH溶液的pH,溶液中RCOOH分子的物质的量分数δ(RCOOH)随之改变[已知![]() ,甲酸(HCOOH)]与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
,甲酸(HCOOH)]与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是

A. 图中M、N两点对应溶液中的c(OH-)比较:前者>后者
B. 丙酸的电离常数K=10-4.88
C. 等浓度的HCOONa和CH3CH2COONa两种溶液的pH比较:前者>后者
D. 将0.1 mol/L的HCOOH溶液与0.1 mol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c(HCOO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VmLFe2(SO4)3溶液中含有Fe3+ag,取![]() mL溶液稀释到5VmL,则稀释后溶液中SO42﹣的物质的量浓度是
mL溶液稀释到5VmL,则稀释后溶液中SO42﹣的物质的量浓度是
A.![]() mol/LB.
mol/LB.![]() mol/L
mol/L
C.![]() mol/LD.
mol/LD.![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)xC(g),有图 I(T表示温度,P 表示压强,C%表示 C 的体积分数)所示的反应曲线,试判断对图 II 的说法中正确的是

A. 若 P3>P4,则 y 轴表示 B 的百分含量
B. 若 P3>P4,则 y 轴表示混合气体的平均摩尔质量
C. 若 P3<P4,则 y 轴表示 B 的体积分数
D. 若 P3<P4,则 y 轴表示混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在0.1mol/L的草酸(H2C2O4)溶液中加入等浓度的NaOH溶液,H2C2O4、HC2O4-、C2O42-三种微粒的物质的量分数(δ)与溶液pH的变化如图所示。下列说法不正确的是

A. 反应过程中c(H2C2O4)+c(HC2O4-)+c(C2O42-)<0.1mol/L
B. lg[K1(H2C2O4)]=-1.2
C. NaHC2O4溶液中c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)
D. 当NaOH溶液与H2C2O4溶液体积之比为3:2时,2c(Na+)+c(OH-)=2c(H2C2O4)+c(HC2O4-)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铜矿(主要成分是CuFeS2)为原料炼铜的方法为火法炼铜和湿法炼铜两种。
(1)火法炼铜时产生大量SO2,根据原电池原理,稀硫酸作电解质溶液,使用惰性电极,一极通入SO2,另一极通入O2,治理SO2污染,负极反应的离子方程式为___________________________。
(2)火法炼铜的过程中,电解出铜制备精铜时产生的废电解液中含有较多Ni2+和Pb2+,从废电解液中除去Pb2+的方法是往其中通入H2S至饱和,使Pb2+转化为硫化物沉淀(已知饱和H2S溶液中c(H2S)为0.1mol/L,![]() ≈10-20;Ksp(NiS)≈10-11)。若废电解液的pH=5,为保证不生成沉淀,Ni2+浓度应控制在_________mol/L以下。
≈10-20;Ksp(NiS)≈10-11)。若废电解液的pH=5,为保证不生成沉淀,Ni2+浓度应控制在_________mol/L以下。
(3)近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐。某工厂运用该原理生产铜和绿矾(FeSO4·7H2O)的工艺如图:

①写出反应的化学反应方程式:___________________________;如果对该反应进行高温加热,发现化学反应速率降低乃至反应停止,请简述理由:___________________________。
②固体A的成分为___________________________。
③欲从滤液中获得绿矾晶体,分离操作I因为_________、_________、过滤。
④写出反应湿法炼铜的化学反应方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a,b,c,d为四种由短周期元素构成的中性粒子,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为______________。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为________。人一旦吸入b气体后,就易引起中毒,是因为__________而中毒。
(3)c是双核单质,写出其电子式____________。c分子中所含共价键的类型为_______(填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是________________________。
(4)d是四核化合物,其结构式为______________;d分子内所含共价键有________个σ键,________个π键;σ键与π键的强度大小关系为σ___π(填“>”、“<”或“=”),原因是:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下列路线合成新抗凝(抗血栓药物)
新抗凝

已知:I:
II:
III:![]()
(1) 所需的试剂是__________。
所需的试剂是__________。
(2) B→C分两步进行,反应类型分别是 __________、__________。
(3)下列说法不正确的是_________。
a.化合物B能使Br2/CCl4褪色
b. 化合物C能发生银镜反应
c.F遇FeCl3溶液显色
d. 新抗凝的分子式C19H15NO6
(4)E+H→新抗凝的化学方程式是_______________________。
(5)已知:![]() ,写出有关化合物的结构简式I ________F________G________。
,写出有关化合物的结构简式I ________F________G________。
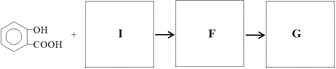
(6)写出一种符合下列条件的A的同分异构体的结构简式_____________________。
① 红外光谱表明分子中含有-COO-、苯环结构
② 1H-NMR谱显示苯环上有三种不同环境的H原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com