
【题目】下列反应中,不属于盐类水解反应的是
A.NH4+ + H2O ![]() NH3H2O + H+B.HCO3- + H2O
NH3H2O + H+B.HCO3- + H2O ![]() CO32- + H3O+
CO32- + H3O+
C.Al3+ + 3H2O![]() Al(OH)3 + 3H+D.S2-+ H2O
Al(OH)3 + 3H+D.S2-+ H2O ![]() HS- + OH-
HS- + OH-
 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】为了实现空间站的零排放,循环利用人体呼出的CO2并提供O2,我国科学家设计了如下图装置,反应完毕,电解质溶液的pH保持不变。下列说法正确的是
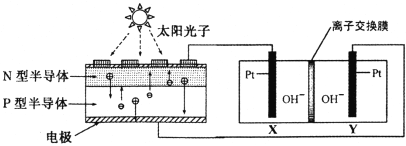
A. 图中N型半导体为正极,P型半导体为负极
B. Y 电极的反应:4OH--4e-=2H2O +O2↑
C. 图中离子交换膜为阳离子交换膜
D. 该装置实现了“太阳能→化学能→电能”的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近几年,节能减排、提高原料利用率来提高经济效益成为人们关注的焦点。某化工厂利用甲烷与氯气反应得到的副产品来制取盐酸实现了变废为宝的梦想,其生产原理可在实验室中模拟如图,请根据要求填空:

(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③__________。
(2)设![]() =x,若理论上欲获得最多的氯化氢,则x值应_________。
=x,若理论上欲获得最多的氯化氢,则x值应_________。
(3)在C装置中,经过一段时间的强光照射后,发现硬质玻璃管内壁附着有油珠,生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应化学方程式为2CHCl3+O2![]() 2COCl2+2HCl,上述反应__________ (填选项符号,下同)。
2COCl2+2HCl,上述反应__________ (填选项符号,下同)。
A.属于取代反应 B.不属于取代反应
为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是____________。
A.氢氧化钠溶液 B.硝酸银溶液
C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
(4)D装置的石棉中均匀混有KI粉末,其作用是___________。
(5)E装置的作用是____________ (填编号)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(6)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为_____________;该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为_____ (填编号)。
①CH4 ②CH3Cl ③CH2Cl2 ④CHCl3 ⑤CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应N2 ( g ) +3H2 ( g ) = 2NH3 ( g ) ,反应过程的能量变化如图所示。已知N2 ( g ) 与 H2( g )反应生成 17 gNH3(g),放出46. 1kJ的热量。请回答下列问题:
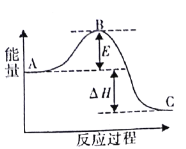
(1)该反应通常用铁作催化剂,加催化剂会使图中E_______________(填“变大”或“变小”) ,E 的大小对该反应的反应热有无影响?___________,理由是__________。
(2)图中△H=________kJ·mol -1。
(3)起始充入2mol·L-1N2和5.5mol·L-1H2,经过50min,NH3的浓度为1mol·L-1,则v(N2)=______mol·L-1·min-1,c(H2)=_____mol·L-1
(4)已知NH3(g)=NH3(l) △H=-QkJ·mol-1,则N2 ( g ) +3H2 ( g ) = 2NH3 ( l )的△H=_______kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,已知醋酸的电离常数Ka=1.6×10-5,醋酸银的溶度积Ksp(CH3COOAg)=3.7×10-3。下列有关说法正确的是
A. 醋酸溶液中,c(CH3COO-)>c(H+)>c(OH-)
B. 将相同浓度的CH3COOH溶液与CH3COO Na溶液等体积混合,所得溶液呈碱性
C. 该温度下,1mol/L的醋酸溶液中,醋酸的电离度为0.4%
D. 该温度下,浓度均为0.02mol/L的CH3COONa溶液和AgNO3溶液等体积混合(忽略混合后溶液体积的变化),有CH3COOAg沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:![]()
已知转化过程中的反应为2CrO42﹣(aq)+2H+(aq)![]() Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是( )
Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是( )
A. 溶液颜色保持不变,说明上述可逆反应达到平衡状态
B. 若用绿矾(FeSO4·7H2O)作还原剂,处理1L废水,至少需要917.4 g
C. 常温下转化反应的平衡常数K=l×1014.则转化后所得溶液的pH=6
D. 常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g) = 4NO(g)+6H2O(g) 在2 L的密闭容器中进行,1分钟后,NH3减少了0.12 mol,则平均每秒钟各物质浓度变化正确的是
A.NO:0.001 mol·L-1B.H2O:0.002 mol·L-1
C.NH3:0.002 mol·L-1D.O2:0.001 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)SiO2是玻璃的成分之一,SiO2与氢氧化钠溶液反应的化学方程式为___,工艺师常用___(填物质名称或化学式)来雕刻玻璃。
(2)用Na2SiO3溶液浸泡过的棉花不易燃烧,体现Na2SiO3的用途可作___的原料。
(3)工业上常用2C+SiO2![]() Si+2CO↑制备硅单质,该反应中有元素化合价升高的物质是___(填化学式,下同),氧化剂是___。
Si+2CO↑制备硅单质,该反应中有元素化合价升高的物质是___(填化学式,下同),氧化剂是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。

回答下列问题:
(1)图B对应的物质名称是_________,其晶胞中的原子数为______,晶体类型为_______。
(2)d中元素的原子核外电子排布式为_______。
(3)图A中由二种元素组成的物质中,沸点最高的是______,原因是______,该物质的分子构型为_________,中心原子的杂化轨道类型为_________。
(4)图A中的双原子分子中,极性最大的分子是_________。
(5)k的分子式为_________,中心原子的杂化轨道类型为_________,属于_________分子(填“极性”或“非极性”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com