
【题目】合成氨反应N2 ( g ) +3H2 ( g ) = 2NH3 ( g ) ,反应过程的能量变化如图所示。已知N2 ( g ) 与 H2( g )反应生成 17 gNH3(g),放出46. 1kJ的热量。请回答下列问题:
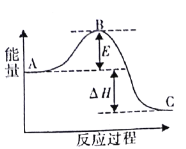
(1)该反应通常用铁作催化剂,加催化剂会使图中E_______________(填“变大”或“变小”) ,E 的大小对该反应的反应热有无影响?___________,理由是__________。
(2)图中△H=________kJ·mol -1。
(3)起始充入2mol·L-1N2和5.5mol·L-1H2,经过50min,NH3的浓度为1mol·L-1,则v(N2)=______mol·L-1·min-1,c(H2)=_____mol·L-1
(4)已知NH3(g)=NH3(l) △H=-QkJ·mol-1,则N2 ( g ) +3H2 ( g ) = 2NH3 ( l )的△H=_______kJ·mol-1
【答案】变小 无 ΔH取决于反应物的总能量和生成物的总能量差 -92.2 0.01 4 -(92.2+2Q)
【解析】
(1)依据催化剂降低反应的活化能加快反应速率分析;反应热取决于反应物和生成物的能量变化,活化能和反应热无关;
(2)结合已知N2(g)与H2(g)反应生成17gNH3(g),放出46.1kJ的热量,分析图象是合成氨反应N2(g)+3H2(g)=2NH3(g),计算得到;
(3)依据化学平衡三段式列式计算;
(4)结合(2)计算的焓变写出反应的热化学方程式,依据盖斯定律计算所需让化学方程式。
(1)催化剂降低反应的活化能加快反应速率,但不改变平衡,反应热不变,E的大小对该反应的反应热无影响,反应热取决于反应物的总能量和生成物的总能量差,故答案为:变小;无;△H取决于反应物的总能量和生成物的总能量差;
(2)已知N2(g)与H2(g)反应生成17gNH3(g),放出46.1kJ的热量,图象是表示的是反应N2(g)+3H2(g)=2NH3(g)能量变化,所以生成34g氨气放热92.2kJ,热化学方程式为:N2(g)+3H2(g)=2NH3(g),△H=-92.2kJ/mol,故答案为:-92.2;
(3)起始充入2molL-1N2和5.5molL-1H2,经过50min,NH3的浓度为1molL-1,则依据所给数据建立如下三段式:
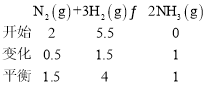
由三段式可得v(N2)=![]() =0.01mol/(Lmin),c(H2)=4mol/L,故答案为:0.01;4;
=0.01mol/(Lmin),c(H2)=4mol/L,故答案为:0.01;4;
(4)由热化学方程式①N2(g)+3H2(g)=2NH3(g)△H=-92.2kJ/mol,②NH3(g)═NH3(l)△H=-QkJmol-1,依据盖斯定律①+②×2得到N2(g)+3H2(g)═2NH3(l)△H=-(92.2+2Q)kJmol-1,故答案为:-(92.2+2Q)。


科目:高中化学 来源: 题型:
【题目】某同学按右图所示的装置进行实验。 A、B为两种常见金属,它们的硫酸盐可溶于水。当 K 闭合时,在交换膜处 SO42-从右向左移动。下列分析正确的是

A.溶液中A2+浓度减小
B.B 的电极反应: B-2eˉ=B2+
C.y 电极上有 H2产生,发生还原反应
D.反应初期,x电极周围出现白色胶状沉淀,不久沉淀溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院深圳先进技术研究院研发出一种新型铝一石墨烯双离子电池(AGDIB电池),该电池以溶有六氟磷酸锂![]() 的碳酸酯类溶剂为电解液放电时合金
的碳酸酯类溶剂为电解液放电时合金![]() 发生去合金化反应阴离子
发生去合金化反应阴离子![]() 从石墨烯C中脱嵌进入电解质溶液。放电时其工作原理如图所示,下列说法错误的是( )
从石墨烯C中脱嵌进入电解质溶液。放电时其工作原理如图所示,下列说法错误的是( )

A.该电池不能用水作为电解质溶液
B.放电时,a电极的电极反应式为Li-e-=Li+
C.废旧AGDIB电池进行“放电处理”时,若转移1mole-,则可回收7gLi
D.充电时,b电极的电极反应式为PF6--e-+Cx=CxPF6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说祛错误的是( )
A.铅蓄电池在放电过程中,负极质量减小,正极质量增加
B.强电解质在液态时,有的导电,有的不导电
C.反应速率常数与浓度无关,但受温度、催化剂、固体表面性质等因素的影响
D.温度一定,当溶液中Ag+和Cl-浓度的乘积等于Ksp时,溶液为AgCl的饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t℃时AgCl的Ksp=4×10-10,下列说法中不正确的是( )
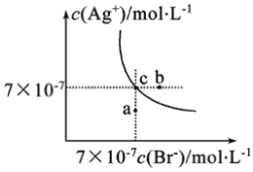
A.在t℃时,AgBr的Ksp为4.9×10-13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K≈816
AgBr(s)+Cl-(aq)平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大
B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
C.在高锰酸钾溶液中,H+、K+、SO42-、葡萄糖分子可以大量共存
D.已知:Ksp(AgCl)=1.8×10-10, Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4的溶解度小于AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于盐类水解反应的是
A.NH4+ + H2O ![]() NH3H2O + H+B.HCO3- + H2O
NH3H2O + H+B.HCO3- + H2O ![]() CO32- + H3O+
CO32- + H3O+
C.Al3+ + 3H2O![]() Al(OH)3 + 3H+D.S2-+ H2O
Al(OH)3 + 3H+D.S2-+ H2O ![]() HS- + OH-
HS- + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量A、B混合气体发生反应:aA(g)+bB(g)![]() cC(g)。平衡时测得A的浓度为0.5mol/L;保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度为0.28mol/L。下列有关判断正确的是
cC(g)。平衡时测得A的浓度为0.5mol/L;保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度为0.28mol/L。下列有关判断正确的是
A. a+b=cB. 该变化使平衡正向移动
C. B的转化率降低D. C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的Fe2+含量,请写出酸性条件下K2Cr2O7与Fe2+反应的离子方程式_________(K2Cr2O7被还原为Cr3+)。
(2)若需配制浓度为0.010 00 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取K2Cr2O7________ g(保留四位有效数字,已知M(K2Cr2O7)=294.0 g·mol-1)。配制该标准溶液时,下列仪器一定不会用到的有________。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤250mL容量瓶 ⑥胶头滴管 ⑦托盘天平
(3)若配制K2Cr2O7标准溶液时,俯视刻度线,则测定结果________(填“偏大”、“偏小”或“不变”,下同);滴定操作中,若滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则滴定结果将____________________________。
(4)用0.010 00 mol·L-1的K2Cr2O7溶液滴定20.00 mL未知浓度的含Fe2+的溶液。恰好完全反应时消耗10.00 mL K2Cr2O7溶液,则溶液中Fe2+的物质的量浓度是多少?_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com