
����Ŀ���±��������Ԫ�����ڱ���һ����Ԫ�أ��ش��������⣺
A | B | C | |||||||||||||||
D | E | F | G | H | I | J | K | ||||||||||
M |
(1)��ϡ�����������������ԭ�Ӱ뾶��С����_____(��Ԫ�ط���)
(2)��������ĸ�����12��Ԫ���У���ѧ��������õ���_____(��Ԫ�ط��ű�ʾ����ͬ)����������ǿ����___(��Ԫ�ط��ű�ʾ)�����ڹ���Ԫ�ص���___(�ÿո��ñ��е���ĸ��ʾ)
(3)��A������⻯��Ϊȼ�ϣ�D������������Ӧˮ����Ϊ�������Һ��ȼ�ϵ�أ��为���缫��ӦʽΪ_____
(4)D��FԪ������������Ӧˮ�������Ӧ�����ӷ���ʽΪ_____________
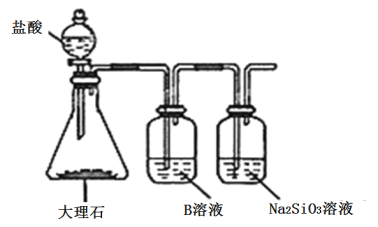
(5)Ϊ�Ƚ�Ԫ��A��G�ķǽ�����ǿ������ͼ��ʾװ�ý���ʵ��(�г���������ȥ��װ������������)����ҺBӦ��ѡ��_____��Һ��������_________����˵��A��G�ǽ�����ǿ���Ļ�ѧ����ʽ�ǣ�______________��
���𰸡�Cl Ar Na M CH4-8e-+10OH- =CO32-+7H2O Al(OH)3+OH���TAlO2��+2H2O ����NaHCO3 ��ȥCO2�е�HCl���� CO2+H2O+Na2SiO3��Na2CO3+H2SiO3��
��������
����Ԫ�����ڱ���AΪCԪ�أ�BΪOԪ�أ�CΪFԪ�أ�DΪNaԪ�أ�EΪMgԪ�أ�FΪAlԪ�أ�GΪSiԪ�أ�HΪPԪ�أ�IΪSԪ�أ�JΪClԪ�أ�KΪArԪ�أ�MΪMnԪ�أ��ݴ˷�����
��1�����������г�ϡ������Ԫ���⣬ԭ�Ӱ뾶��С��ΪClԪ�أ�
��2����12��Ԫ������������õ���ArԪ�أ���������ǿ����NaԪ�أ����ڹ��Ƚ�������MnԪ�أ�
��3��A�ļ��⻯��ΪCH4��D������������Ӧˮ����ΪNaOH����ԭ�ϵ�صĸ�������ʽΪCH4-8e-+10OH-=CO32-+7H2O��
��4��D��FԪ������������Ӧˮ����ֱ�ΪNaOH��Al(OH)3������߷�����Ӧ�����ӷ���ʽΪAl(OH)3+OH-=AlO2-+2H2O��
��5��Ϊ�Ƚ�Ԫ��A��G�ķǽ�����ǿ������ҺBӦ��ѡ�ñ���NaHCO3��Һ�������dz�ȥCO2�е�HCl���ʣ���˵��A��G�ǽ�����ǿ���Ļ�ѧ����ʽ��CO2+H2O+Na2SiO3��Na2CO3+H2SiO3����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����2L���ܱ������з���4molN2O5���������·�Ӧ:2N2O5(g)![]() 4NO2(g)+O2(g)����Ӧ��5minʱ�����N2O5ת����20%����v(NO2)Ϊ___��c��N2O5��Ϊ___��O2�����ʵ���Ũ��Ϊ___��
4NO2(g)+O2(g)����Ӧ��5minʱ�����N2O5ת����20%����v(NO2)Ϊ___��c��N2O5��Ϊ___��O2�����ʵ���Ũ��Ϊ___��
��2��ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��仯��������ͼ��ʾ������ͼ��������գ�

�ٸ÷�Ӧ�Ļ�ѧ����ʽΪ___��
�ڷ�Ӧ��ƽ��ʱ��v��X��Ϊ___��c��Z��Ϊ___��
����X��Y��Z��Ϊ���壬���ƽ��ʱ�������ڻ�������ƽ����Է�����������ʼͶ��ʱ___(��������������С�����������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ԫ�ط��Ż�ѧʽ��ջش��������⣺
���� ���� | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
������ЩԪ���У�����õķǽ���Ԫ����___________����ѧ��������õ�Ԫ����______________��
�Ʊ��н�������ǿ��Ԫ����_______________����ԭ�ӽṹʾ��ͼΪ _______________________ ��
�DZ���Ԫ�ص�����������Ӧ��ˮ������������ǿ����__________�������Ե�����������______��
��Ԫ�آ��Ԫ�ط���Ϊ ____________ ��Ԫ�آߵ�ԭ����Ϊ_________��
���ڢ١���Ԫ���У�ԭ�Ӱ뾶������_____________��ԭ�Ӱ뾶��С����_____________��
��ʮ��Ԫ������һ��Ԫ�ص��⻯��ˮ��Һ�ʼ��ԣ����⻯��ĵ���ʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������зḻ��ʳƷ���������Դ��ҩ���ˮ����Դ����ͼΪ��ˮ���õIJ��ֹ��̡�
�����й�˵����ȷ����
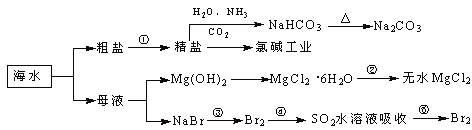
A. �������г�ȥ�����е�SO42-��Ca2����Mg2����Fe3�������ʣ������ҩƷ˳��Ϊ��Na2CO3��Һ��NaOH��Һ��BaCl2��Һ�����˺������
B. �ó����ʯ��ˮ�ɼ���NaHCO3��Na2CO3
C. �������нᾧ����MgCl2��6H2OҪ��HCl��Χ�м�����ˮ�Ƶ���ˮMgCl2
D. ��ҵ��ͨ����ⱥ��MgCl2��Һ��ȡ����þ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Fe3+��Fe2+����ʵ���˵���������

A. ����ͼװ�ÿ����Ʊ�����Fe(OH)2
B. ����FeCl3��Һʱ���Ƚ��Ȼ����������ڽ�Ũ�������У��ټ�ˮϡ�͵�����Ҫ��Ũ��
C. FeCl3��Һ�еμ�KSCN��Һ�����ɺ�ɫ����
D. ��FeCl2��Һ�м�������������Ϊ�˷�ֹFe2+������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(NH3��BH3)��ؿ��ڳ����¹�����װ����ͼ��ʾ��δ���백����֮ǰ��������������ȣ���ط�ӦΪNH3��BH3��3H2O2==NH4BO2��4H2O ����֪H2O2����������˵����ȷ����(����)

A. �����ĵ缫��ӦʽΪ2H����2e��===H2��
B. ��ع���ʱ��H��ͨ�����ӽ���Ĥ���ƶ�
C. ��ع���ʱ�����������ֱ�ų�H2��NH3
D. �����㹻��ʱ���������������������Ϊ1.9 g�����·��ת��0.6 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����и��������У�A.O2��O3 B.12C��13C C.H2O��D2O
___�������ʻ�Ϊͬλ�أ�___�������ʻ�Ϊͬ�������塣
��2����ҵ����![]() ��ԭ����ȡ���ᣬҪ����������Ҫ��Ӧ����д���ڶ����͵�������Ӧ�Ļ�ѧ����ʽ��
��ԭ����ȡ���ᣬҪ����������Ҫ��Ӧ����д���ڶ����͵�������Ӧ�Ļ�ѧ����ʽ��
��һ����Ӧ��4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
�ڶ�����Ӧ��___��
��������Ӧ��___��
��3�����������������������ֳ�����������д�ڿհ״���
��ϡ������ϴ����___��
�����ڳ����ձ��е�Ũ������������__��
Ũ�������ֽ��ʱ��ֽ��ڡ�__��
��ͭƬ�����ȵ�Ũ������ʱ��������ų���___��
��4���������գ����������У���PH3 ��H2O2 ��Na2O2 ��KOH ��(NH4)2SO4 ��F2
ֻ�����ۼ�����___���Ⱥ����Ӽ��ֺ����Լ�����___���Ⱥ����Ӽ��ֺ��Ǽ��Լ�����___��
��5�����з�Ӧ�У����ڷ��ȷ�Ӧ����___(�����)��
������ʯ��ʯ(��Ҫ�ɷ���CaCO3)����ʯ��(CaO)
��Ba(OH)2��8H2O��NH4Cl����ķ�Ӧ
��ըҩ��ը
���������кͷ�Ӧ
����ʯ����ˮ��������ʯ��
��ʳ��������������
���Ҵ�ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���绯ѧ���ճ���������;�㷺��ͼ����ԭ��أ�����ܷ�ӦΪMg+ClO-+H2O=Cl-+ Mg(OH)2��ͼ���ǵ��أ����ں�Cr2O72-�Ĺ�ҵ��ˮ�Ĵ���������˵���������
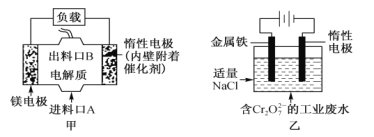
A. ͼ���з�����������Ӧ��Mg��2e-=Mg2+
B. ͼ���ж��Ե缫�����ص��������缫������H2�ų�
C. ͼ����Cr2O72-����Ե缫�ƶ����ü�������Cr(OH)3����
D. ��ͼ����Ϊͼ�ҵĵ�Դ��������3.6gþʱ��������Ҳ����8.4g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪij�ӵ��α�ǩ��һ���֡�

��֪����KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
��I2+2Na2S2O3=2NaI+Na2S4O6����ɫ��
ijͬѧ�붨���ⶨ�˼ӵ����е�Ԫ�صĺ�������������ʵ����
����1����ȡag����ʳ�Σ������Һ��ȫ��ת������ƿ�У�������������KI��Һ�����뼸��ϡ���ᣬ��Һ���ɫ���ټ���3�ε�����Һ��
����2��ȡһ֧50mL��ʽ�ζ��ܣ���bmol��L-1������Na2S2O3 ��Һ��ϴ2��3�κ�װ����Һ������Һ��߶���0�̶ȡ�
����3����ʼ�ζ�ֱ���յ㣬�ظ�����2��3�Σ�ʵ�����ݼ�¼���£�

��1����һ�ζ���Ϊ mL��
��2���ζ��յ���жϷ��� ��
��3���������㣬�˵�����Ԫ���ĺ���Ϊ mg��kg-1���ú�a��b��������ʽ��ʾ�� ��
��4�����в������ܻᵼ�²������ƫ�͵��� ��
A������1�г�ȡʳ��ʱ������������̣�ʳ�η��ڷ������̣��������Ϊ0.5g
B������1����ʳ����Һδ��ȫת������ƿ
C������2�еζ���ϴ�Ӻ�δ��ϴ
D������3�ζ�ǰ�ζ��ܼ��촦�����ݣ��ζ���������ʧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com