
【题目】短周期中三种元素a、b、c在周期表中的位置如图所示,下列有关这三种元素的说法正确的是
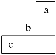
A. a是一种活泼的非金属元素B. b的气态氢化物比c的稳定
C. c的氧化物对应的水化物是强酸D. b元素的最高化合价为+7价
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知反应A2(g)+2B2(g)![]() 2AB2(g) ΔH<0,下列说法正确的是( )
2AB2(g) ΔH<0,下列说法正确的是( )
A. 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
B. 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
C. 升高温度有利于反应速率增加,从而缩短达到平衡的时间
D. 升高温度,正向反应速率增加,逆向反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置(夹持仪器省略)进行实验,将液体A逐渐加入固体B中。回答下列问题:
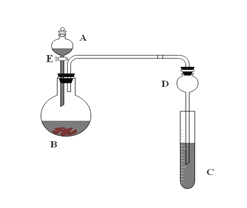
(1)图中D装置在实验中的作用____________________;
(2)若A中为浓盐酸,B中为高锰酸钾,C中盛有KI淀粉溶液,旋开E后,C中的现象是溶液变蓝色,试写出A与B反应的化学方程式_________________________:
(3)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E足够长的时间后,C中的现象是____________________,C中发生反应的化学方程式为:__________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5 mL 0.005 mol·L-1 FeCl3溶液和5 mL 0.015 mol·L-1 KSCN溶液混合。达到平衡后溶液呈红色。再将混合液等分为5份,分别进行如下实验:
| 实验①:滴加4滴水,振荡 |
实验②:滴加4滴饱和FeCl3溶液,振荡 | |
实验③:滴加4滴1 mol·L-1 KCl溶液,振荡 | |
实验④:滴加4滴1 mol·L-1 KSCN溶液,振荡 | |
实验⑤:滴加4滴6 mol·L-1 NaOH溶液,振荡 |
下列说法不正确的是
A. 对比实验①和②,为了证明增加反应物浓度,平衡发生正向移动
B. 对比实验①和③,为了证明增加生成物浓度,平衡发生逆向移动
C. 对比实验①和④,为了证明增加反应物浓度,平衡发生正向移动
D. 对比实验①和⑤,为了证明减少反应物浓度,平衡发生逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.明矾、小苏打、醋酸、次氯酸均为电解质
B.碘酒、牛奶、豆浆、漂白精均为胶体
C.根据是否具有丁达尔现象可将分散系分为溶液、胶体和浊液
D.物质可根据在水中或熔化状态下的导电性分为电解质与非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关卤素的说法不正确的是
A. ICl在反应ICl+2NaOH![]() NaCl+NaIO+H2O中作氧化剂
NaCl+NaIO+H2O中作氧化剂
B. 金属钠与氯气反应生成氯化钠后,其结构的稳定性增强,体系的能量降低
C. 淀粉碘化钾在空气中变蓝,发生了4I-+ O2 + 2H2O![]() 2I2 + 4OH-
2I2 + 4OH-
D. HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组学习了亚铁盐的性质后,欲探究FeSO4溶液分别与Na2CO3溶液、NaHCO3溶液的反应。已知:Fe(OH)2和FeCO3均为白色沉淀,不存在Fe(HCO3)2。实验操作及现象记录如下:
实验 | 试剂 | 操作及现象 | ||
试管(I) | 试管(II) | |||
(试管容积为50 mL) | 实验a | 1.0 mol·L-1 FeSO4溶液 24 mL | 1.0 mol·L-1 Na2CO3溶液24mL | 倾倒完后,迅速用胶塞塞紧试管I的口部,反复上下颠倒摇匀,使反应物充分混合 反应过程中无气泡产生,生成白色絮状沉淀 放置1.5~2 h后,白色絮状沉淀转化为白色颗粒状沉淀 |
实验b | 1.0 mol·L-1 FeSO4溶液 10 mL | 1.0 mol·L-1 NaHCO3溶液 20 mL | 倾倒完后,迅速产生白色颗粒状沉淀和大量气泡。振荡,经2~4 min后液面上方试管内壁粘附的白色颗粒状沉淀物变成红褐色 | |
(1)甲同学认为实验a中白色颗粒状沉淀是FeCO3,写出该反应的离子方程式:________;他为了证实自己的观点,进行实验:取少量白色颗粒状沉淀,加入________,发现产生大量气泡。
(2)乙同学推测实验a的白色颗粒状沉淀中还可能含有Fe(OH)2,他将实验a中两种溶液体积均改成15 mL后再进行实验,证实了他的推测。能证明Fe(OH)2存在的实验现象是_________。
(3)实验b中白色颗粒状沉淀主要成分也为FeCO3,写出生成FeCO3的离子方程式:________。
(4)实验b中液面上方试管内壁粘附的白色颗粒状沉淀物变成红褐色,主要原因是潮湿的FeCO3被氧气氧化,写出该反应的化学方程式:__________。
(5)乙同学反思,实验a中含有Fe(OH)2,实验b中几乎不含有Fe(OH)2,对比分析出现差异的原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表各组物质之间通过一步反应不可以实现如下图所示转化关系的是
选项 | X | Y | Z | 对应过程的反应条件 |
A | SiO2 | Na2SiO3 | H2SiO3 | ①Na2CO3熔融 |
B | NaOH | NaHCO3 | Na2CO3 | ②加热 |
C | N2 | NO2 | HNO3 | ③加热 |
D | C | CO | CO2 | ④灼热炭粉 |
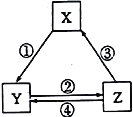
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com