
【题目】在粗盐提纯的实验中,蒸发时正确的操作是( )
A.把浑浊的液体倒入蒸发皿内加热
B.开始析出晶体后用玻璃棒搅拌
C.待水分完全蒸干后停止加热
D.蒸发皿中出现大量固体时即停止加热
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是优秀的水处理剂,具有很强的氧化性,氧化能力优于氯气和臭氧,溶于水中能有效杀灭水中的微生物和藻类,还能氧化分解各种有机、无机污染物,如酚、有机氮、硫化物、氰化物等,而且在整个净化过程中不会产生三氯甲烷、氯代酚等二次污染物。工业上常用次氯酸钠氧化法和电解法先制得高铁酸钠后再与氢氧化钾饱和溶液反应制备高铁酸钾。
I.电解法采用氢氧化钠作电解质溶液,铁丝网和石墨作电极材料,先制得高铁酸钠,请判断铁丝网作_______极, 阴极产生气体是__________。
II.次氯酸钠氧化法制备高铁酸钾简要流程如下:

(1)写出在碱性条件下过程①反应的离子方程式:___________________________________。
(2)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因:______________________________________。
(3)K2FeO4溶于水后,会慢慢放出气体,并杀菌消毒,净化水中悬浮杂质,写出它和水反应的离子方程式_______________________________________________________。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用___________(填序号)。
A.H2O B.稀KOH溶液、异丙醇
C.KCl溶液、异丙醇 D.Fe(NO3)3溶液、异丙醇
(4)K2FeO4溶于水后,会水解生成如下图中的物种,纵坐标表示其分布分数,则下列说法不正确的是________________。
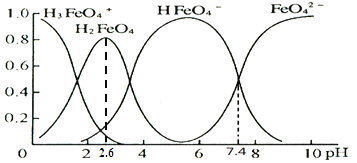
A.FeO42+H2OHFeO4+OH的平衡常数为107.4
B.从pH=1到pH=2.6,H2FeO4的分布分数逐渐增大
C.向pH=6的该溶液中加KOH溶液,反应的离子方程式为HFeO4+ OH = FeO42+H2O
D.根据图中信息,铁元素有4种存在形态,它们总是可以同时大量存在
(5)可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式为:
①FeO42+CrO2 +2H2O=CrO42+Fe(OH)3↓+OH
②2CrO42+2H+=Cr2O72+H2O
③Cr2O72+6Fe2++14H+=2Cr3++6Fe3+ +7H2O
现称取1.980g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤,滤液定容于250 mL容量瓶中。每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为21.90 mL。则上述样品中高铁酸钾的质量分数为______________。(保留四位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如下表:
物质 | 熔点/℃ | 性质 |
H2C2O4 | 189.5 | 有毒,具有腐蚀性,易溶于水,二元弱酸,比醋酸酸性强,100℃开始升华,157℃时开始分解.草酸与浓硫酸混合加热产生CO2,CO和H2O.草酸钙和草酸氢钙均为白色难溶物 |
[实验一]根据下图提供的仪器和试剂(可重复使用),设计实验证明草酸与浓硫酸混合加热产物中含有CO2和CO(部分夹持仪器和加热装置省略)。

(1)仪器接口依次连接的合理顺序为a→____________________________.
(2)用上图提供的仪器和试剂做实验时,首次使用的装置B中出现白色浑浊,并不能说明草酸受热分解产物中一定有CO2,请你提出改进意见:__________________.
(3)利用改进后的装置进行实验时,要先加热______装置(填装置标号,下同)后加热______装置.
[实验二]利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.
(4)实验时,先分别量取两种溶液,然后倒入试管中,迅速振荡混匀并开始计时,通过测定溶液褪色所需的时间来判断反应的快慢.该小组设计了如下的方案:
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
浓度/ mol·L-1 | 体积/mL | 浓度/ mol·L-1 | 体积/mL | ||
1 | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
2 | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
3 | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
①已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需满足的关系为n(H2C2O4)/n(KMnO4) ≥__________.
②探究温度对化学反应速率影响的实验编号是__________,探究反应物浓度对化学反应速率影响的实验编号是__________.
③已知50℃时c(MnO![]() )-t(反应时间)的变化曲线如图.若保持其他条件不变,请在图中画出25℃时c(MnO
)-t(反应时间)的变化曲线如图.若保持其他条件不变,请在图中画出25℃时c(MnO![]() )-t的变化曲线示意图并注明温度.
)-t的变化曲线示意图并注明温度.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氢弥猴桃内酯(J)是一种调配烟草用香精,制备该物质的合成路线如下:

已知:A、B、C中含有一种相同的官能团,B和C中均含有两个甲基。
(1)A的化学名称是_________;Ⅰ中所含官能团的名称是_________。
(2)A生成B或C的反应类型是_________,G生成H的反应类型是_________。
(3)A在催化剂作用下发生加聚反应,生成的常见高分子化合物的结构简式为_________。
D生成E所用的试剂为乌洛托品,其相对分子质量为140,可由甲醛与氨气以物质的量之比3∶2反应脱去水得到,乌洛托品分子中有4个六元环,所有氢原子化学环境相同,乌洛托品的分子式为_________,结构简式为_____________________________。
(4)化合物E与足量H2 在催化剂及加热条件下反应的化学方程式为________________________。
(5)芳香族化合物X是J 的同分异构体,1mol X能与2mol NaOH 反应,X的核磁共振氢谱有5组峰,且峰面积之比为1∶1∶2∶6∶6,写出一种符合条件的X的结构简式:__________________。
(6)写出以1-丙醇为原料(其他试剂任选)制备2-丁烯酸的合成路线____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茅台酒中存在少量具有凤梨香味的物质X,其结构如图所示。下列说法正确的是

A. X难溶于乙醇
B. 酒中的少量丁酸能抑制X的水解
C. X的分子式为C6H10O2
D. 分子式为C4H8O2且官能团与X相同的物质共有5种(不考虑立体异构)
【答案】B
【解析】X是醇,易溶于酒精,故A错误;X水解产物是丁酸,所以丁酸能抑制X的水解,故B正确;X的分子式为C6H12O2,故C错误;分子式为C4H8O2且官能团与X相同的物质有HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3COOCH2CH3、CH3CH2COOCH3共4种,故D错误。
【题型】单选题
【结束】
5
【题目】W、X、Y、Z为原子序数依次增大的短周期主族元素,W、X处于不同周期,原子的最外层电子数X比Y多一个但比Z少一个,原子的电子层数X比Y、Z少一层。下列说法正确的是
A. 原子半径的大小为:Z>Y>X>W
B. 若Y、Z的核电荷数之和为X的4倍,则X、Z的气态氢化物的沸点:前者低于后者
C. 元素的非金属性:Y>Z
D. 若X的单质为常见的非金属导体,则Y的简单离子能破坏水的电离平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是__________,装置B中玻璃棒的作用是__________,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中①的名称是__________,①中加入沸石的作用是______________,冷却水的方向是_________。装置D在分液时为使液体顺利滴下,应进行的具体操作是_________。
(3)从氯化钠溶液中得到氯化钠固体,选择装置__________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置__________。检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加________,不产生白色沉淀表明Cl-已除净。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是( )
A. 电子层序数越大,s原子轨道的形状相同、半径越小
B. 在同一电子层上运动的电子,其自旋方向肯定不同
C. 镁原子由1s22s22p63s2→ls22s22p63p2时,原子吸收能量,由基态转化成激发态
D. 原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com