
【题目】下列的图示与对应的叙述相符的是( )
A.如图表示向A1Cl3溶液中滴加NaOH溶液时n [Al(OH)3]的变化情况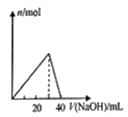
B.如图表示KNO3的溶解度曲线,图中a点表示的溶液通过升温可以得到b点
C.如图表示某一放热反应,若使用催化剂,E1、E2、△H都会发生改变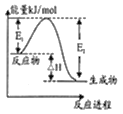
D.如图表示向Na2CO3溶液中滴加稀盐酸时,产生n (CO2)的情况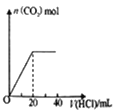
【答案】A
【解析】
A. 氯化铝和氢氧化钠反应生成氢氧化铝和氯化钠的反应,反应的化学方程式为:AlCl3+3NaOH=Al(OH)3↓+3NaCl;氢氧化铝沉淀溶解的过程,反应生成偏铝酸钠和水,反应的离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,前后NaOH的物质的量之比为3:1,符合此图,故A正确;
B. b点为硝酸钾在80℃时的饱和溶液,a点为不饱和溶液,可以通过升高温度蒸发掉部分溶剂,然后恢复到80℃可以变成饱和溶液,但是仅仅升高温度不行,故B错误;
C. 催化剂能改变活化能,但不能改变反应热,故C错误;
D. 向Na2CO3溶液中逐滴加入盐酸时,发生的反应依次为Na2CO3+HCl=NaCl+NaHCO3和NaHCO3+HCl=NaCl+CO2↑+H2O,不会立刻产生二氧化碳,故D错误;
正确答案是A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)氯酸钾熔化,粒子间克服了________的作用力;二氧化硅熔化,粒子间克服了________的作用力;碘的升华,粒子间克服了________的作用力。三种晶体的熔点由高到低的顺序是______(填化学式)。
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为________(填序号)。
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子是________,由非极性键形成的非极性分子是________,能形成分子晶体的物质是________,含有氢键的晶体的化学式是__________,属于离子晶体的是_________,属于原子晶体的是_______,五种物质的熔点由高到低的顺序是__________。
(4)A、B、C、D为四种晶体,性质如下:
A 固态时能导电,能溶于盐酸
B 能溶于CS2,不溶于水
C 固态时不导电,液态时能导电,可溶于水
D 固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:
A.______;B.______;C.________;D._____。
(5)相同压强下,部分元素氟化物的熔点见下表:
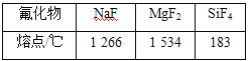
试解释上表中氟化物熔点差异的原因:__________
(6)镍粉在CO中低温加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。150 ℃时,Ni(CO)4分解为Ni和CO。Ni(CO)是________晶体,Ni(CO)4易溶于下列________(填序号)
a 水 b 四氯化碳 c 苯 d 硫酸镍溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 反应A(g)+3B(g)![]() 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率
分别如下,其中反应速率最大的是( )
A.v(C)=0.04 mol/(L·s)
B.v(B)=0.06 mol/(L·min)
C.v(A)=0.15 mol/(L·min)
D.v(D)=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 按要求写出下列反应的方程式。
①醋酸电离方程式:______________。
②一水合氨电离方程式:_______________________。
③碳酸氢钠与氢氧化钠反应离子方程式:___________。
(2) 在0.2 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如下图所示,回答下列问题:
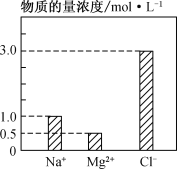
①该混合液中,NaCl的物质的量为________mol,含溶质MgCl2的质量为________g。
②该混合液中CaCl2的物质的量为________mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钾是一种无色晶体,易溶于水。实验室制备KI晶体的步骤如下:
Ⅰ.在如下图所示的三颈烧瓶中加入研细的I2和一定量的30%KOH溶液,搅拌(已知:I2与KOH反应产物之一是KIO3);
Ⅱ.碘完全反应后,打开分液漏斗中的活塞、弹簧夹1、2,向装置C中通入足量的H2S;
Ⅲ.反应结束后,向装置C中加入稀H2SO4酸化,水浴加热;
Ⅳ.冷却,过滤得KI粗溶液。
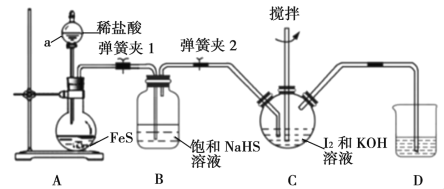
(1)仪器a的名称是__________,步骤Ⅰ中控制KOH溶液过量的目的是______________。
(2)装置B的作用是_____________,装置D中盛放的溶液是________________。
(3)装置C中H2S和KIO3反应的离子方程式为_______________________。
(4)步骤Ⅲ中水浴加热的目的是除去_________________________(填化学式)。
(5)由步骤Ⅳ所得的KI粗溶液中含有少量K2SO4,需进行提纯,提纯流程如下:
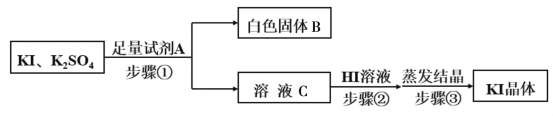
①已知白色固体B是混合物,试剂A为__________,为除去溶液C中的杂质,步骤②中调节溶液为弱酸性,则加入HI溶液后产生的现象是___________________。
②为测定最后所得KI晶体的纯度,取a g晶体配制100mL溶液,取出25mL溶液,滴入足量稀的酸性K2Cr2O7溶液,充分反应后,滴加几滴淀粉溶液为指示剂,用b mol·L-1的Na2S2O3溶液进行滴定,消耗Na2S2O3溶液VmL。
滴定过程中涉及的反应为:![]() ,
,![]() 则滴定终点时的现象为________________________,晶体的纯度为_______________________(列出计算式)。
则滴定终点时的现象为________________________,晶体的纯度为_______________________(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol甲醇分子中含有的共价键数为4NA
B.2.4 g镁在足量的氧气中燃烧,转移的电子数为0.1NA
C.标准状况下,5.6 L二氧化碳气体中含有的氧原子数为0.5NA
D.1 L 0.5 mol/L CH3COONa溶液中含有的CH3COO-数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是___,氧化产物是___(填写化学式)。
(2)根据上述反应,鉴别NaNO2、NaCl.可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有______(填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是______(填编号)。
A.NaClB.NH4ClC.HNO3D.浓H2SO4
(4)化学方程式:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.若反应过程中转移5mole-,则生成标准状况下N2的体积为______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】活性炭可处理大气污染物NO。为模拟该过程,T℃时,在3L密闭容器中加入NO和活性炭粉,反应体系中各物质的量变化如下表所示。下列说法正确的是
活性炭/mol | NO/mol | X/mol | Y/mol | |
起始时 | 2.030 | 0.100 | 0 | 0 |
10min达平衡 | 2.000 | 0.040 | 0.030 | 0.030 |
A. X一定是N2,Y一定是CO2
B. 10min后增大压强,NO的吸收率增大
C. 10min后加入活性炭,平衡向正反应方向移动
D. 0~10min的平均反应速率v(NO)=0.002 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. CS2为V形的极性分子,形成分子晶体
B. ClO3-的空间构型为平面三角形
C. 氯化硼BCl3的熔点为-107 ℃,氯化硼液态时能导电而固态时不导电
D. SiF4和SO32-的中心原子均为sp3杂化,SiF4分子呈空间正四面体,SO32-呈三角锥形
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com