
【题目】中科院科学家们研究开发了一种柔性手机电池,示意图如图所示[其中多硫化锂(Li2Sx)中x=2、4、6、8]。下列说法错误的是
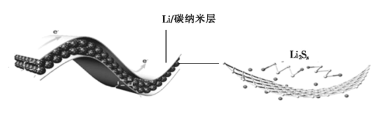
A.碳纳米层具有导电性,可用作电极材料
B.放电时,Li+移向Li2Sx膜
C.电池工作时,正极可能发生反应:2Li2S6+2Li++2e-=3Li2S4
D.电池充电时间越长,电池中Li2S2的量越多
科目:高中化学 来源: 题型:
【题目】元素周期表中ⅦA族元素的单质及其化合物的用途广泛。
23、三氟化溴(BrF3)常用于核燃料生产和后处理,遇水立即发生如下反应:3BrF3 +5H2O → HBrO3+ Br2+ 9HF+ O2 。该反应中氧化剂与还原剂的物质的量之比为________,每生成2.24 LO2(标准状况)转移电子数为__________。
24、在食盐中添加少量碘酸钾可预防缺碘。为了检验食盐中的碘酸钾,可加入醋酸和淀粉-碘化钾溶液。看到的现象是________________________,相应的离子方程式是_______________________。
氯常用作饮用水的杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)![]() Cl2(aq) ---------------①
Cl2(aq) ---------------①
Cl2(aq)+ H2O![]() HClO + H++Cl------②
HClO + H++Cl------②
HClO![]() H++ ClO----------------③
H++ ClO----------------③
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
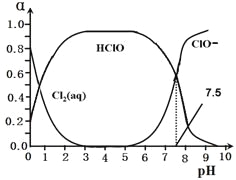
25、写出上述体系中属于电离平衡的平衡常数表达式:Ki =_______,由图可知该常数值为_________。
26、在该体系中c(HClO) + c(ClO-)_______c(H+)-c(OH-)(填“大于”“小于”或“等于”)。
27、用氯处理饮用水时,夏季的杀菌效果比冬季______(填“好”或“差”),请用勒夏特列原理解释________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种储能较大的新型可充电锌溴液流电池工作原理如图所示。下列说法不正确的是( )
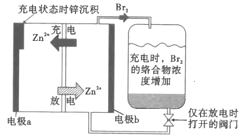
A.电极a在充电时连接电源的负极
B.放电时,电极b发生的反应是Zn2++2e-=Zn
C.放电时,电极b附近的Zn2+和Br-的浓度均增加
D.电池采用澳络合剂将溴单质络合,可以提高系统的安全性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烷烃C5H12有三种同分异构体,有关它们的结构和性质的说法不正确的是( )
A.三种同分异构体在常温常压下均为液体
B.其中一种同分异构体的碳原子间结构:具有空间正四面体对称结构
C.三种同分异构体具有相同的分子式.相对原子质量,化学性质相似
D.C5H11Cl共有8种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年纳雍县的财政收入25.4亿元,然而每年因钢铁腐蚀损失1500亿元,可见防止钢铁腐蚀具有重要意义,下列做法不能达到保护金属的是( )
A.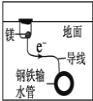 B.
B.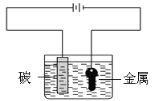
C.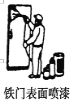 D.
D.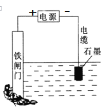
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基态原子由原子核和绕核运动的电子组成,下列有关核外电子说法正确的是
A.基态原子的核外电子填充的能层数与元素所在的周期数相等
B.基态原子的核外电子填充的轨道总数一定大于或等于![]() (m表示原子核外电子数)
(m表示原子核外电子数)
C.基态原子的核外电子填充的能级总数为![]() (n为原子的电子层数)
(n为原子的电子层数)
D.基态原子的核外电子运动都有顺时针和逆时针两种自旋状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的是

A.两种酸溶液的物质的量浓度一定相等B.稀释后A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸D.若1<a<4,则A、B都是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列物质的转化关系,回答问题:
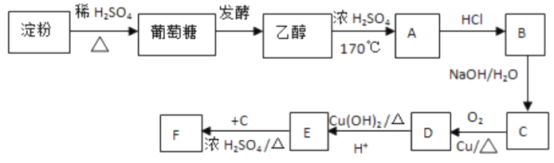
(I)淀粉属于___。
A.多糖 B.酯类 C.高分子化合物 D.单糖
(2)葡萄糖常用于水壶胆镀银,说明它有___(写出官能团名称);
(3)完成下列方程式:C6H12O6![]() 2C2H5OH+2___
2C2H5OH+2___
(4)写出B的结构简式:___;
(5)写出下列化学方程式:
①C→D:___;
②E+C→F:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体([CH3CH(OH)COO]2Fe·3H2O ,相对分子质量为288)易溶于水,是一种很好的补铁剂,可由乳酸[CH3CH(OH)COOH]与FeCO3反应制得。I.碳酸亚铁的制备(装置如图所示)
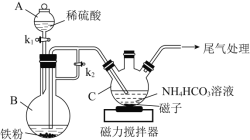
(1)仪器B的名称是______;实验操作如下:打开k1、k2,加入适量稀硫酸,关闭k1,使反应进行一段时间,其目的是______。
(2)接下来要使仪器C中的制备反应发生,需要进行的操作是______,其反应的离子方程式为______。
(3)仪器C中混合物经过滤、洗涤得到FeCO3沉淀,检验其是否洗净的方法是____。
Ⅱ乳酸亚铁的制备及铁元素含量测定
(4)向纯净FeCO3固体中加入足量乳酸溶液,在75℃下搅拌使之充分反应,经过滤,在______的条件下,经低温蒸发等操作后,获得乳酸亚铁晶体。
(5)两位同学分别用不同的方案进行铁元素含量测定:
①甲同学通过KMnO4滴定法测定样品中Fe2+的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于100%,其原因可能是______
②乙同学经查阅资料后改用碘量法测定铁元素的含量计算样品纯度。称取3.000g样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成100mL溶液。吸取 25.00mL该溶液加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.100 mol·L-1硫代硫酸钠溶液滴定(已知: I2+2S2O32-=S4O62-+2I-),当溶液______ ,即为滴定终点;平行滴定3次,硫代硫酸钠溶液的平均用量为24.80 mL,则样品纯度为______ %保留1位小数 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com