
【题目】元素周期表中ⅦA族元素的单质及其化合物的用途广泛。
23、三氟化溴(BrF3)常用于核燃料生产和后处理,遇水立即发生如下反应:3BrF3 +5H2O → HBrO3+ Br2+ 9HF+ O2 。该反应中氧化剂与还原剂的物质的量之比为________,每生成2.24 LO2(标准状况)转移电子数为__________。
24、在食盐中添加少量碘酸钾可预防缺碘。为了检验食盐中的碘酸钾,可加入醋酸和淀粉-碘化钾溶液。看到的现象是________________________,相应的离子方程式是_______________________。
氯常用作饮用水的杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)![]() Cl2(aq) ---------------①
Cl2(aq) ---------------①
Cl2(aq)+ H2O![]() HClO + H++Cl------②
HClO + H++Cl------②
HClO![]() H++ ClO----------------③
H++ ClO----------------③
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
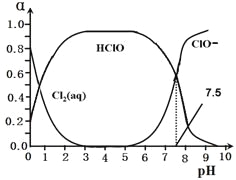
25、写出上述体系中属于电离平衡的平衡常数表达式:Ki =_______,由图可知该常数值为_________。
26、在该体系中c(HClO) + c(ClO-)_______c(H+)-c(OH-)(填“大于”“小于”或“等于”)。
27、用氯处理饮用水时,夏季的杀菌效果比冬季______(填“好”或“差”),请用勒夏特列原理解释________________________________________________________________。
【答案】2:3 0.6NA 溶液变蓝 5I-+ IO3-+6 CH3COOH →3I2+ 3H2O + 6CH3COO-  10-7.5或 3.16×10-8 小于 差 温度升高,(溶解)平衡①逆向移动,Cl2(aq)浓度减少,使得(化学平衡)②逆向移动,c(HClO)减少,杀菌效果变差
10-7.5或 3.16×10-8 小于 差 温度升高,(溶解)平衡①逆向移动,Cl2(aq)浓度减少,使得(化学平衡)②逆向移动,c(HClO)减少,杀菌效果变差
【解析】
23.在反应3BrF3 +5H2O =HBrO3+ Br2+ 9HF+ O2中,3个BrF3 分子中,1分子是还原剂,2分子是氧化剂,另外5个水分子中也有2分子是还原剂,故反应中氧化剂与还原剂的物质的量之比为2:3;每生成为0.1molO2时,有0.2mol BrF3被还原转移电子数为0.6NA。
24.检验食盐中的碘酸钾,可加入醋酸和淀粉-碘化钾溶液后可看到溶液变蓝,是由于酸性条件下碘酸根离子被还原,碘离子被氧化生成碘单质的缘故,发生反应的离子方程式为:5I-+ IO3-+6 CH3COOH =3I2+ 3H2O + 6CH3COO-要注意醋酸为弱酸不可拆分。
25.反应③为电离平衡,故电离平衡常数为:K= ;图中显示在pH=7.5时达到电离平衡,此时c(ClO-)=c(HClO),K=c(H+)=10-7.5;
;图中显示在pH=7.5时达到电离平衡,此时c(ClO-)=c(HClO),K=c(H+)=10-7.5;
26.在该体系中存在电荷守恒,即:c(OH-)+ c(ClO-) + c(Cl-)==c(H+),可得c(ClO-) + c(Cl-)==c(H+)-c(OH-),溶液中c(Cl-)大于c(HClO),故c(HClO) + c(ClO-)小于c(H+)-c(OH-);
27.用氯处理饮用水时,夏季的杀菌效果比冬季差,原因是依据勒夏特列原理,夏季温度高,溶解平衡逆向移动,Cl2(aq)浓度减少,使得反应②逆向移动,溶液中HClO的浓度减少,漂白效果降低。


科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)可用作火箭推进剂等。制备NH4ClO4的工艺流程如下:
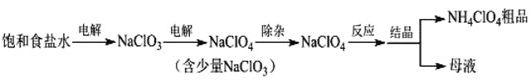
(1)电解NaClO3溶液时,ClO3-在____极发生反应,其电极反应式为____。
(2)“除杂”有两种方案。
①方案1:加入盐酸和H2O2溶液,NaClO3转化为ClO2,化学方程式为______。
方案2:加入氨水和FeCl24H2O,NaClO3转化为Cl-,离子方程式为____,如果FeCl24H2O过量会出现黑色磁性沉淀,该沉淀可能是______。(填化学式)
②比较氧化性:ClO3-_____ClO4-(填“>”或“<”)。
③两种方案相比,方案1的优点是____。(答一条即可)
(3)“反应”时用NaClO4和NH4Cl在90℃制备NH4ClO4。如果用浓盐酸和液氨代替NH4Cl,则无需加热,原因是____。
(4)该流程中可循环利用的物质是_________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理对于消除环境污染有重要意义。NO在空气中存在如下反应:2NO(g)+O2(g)![]() 2NO2(g) △H,上述反应分两步完成,其反应历程如图所示:
2NO2(g) △H,上述反应分两步完成,其反应历程如图所示:
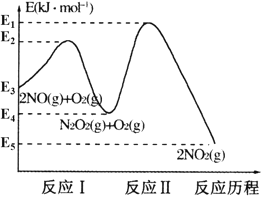
回答下列问题:
(1)写出反应I的热化学方程式___。
(2)反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)![]() 2NO2(g)反应速率的是___(填“反应I”或“反应Ⅱ”);对该反应体系升高温度,发现总反应速率反而变慢,其原因可能是___(反应未使用催化剂)。
2NO2(g)反应速率的是___(填“反应I”或“反应Ⅱ”);对该反应体系升高温度,发现总反应速率反而变慢,其原因可能是___(反应未使用催化剂)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚硝酰(NOC1,沸点为-5.5 °C )是有机合成中的重要试剂,为黄色气体,具有刺鼻恶臭味,遇水反应,有多种方法制备氯化亚硝酰。已知:HNO2既有氧化性又有还原性,AgNO2微溶于水,溶于硝酸:AgNO2 + HNO3 =AgNO3+ HNO2。
(1)将5g在300°C下干燥了3h并研细的KCl粉末装入50mL带有接头及抽真空用活塞的玻璃容器内。将容器尽量减压,在减压条件下通入0.002 mol NO2。反应12~36 min即可完成,红棕色的NO2消失,出现黄色的氯化亚硝酰,同时还得到一种盐,该盐的化学式为____________, 氯化钾需要“干燥”的原因是_____________。
(2)实验室可由氯气与一氧化氮在常温常压下合成氯化亚硝酰,装置如图所示。
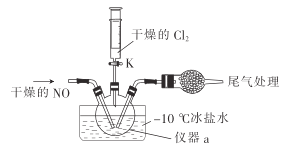
①仪器a的名称为__________。
②干燥管中盛放的试剂为____________。
③生成NOCl的化学方程式为________________。
(3)为验证NOCl与H2O反应后的溶液中存在Cl-和HNO2,设计如下实验步骤,完成下列表格。
步骤 | 实验现象或反应的化学方程式 |
①取5ml三颈烧瓶中产品,加入盛有水的烧杯中,充分反应 | NOCl与H2O发应的化学方程式_______ |
②向烧杯中滴加足量AgNO3溶液,有白色沉淀生成,再加入足量稀硝酸 | 加入稀硝酸后,实验现象为___________ |
③向步骤②烧杯中滴加酸性KMnO4溶液 | 实验现象为___________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用10 mol/L的浓盐酸配制250mL 1 mol/L的稀盐酸,并进行有关实验。请回答下列问题:
(1)需要量取浓盐酸_________mL。
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有_______、______等。
(3)取所配制的稀盐酸100mL,与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,则参加反应的锌的质量为______g ;设反应后溶液的体积仍为100 mL ,则反应后溶液中H+的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质。(反应过程中生成的水及其他产物已略去)
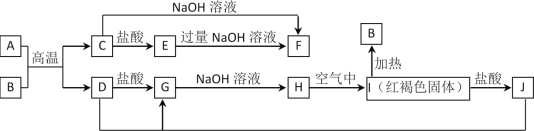
请回答以下问题:
(1)B是__________,H是_______________。(填化学式)
(2)写出J与D反应转化为G的离子方程式_________________________________。
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物心舒宁(又名冠心宁)是一种有机酸盐,用于治疗心脉瘀阻所致的冠心病、心绞痛等,可用以下路线合成。
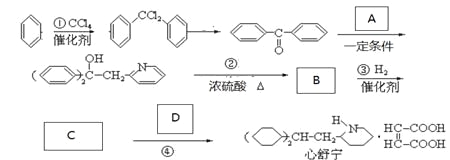
完成下列填空:
47、写出反应类型:反应①______________、反应②_______________。
48、写出结构简式:A__________________、C____________________。
49、由1mol B转化为C,消耗H2的物质的量为_______________。如果将③、④两步颠倒,则最后得到的是(写结构简式)__________________________。
50、D有同类别的同分异构体E,写出E与乙二醇发生缩聚反应所得产物的结构简式______________。
51、写出与A的属于芳香族化合物的同分异构体与盐酸反应的化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下,下列叙述不正确的是
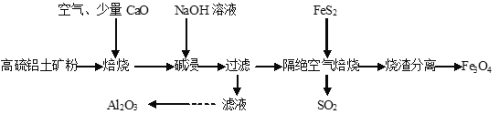
A.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
B.向滤液中通入过量HCl气体、过滤、洗涤、灼烧沉淀可制得Al2O3
C.隔绝空气焙烧时理论上反应消耗的n(FeS2):n(Fe2O3)=1:5
D.烧渣分离可用磁选法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院科学家们研究开发了一种柔性手机电池,示意图如图所示[其中多硫化锂(Li2Sx)中x=2、4、6、8]。下列说法错误的是
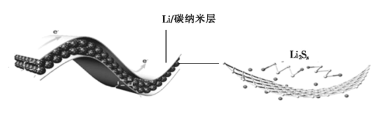
A.碳纳米层具有导电性,可用作电极材料
B.放电时,Li+移向Li2Sx膜
C.电池工作时,正极可能发生反应:2Li2S6+2Li++2e-=3Li2S4
D.电池充电时间越长,电池中Li2S2的量越多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com