
【题目】药物心舒宁(又名冠心宁)是一种有机酸盐,用于治疗心脉瘀阻所致的冠心病、心绞痛等,可用以下路线合成。
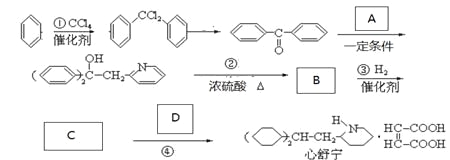
完成下列填空:
47、写出反应类型:反应①______________、反应②_______________。
48、写出结构简式:A__________________、C____________________。
49、由1mol B转化为C,消耗H2的物质的量为_______________。如果将③、④两步颠倒,则最后得到的是(写结构简式)__________________________。
50、D有同类别的同分异构体E,写出E与乙二醇发生缩聚反应所得产物的结构简式______________。
51、写出与A的属于芳香族化合物的同分异构体与盐酸反应的化学方程式______________。
【答案】取代反应 消去反应 ![]()
![]() 10mol
10mol 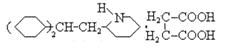
![]()
![]()
【解析】
根据流程图中苯转化为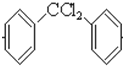 ,为四氯化碳中的两个氯原子被苯环上的碳取代,同一碳上的羟基不稳定,所以卤代烃水解消去得到酮
,为四氯化碳中的两个氯原子被苯环上的碳取代,同一碳上的羟基不稳定,所以卤代烃水解消去得到酮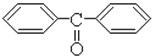 ,根据酮和A反应生成
,根据酮和A反应生成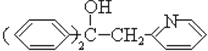 ,推之酮和A发生加成反应的产物,所以A为:
,推之酮和A发生加成反应的产物,所以A为: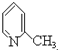 ,
,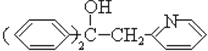 在浓硫酸的作用下发生醇羟基的消去反应生成B
在浓硫酸的作用下发生醇羟基的消去反应生成B![]() ,和氢气发生加成反应生成C
,和氢气发生加成反应生成C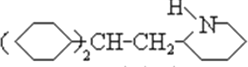 ,C与D反应生成心舒宁,所以D为:
,C与D反应生成心舒宁,所以D为:![]() ;据以上分析进行解答。
;据以上分析进行解答。
据流程图中苯转化为 ,为四氯化碳中的两个氯原子被苯环上的碳取代,CCl4+2
,为四氯化碳中的两个氯原子被苯环上的碳取代,CCl4+2![]() →
→ +2HCl,同一碳上的羟基不稳定,所以卤代烃水解消去得到酮
+2HCl,同一碳上的羟基不稳定,所以卤代烃水解消去得到酮 ,根据酮和A反应生成
,根据酮和A反应生成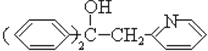 ,推之酮和A发生加成反应的产物,
,推之酮和A发生加成反应的产物, +
+ →
→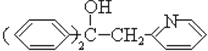 ,A为:
,A为: ,
,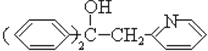 在浓硫酸的作用下发生醇羟基的消去反应
在浓硫酸的作用下发生醇羟基的消去反应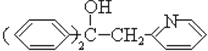 →
→![]() +H2O,生成B
+H2O,生成B![]() ,和氢气发生加成反应
,和氢气发生加成反应![]() +10H2→
+10H2→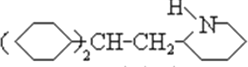 ,生成C
,生成C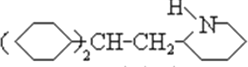 ,C与D反应生成心舒宁,所以D为:
,C与D反应生成心舒宁,所以D为:![]() ,反应为:
,反应为: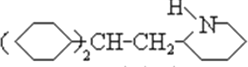 +
+![]() →
→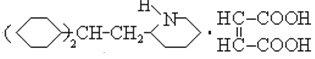 ,
,
47.结合以上分析可知,反应①取代反应、 反应②是醇的消去;
48.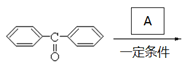 发生加成反应生成
发生加成反应生成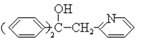 ,结合原子守恒和碳架结构可得出A的结构简式:
,结合原子守恒和碳架结构可得出A的结构简式:![]() ;C是由
;C是由![]() 经过醇的消去,再和氢气完全加成的产物,可C的结构简式为:
经过醇的消去,再和氢气完全加成的产物,可C的结构简式为:![]() ;
;
49.B与氢气加成时二个苯环和右侧六元环需要9个氢分子,另外还有一个碳碳双键,故由1mol B转化为C,完全加成消耗H2的物质的量为10mol;如果将③、④两步颠倒,则发生反应为中间体B先与
![]() 生成盐,后再与H2加成,故最后得到的产物的结构简式中应不含不饱和的双键.即为
生成盐,后再与H2加成,故最后得到的产物的结构简式中应不含不饱和的双键.即为![]() ;
;
50.D为![]() 与之同类别的同分异构体E为
与之同类别的同分异构体E为![]() ,E与乙二醇发生缩聚反应所得产物的结构简式
,E与乙二醇发生缩聚反应所得产物的结构简式![]() ;
;
51.A的属于芳香族化合物的同分异构体为![]() 与盐酸反应的化学方程式
与盐酸反应的化学方程式
![]() 。
。


科目:高中化学 来源: 题型:
【题目】I.某化工厂以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分Na2Cr2O7.2H2O),其主要工艺流程如下图:
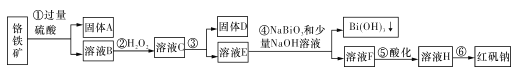
查阅资料得知:
i.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-。
ii.
金属离子 | Fe3+ | Al3+ | Cr3+ | Fe2+ | Bi3+ |
开始沉淀的 pH | 2.7 | 3.4 | 5.0 | 7.5 | 0.7 |
沉淀完全的pH | 3.7 | 4.9 | 5.9 | 9.7 | 4.5 |
回答下列问题:
(1)固体A的主要成分为____(填化学式)。
(2)步骤③加的试剂为氢氧化钠溶液,此时溶液pH要调到5.0的目的是____。
(3)写出④反应的离子反应方程式:____。
(4)取一定质量的固体D溶解于200 mL的硫酸中,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V关系如图所示,则加入NaOH溶液体积为200~240 mL时发生反应的化学方程式为____,固体D中含铁化合物的物质的量为____

Ⅱ.经检测该化工厂的工业废水中含5.00×10-3mol/L的Cr2O72-,其毒性较大。该化工厂的科研人员为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Fe的化合价依次为+3、+2),又设计了如下工艺流程:
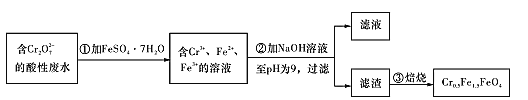
(5)第①步反应的离子方程式为____。
(6)欲使1 L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4。理论上需要加FeSO4.7H2O的质量为 ___g(已知FeSO4.7H2O的摩尔质量为278 g/mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,用0.1000 mol· L -1的NaOH溶液滴定0. 1000 mol· L -1的顺丁烯二酸H2A的滴定曲线如下图所示(pKa= lgKa),下列说法错误的是
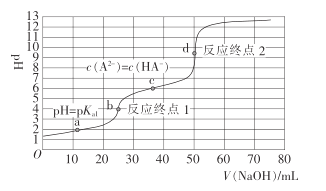
A.用NaOH溶液滴定NaHA溶液可用酚酞作指示剂
B.a点:c(HA-)=c(H2A)
C.H2A的Ka2=10-6
D.d点:c(Na+)<c(HA-)+2c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中ⅦA族元素的单质及其化合物的用途广泛。
23、三氟化溴(BrF3)常用于核燃料生产和后处理,遇水立即发生如下反应:3BrF3 +5H2O → HBrO3+ Br2+ 9HF+ O2 。该反应中氧化剂与还原剂的物质的量之比为________,每生成2.24 LO2(标准状况)转移电子数为__________。
24、在食盐中添加少量碘酸钾可预防缺碘。为了检验食盐中的碘酸钾,可加入醋酸和淀粉-碘化钾溶液。看到的现象是________________________,相应的离子方程式是_______________________。
氯常用作饮用水的杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)![]() Cl2(aq) ---------------①
Cl2(aq) ---------------①
Cl2(aq)+ H2O![]() HClO + H++Cl------②
HClO + H++Cl------②
HClO![]() H++ ClO----------------③
H++ ClO----------------③
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
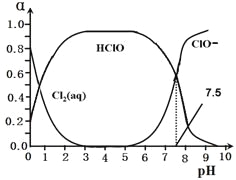
25、写出上述体系中属于电离平衡的平衡常数表达式:Ki =_______,由图可知该常数值为_________。
26、在该体系中c(HClO) + c(ClO-)_______c(H+)-c(OH-)(填“大于”“小于”或“等于”)。
27、用氯处理饮用水时,夏季的杀菌效果比冬季______(填“好”或“差”),请用勒夏特列原理解释________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为常见的有机物,在一定条件下,它们有如图所示的转化关系:

其中M(C)> M(B)> M(A)(M表示摩尔质量)。请根据图回答:
(1)不溶于水的物质是(填字母)_______________。
(2)能使紫色石蕊试液变红的物质是(填名称)_________。
(3)属于还原反应的是(填序号)___________________。
(4)写出D与水反应生成B和C的化学方程式(有机物用结构简式表示)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验制备Ca(NO2)2,实验装置如图所示(夹持装置已略去)。已知:2NO+CaO2==Ca(NO2)2;2NO2+CaO2==Ca(NO3)2。下列说法不正确的是
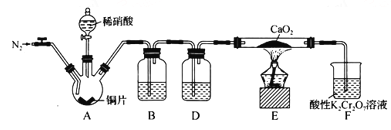
A. 通入N2是为了排尽装置中的空气
B. 装置B、D中的试剂可分别为水和浓硫酸
C. 将铜片换成木炭也可以制备纯净的亚硝酸钙
D. 借助装置A及氢氧化钠溶液和稀硫酸可以分离CO2和CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的装置中,通电5min后,铜电极的质量增加2.16g。试回答下列问题:
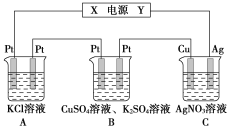
(1)电源中X极为直流电源的__极。
(2)溶液pH的变化情况:A__,B__,C__(填“增大”“减小”或“不变”)。
(3)通电5min后,B装置中共收集224mL(标准状况下)气体,溶液体积为200mL,则通电前该装置溶液中CuSO4的物质的量浓度为__(设电解前后溶液体积无变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种储能较大的新型可充电锌溴液流电池工作原理如图所示。下列说法不正确的是( )
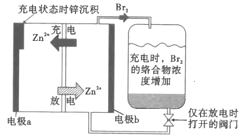
A.电极a在充电时连接电源的负极
B.放电时,电极b发生的反应是Zn2++2e-=Zn
C.放电时,电极b附近的Zn2+和Br-的浓度均增加
D.电池采用澳络合剂将溴单质络合,可以提高系统的安全性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的是

A.两种酸溶液的物质的量浓度一定相等B.稀释后A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸D.若1<a<4,则A、B都是弱酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com