
【题目】A~H为中学化学中常见的物质,转化关系如下所示,其中“O”代表化合物,“□”代表单质,A为医疗上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体.
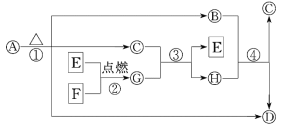
请回答下列问题:
(1)G的化学式为________,每生成1 mol G转移电子________mol.
(2)反应①②③④中________(填序号)属于氧化还原反应.
(3)写出下列反应的化学方程式:A→B+C+D:_______________________________,F+C:________________________________.
【答案】Na2O2 2 ②③ 2NaHCO3![]() Na2CO3+H2O+CO2↑ 2Na+2H2O===2NaOH+H2↑
Na2CO3+H2O+CO2↑ 2Na+2H2O===2NaOH+H2↑
【解析】
化合物G为淡黄色固体,化合物C在通常状况下为无色液体,二者反应生成气体单质E与化合物H,则G是Na2O2,C是H2O,H为NaOH,E是O2,由反应②可知单质F为Na.根据反应④可知D中含有Na元素,A是医疗上治疗胃酸过多的一种药剂,加热分解生成水、B及含Na元素化合物D,可推知A是NaHCO3、B为CO2、D为Na2CO3,二氧化碳与氢氧化钠反应生成碳酸钠与水,符合转化关系,据此解答。
(1)由上述分析可知,G为Na2O2,反应②中每生成1molNa2O2需要2molNa,Na元素化合价由0价升高为+1,故转移电子为2mol×1=2mol,
故答案为:Na2O2;2。
(2)再反应①②③④中,Na与氧气反应生成过氧化钠、过氧化钠与水反应生成氢氧化钠与氧气,二者都属于氧化还原反应,
故答案为:②③。
(3)A→B+C+D的化学方程式为:2NaHCO3![]() Na2CO3+H2O+CO2↑,F+C反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,
Na2CO3+H2O+CO2↑,F+C反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:2NaHCO3![]() Na2CO3+H2O+CO2↑,2Na+2H2O=2NaOH+H2↑。
Na2CO3+H2O+CO2↑,2Na+2H2O=2NaOH+H2↑。


科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式正确的是( )
A. 氯化铝溶液与过量的氨水反应:Al3++4NH3·H2O===AlO![]() +4NH
+4NH![]() +2H2O
+2H2O
B. 小苏打溶液中加入过量的澄清石灰水:Ca2++2OH-+2HCO![]() ===CaCO3↓+ CO
===CaCO3↓+ CO![]() +2H2O
+2H2O
C. 纯碱溶液中滴加少量盐酸:CO32-+H+===HCO![]()
D. 用FeCl3溶液腐蚀铜电路板:Fe3++ Cu === Fe2++ Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用海水可以提取溴和镁,提取过程如下:

(1)提取溴的过程中,经过2次Br-→Br2转化的目的是_______,吸收塔中发生反应的离子方程式是SO2+Br2+2H2O=4H++2Br-+SO42-,蒸馏塔中发生反应的离子方程式是_____。
(2)从MgCl2溶液中得到MgCl26H2O晶体的主要操作是_________、冷却结晶、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是___。
(3)海水提取镁要用到海滩上的贝壳,贝壳的作用是:_______,贝壳经历变化的化学方程式为:____,CaO+H2O = Ca(OH)2
(4)六水合氯化镁脱水变成无水氯化镁的工艺条件是:____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种离子。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中不正确的是( )
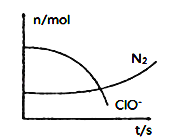
A.标准状况下若生成2.24LN2,则转移电子1mol
B.还原性:Cl-<CN-
C.参与反应的氧化剂与还原剂的物质的量之比为5:2
D.氧化剂是含ClO-的物质,氧化产物只有N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3.06 g铝和镁的混合物粉末放入100 mL盐酸中,恰好完全反应,并得到标准状况下3.36 LH2 计算:(要有过程)
(1)该合金中铝的物质的量_____。
(2)反应后溶液中Cl﹣的物质的量浓度(假定反应体积仍为100 mL)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.1 molNa在空气中完全燃烧,转移的电子数为2NA
B.常温下,2.7g铝与足量NaOH溶液反应,消耗0.1NA个水分子
C.0.1molFe与足量水蒸气反应生成H2的分子数为0.1NA
D.11.2LCl2含有的原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学向两个容积相同的烧瓶内分别充入一定量的HCl与NH3(假设烧瓶内其它气体难溶于水)。利用如图所示的装置进行实验,实验开始前各活塞均关闭。
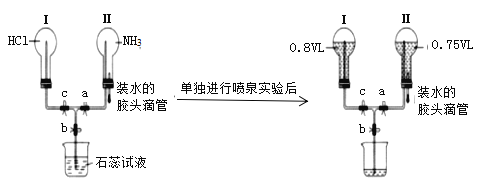
(1)同温同压下,两个烧瓶内充入的HCl与NH3分子数目之比为___,烧瓶Ⅱ中喷泉的颜色是___。
(2)单独进行喷泉实验后,烧瓶I中c(Cl-)=___molL-1(实验条件下气体摩尔体积为Vm)
(3)实验表明,若只是关闭b、打开a、c,则易在烧瓶I中观察到白烟,这表明气体分子扩散速率随着气体相对分子质量的增大而____(填“增大”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用铁的氧化物在高温条件下循环裂解水制氢气的流程如下图所示。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________。
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________。
(2)反应III为:CO2(g)+C(s)![]() 2CO(g)
2CO(g) ![]() H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________(任写一条措施)。
H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________(任写一条措施)。
(3)上述流程中铁的氧化物可用来制备含有Fe3+的刻蚀液,用刻蚀液刻蚀铜板时,可观察到溶液颜色逐渐变蓝,该反应的离子方程式为_________。刻蚀液使用一段时间后会失效,先加酸,再加入过氧化氢溶液,可实现刻蚀液中Fe3+的再生,该反应的离子方程式为_________。
(4)上述流程中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是()
A.2g氢气中的原子数为NA
B.1mol/LCaCl2溶液中Cl- 数为2NA
C.标准状况下22.4LCO2中原子数为3NA
D.2L2mol/LC2H5OH溶液中分子数为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com