
【题目】(1)在25 ℃、101 kPa的条件下,请回答下列有关问题:
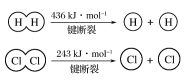
①由H+H→H2,当形成1 mol H—H键时,要________(填“吸收”或“放出”,下同)436 kJ的能量;由Cl2→Cl+Cl,当断裂1 mol Cl—Cl键时,要________243 kJ的能量。
②对于反应H2(g)+Cl2(g)=2HCl(g),测得生成2 molHCl(g)时,反应过程中放出183 kJ的热量,则断开 1 mol H—Cl 键所需的能量是________kJ。
③有两个反应:a.H2(g)+Cl2(g)![]() 2HCl(g),b.H2(g)+Cl2(g)
2HCl(g),b.H2(g)+Cl2(g)![]() 2HCl(g)。这两个反应中,相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量________(填“相等”或“不相等”)。
2HCl(g)。这两个反应中,相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量________(填“相等”或“不相等”)。
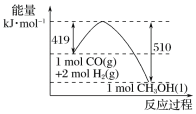
(2)①根据图示的能量转化关系判断,生成16 g CH3OH(l)________(填“吸收”或“放出”) ________kJ能量。
②1mol CO(g)的总键能_______(填“>”、“=”或“<”)1mol CH3OH(l)的总键能
【答案】放出 吸收 431 相等 放出 45.5 <
【解析】
断裂共价键时需要吸收热量,形成共价键时能够放出热量,化学反应的热效应等于反应物的总键能减去生成物的总键能,也等于生成物的总能量减去反应物的总能量,由此关系,也可求出反应物或生成物中某物质的能量或键能;对于一个化学反应,当反应物和生成物确定,化学反应的热效应也就确定,但与反应的条件无关。
(1)①形成共价键时,会放出热量,断裂共价键时,需吸收热量。从图中可以看出,当形成1 mol H-H键时,要放出436 kJ的能量;当断裂1 mol Cl-Cl键时,要吸收243 kJ的能量。
②设H-Cl 键能为x,则436kJ+243kJ-2x= -183kJ,x=431kJ,则断开 1 mol H-Cl 键所需的能量是431kJ。
③对于同一反应,当反应物的用量相同时,条件不影响反应的热效应,则两个反应:a.H2(g)+Cl2(g)![]() 2HCl(g),b.H2(g)+Cl2(g)
2HCl(g),b.H2(g)+Cl2(g)![]() 2HCl(g),相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量相等。答案为:放出;吸收;431;相等;
2HCl(g),相同物质的量的H2(g)、Cl2(g)反应生成相同质量的HCl(g)时,放出的能量相等。答案为:放出;吸收;431;相等;
(2)①由图中可知,1molCO(g)与2molH2(g)完全反应生成1molCH3OH(l),放热91kJ,则生成16 g CH3OH(l)(物质的量为0.5mol),放出91kJ/mol×0.5mol=45.5kJ能量。
②由图可知,反应物的总键能-生成物的总键能= -91kJ,即1mol CO(g)的总键能+2×436kJ-1mol CH3OH(l)的总键能= -91kJ,则1mol CO(g)的总键能-1mol CH3OH(l)的总键能= -91kJ-2×436kJ<0,所以1mol CO(g)的总键能<1mol CH3OH(l)的总键能。答案为:放出;45.5;<。


科目:高中化学 来源: 题型:
【题目】三草酸合铁酸钾K3[Fe(C2O4)3]·3H2O是一种绿色晶体,易溶于水,难溶于乙醇等有机溶剂,光照或受热易分解。实验室要制备K3[Fe(C2O4)3]·3H2O并测定![]() 的含量。请回答下列相关问题。
的含量。请回答下列相关问题。
I.FeC2O4·2H2O的制备
向烧杯中加入5.0g(NH4)2Fe(SO4)2·6H2O、15mL蒸馏水、1mL3moL/L的硫酸,加热溶解后加入25mL饱和H2C2O4溶液,继续加热并搅拌一段时间后冷却,将所得FeC2O4·2H2O晶体过滤、洗涤。
(1)制备FeC2O4·2H2O时,加入3mol/L硫酸的作用是________________________。
II.K3[Fe(C2O4)3]·3H2O的制备
向I中制得的FeC2O4·2H2O晶体中加入10mL饱和K2C2O4溶液,水浴加热至40℃,缓慢加入过量3%的H2O2溶液并不断搅拌,溶液中产生红褐色沉淀,H2O2溶液完全加入后将混合物加热煮沸一段时间,然后滴加饱和H2C2O4溶液使红褐色沉淀溶解。向溶液中再加入10mL无水乙醇,过滤、洗涤、干燥。
(2)制备过程中有两个反应会生成K3[Fe(C2O4)3],两个化学方程式依次是:______________________、2Fe(OH)3+3K2C2O4+3H2C2O4=2K3[Fe(C2O4)3]+6H2O。
(3)H2O2溶液完全加入后将混合物加热煮沸一段时间的目的是______________________。
III.![]() 含量的测定
含量的测定
称取0.22gⅡ中制得的K3[Fe(C2O4)3]·3H2O晶体于锥形瓶中,加入50mL蒸馏水和15mL3mol/L的硫酸,用0.02000mol/L的标准KMnO4溶液滴定,重复3次实验平均消耗的KMnO4溶液体积为25.00mL。
(4)滴定时KMnO4溶液应盛放在_____________(填仪器名称)中,判断滴定终点的依据是_________________。
(5)滴定终点时,所得溶液中的溶质除硫酸外,还有__________________________(写化学式),K3[Fe(C2O4)3]·3H2O样品中![]() 的质量分数是____________________。
的质量分数是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知亚硫酸钠在空气中能被氧气氧化生成硫酸钠。
I. 甲同学设计两种方案来检验![]() 是否发生变质。
是否发生变质。
方案一:取样,加入稀盐酸有气泡生成,认为亚硫酸钠没有变质。
方案二:取样,加入氯化钡溶液有白色沉淀生成,认为亚硫酸钠完全变质。
请你对两方案做出评价:
方案一:_________(填“合理”或“不合理”),理由是_____________________。
方案二:_________(填“合理”或“不合理”),理由是____________________。
Ⅱ. 乙同学为了探究![]() 是否发生变质,设计如下实验测定
是否发生变质,设计如下实验测定![]() 溶液的实际浓度。
溶液的实际浓度。

(1)①分液漏斗中应加入足量的________(填字母)。
a.浓硝酸 b.65%硫酸 c.浓盐酸
②装置B中盛装的试剂为_____________。
(2)实验前后测得装置C增重3.2g,则![]() 溶液实际的物质的量浓度为___________________(保留2位有效数字)。
溶液实际的物质的量浓度为___________________(保留2位有效数字)。
(3)该实验装置还存在一个明显的缺陷是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2的制取及其在污水处理方面的应用是当前科学研究的热点。
(1)“氧阴极还原法”制取H2O2的原理如题图所示:
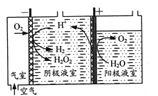
阴极表面发生的电极反应有:
Ⅰ.2H++O2+2e-=H2O2
Ⅱ. H2O2+2H++ 2e-=2H2O
Ⅲ. 2H+ +2e-=H2↑
①写出阳极表面的电极反应式:___。
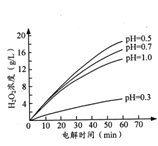
②其他条件相同时,不同初始pH(均小于2)条件下,H2O2浓度随电解时间的变化如图所示,c(H+)过大或过小均不利于H2O2制取,原因是_______。
(2)存碱性条件下,H2O2的一种催化分解机理如下:
H2O2(aq)+Mn2+(aq)=·OH(aq)+Mn3+(aq)+OH-(aq) H=akJ/mol
H2O2(aq)+ Mn3+(aq) +2OH-(aq)= Mn2+(aq) +·O2-(aq) +2H2O(l) H=bkJ/mol
·OH(aq) +·O2-(aq)=O2(g) +OH-(aq) H=ckJ/mol
2H2O2(aq)= 2H2O(l)+O2(g) △H=_______ 。该反应的催化剂为 ____。
(3)H2O2、O3在水中可形成具有超强氧化能力的羟基自由基(·OH),可有效去除废水中的次磷酸根离子(H2PO2-)。
①弱碱性条件下·OH将H2PO2-氧化成PO43-,理论上l.7g·OH可处理含0.001mol/L H2PO2-的模拟废水的体积为______。
②为比较不同投料方式下含H2PO2-模拟废水的处理效果,向两份等体积废水样品中加入等量H2O2和O3,其中一份再加入FeSO4。反应相同时间,实验结果如图所示:
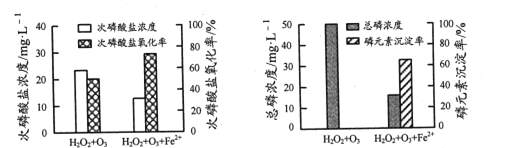
添加FeSO4后,次磷酸盐氧化率、磷元素沉淀率均显著提高,原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是( )
A. 正极的电极反应式为Ag2O+2e-+H2O=2Ag+2OH-
正极的电极反应式为Ag2O+2e-+H2O=2Ag+2OH-
B. 锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
C. Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
D. 使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相对分子质量为70的烯烃的分子式为________;若该烯烃与足量的H2加成后能生成含3个甲基的烷烃,则该烯烃的可能的结构简式为_______、_________、_________。
(2)有机物A的结构简式为
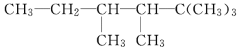
①用系统命名法命名A:___________________________
②若A的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个非常对称的分子构型,有顺、反两种结构。写出A的该种同分异构体的结构简式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 同等质量的氧气和臭氧中,电子数相同
C. 1 mol重水与1 mol水中,中子数比为2∶1
D. 1 mol乙烷和1 mol乙烯中,化学键数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置符合实验目的是( )
目的 | 粗铜的精炼 | 验证NaCl溶液(含酚酞)的产物 | 在铁制品上镀铜 | 构成原电池 |
装置 |
|
|
|
|
选项 | A | B | C | D |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种新型高分子材料的结构简式如图,对此高聚物叙述正确的是( )
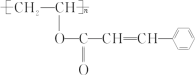
A.化学式为(C11H11O2)n
B.可以发生水解反应、氧化反应,不能发生取代反应
C.1mol该有机物分子最多能和4molH2发生加成反应
D.该高分子材料是由两种单体经酯化后加聚而成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com