
【题目】香豆素是广泛存在于植物中的一类芳香化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2,该芳香内酯A经下列步骤转变为水杨酸和和化合物E。
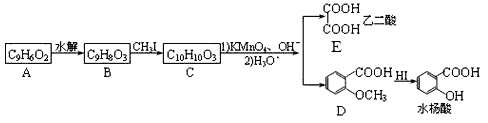
已知:CH3CH = CHCH2CH3![]() CH3COOH + CH3CH2COOH
CH3COOH + CH3CH2COOH
请回答下列问题:
(1)C中官能团的名称为________;化合物A的结构简式为________。
(2)C生成D和E的反应类型为________,化合物E的化学名称是________。
(3)写出B→C的化学反应方程式_________ 。
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的二元取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体共有________种;写出其中核磁共振氢谱有4种峰,且其信号强度之比为1:2:2:3的一种同分异构体的结构简式________ 。
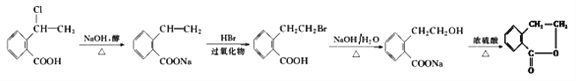
(5)已知: R- CH=CH2![]() R-CH2CH2Br,请设计合理方案由
R-CH2CH2Br,请设计合理方案由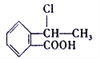 合成
合成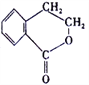 (其他无机原料自选,用反应流程图表示,并注明反应条件)。_______。示例:原料
(其他无机原料自选,用反应流程图表示,并注明反应条件)。_______。示例:原料![]() ……产物
……产物
【答案】 碳碳双键、羧基、醚键 ![]() 氧化反应 乙二酸或草酸
氧化反应 乙二酸或草酸 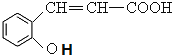 +CH3I—→
+CH3I—→ 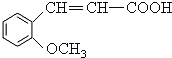 +HI 9
+HI 9 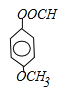
【解析】C被高锰酸钾氧化生成乙二酸和D,结合题给信息及C的分子式知,C的结构简式为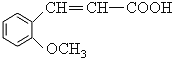 ,B和CH3I发生取代反应生成C,则B的结构简式为:
,B和CH3I发生取代反应生成C,则B的结构简式为: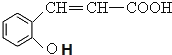 ,A水解生成B,且A的分子式为C9H6O2,所以A的结构简式为:
,A水解生成B,且A的分子式为C9H6O2,所以A的结构简式为:![]() ,D和IH发生取代反应生成水杨酸.
,D和IH发生取代反应生成水杨酸.
(5)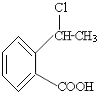 和氢氧化钠的醇溶液发生消去反应生成
和氢氧化钠的醇溶液发生消去反应生成 ,再与氢溴酸发生加成反应生成
,再与氢溴酸发生加成反应生成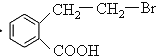 ,
,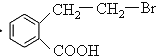 和氢氧化钠的水溶液发生取代反应生成为
和氢氧化钠的水溶液发生取代反应生成为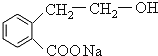 ,最后在浓硫酸加热条件下发生酯化反应生成
,最后在浓硫酸加热条件下发生酯化反应生成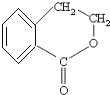 。
。
解析:
(1)C中官能团的名称为:碳碳双键、羧基、醚键;化合物A的结构简式为:![]() 。
。
(2)C生成D和E的反应类型为:氧化反应,化合物E的化学名称是:乙二酸或草酸。
(3)B和CH3I发生取代反应生成C,反应方程式为: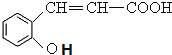 +CH3I—→
+CH3I—→ 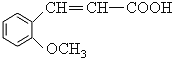 +HI。
+HI。
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的二取代物,说明含有两个取代基,能水解说明含有酯基,且水解后生成的产物之一能发生银镜反应,说明含有醛基,则其同分异构体为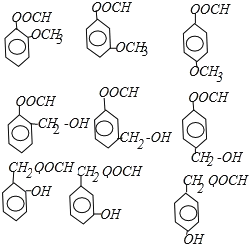 ,其中核磁共振氢谱有4种峰,且其信号强度之比为1:1:2:3的同分异构体的结构简式为:
,其中核磁共振氢谱有4种峰,且其信号强度之比为1:1:2:3的同分异构体的结构简式为: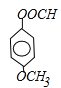 故答案为:9种;
故答案为:9种; 。
。
(5) 和氢氧化钠的醇溶液发生消去反应生成
和氢氧化钠的醇溶液发生消去反应生成 ,再与氢溴酸发生加成反应生成
,再与氢溴酸发生加成反应生成 ,
,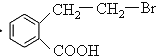 和氢氧化钠的水溶液发生取代反应生成为
和氢氧化钠的水溶液发生取代反应生成为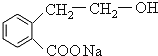 ,最后在浓硫酸加热条件下发生酯化反应生成
,最后在浓硫酸加热条件下发生酯化反应生成 ,合成路线流程图为:
,合成路线流程图为: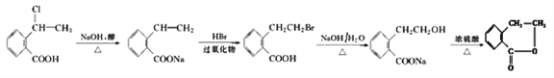


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | -33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)戊装置中冷凝管的进水口为___________(填“a”或“b”)。
(2)用甲装置制氯气,MnO4-被还原为Mn2+,该反应的离子方程式为________________________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到___________(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:①促进氯气与锡反应;②_______________________________。
(4)如果缺少乙装置,可能产生的后果是___________________;己装置的作用是__________________。
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2 的有_______________(填标号)。
a.FeCl3溶液(滴有KSCN) b.H2O2溶液 C.溴水 d.AgNO3溶液
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38 gSnCl4,则SnCl4的产率为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用 元素符号或化学式 填空回答以下问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在③~⑦元素中,原子半径最大的是_________,其离子的原子结构示意图为_____________
(2)①~⑩元素中,最不活泼的元素是____________,元素的最高价氧化物对应的水化物中酸性最强的酸是___________, 碱性最强的碱是_____________,呈两性的氢氧化物是
(3)按要求填写: ①的氢化物的电子式__________________;用电子式表示 ③和⑦形成化合物的形成过程__________________________________________;
(4)② ⑦和⑩的单质的氧化性由强到弱顺序是_________________________________,可用说明⑦和⑩的单质氧化性强弱的反应事实是(用化学反应方程式表示):__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】达康书记指出垃圾就是放错地方的财富。干电池中有氯化铵,手机电池中有钴酸锂(LiCoO2),铅蓄电池中有硫酸。那么请问局长:废旧电池属于那一类垃级?上面所说的三种物质中有几种是离子化合物?
A. 可回收垃圾,三种 B. 有害垃圾,两种。
C. 有害垃圾,三种 D. 其它垃圾,两种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道,“性最烈。能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指()
A. 氨水 B. 醋 C. 硝酸 D. 卤水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10 m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
-2 | -3 | -1 | -3 |
(1)元素①在周期表中的位置为_____。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为____(填化学式)。
(3)元素①、③形成的18电子化合物的电子式为____,元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是______(填化学式)。
(4)元素②、⑤形成化合物的电子式为_____。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4===2PbSO4+2H2O。铅蓄电池放电时正极是______(填物质化学式)。若电解液体积为2L(反应过程溶液体积变化忽略不计),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol/L下降到________mol/L。
(2)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式为:Zn+2OH--2e-=ZnO+H2O、Ag2O+H2O+2e-=2Ag+2OH-,电池的正极是____________,负极发生的是____________反应(填“氧化”或“还原”)。
(3)中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇(CH3OH)燃料电池的工作原理如图所示。

①该电池工作时,b口通入的物质为________
②该电池工作时,电子的流向为___________(填“从左到右”或“从右到左”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com