
【题目】实验室欲从含MgBr2的水中提取Br2,下列操作未涉及的是
A. 氧化 B. 过滤
B. 过滤 C. 分液
C. 分液 D. 蒸馏
D. 蒸馏
【答案】B
【解析】
欲从含MgBr2的水中提取Br2,首先氯气与溴化镁溶液反应生成氯化镁和溴单质;即发生反应:Cl2+MgBr2=MgCl2+Br2;因为溴溶于水,更易溶于有机溶剂,所以再加入苯或四氯化碳进行萃取,静置溶液分层,然后进行分液;又因为溴与有机物的沸点不同,可再进行蒸馏操作,可得到溴单质。
欲从含MgBr2的水中提取Br2,首先氯气与溴化镁溶液反应生成氯化镁和溴;即发生反应:Cl2+MgBr2=MgCl2+Br2,通过A装置完成;因为溴溶于水,更易溶于有机溶剂,所以再加入苯或四氯化碳进行萃取,使溶液分层,然后进行分液,通过C装置完成;又因为溴与有机物的沸点不同,可再进行蒸馏操作,可得到溴单质,通过D装置完成。根据以上分析没有用到过滤操作,所以答案为B。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】香豆素是广泛存在于植物中的一类芳香化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2,该芳香内酯A经下列步骤转变为水杨酸和和化合物E。
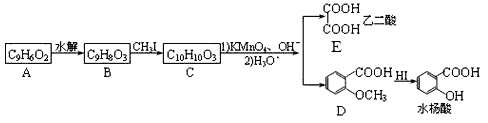
已知:CH3CH = CHCH2CH3![]() CH3COOH + CH3CH2COOH
CH3COOH + CH3CH2COOH
请回答下列问题:
(1)C中官能团的名称为________;化合物A的结构简式为________。
(2)C生成D和E的反应类型为________,化合物E的化学名称是________。
(3)写出B→C的化学反应方程式_________ 。
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的二元取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体共有________种;写出其中核磁共振氢谱有4种峰,且其信号强度之比为1:2:2:3的一种同分异构体的结构简式________ 。
(5)已知: R- CH=CH2![]() R-CH2CH2Br,请设计合理方案由
R-CH2CH2Br,请设计合理方案由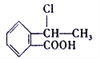 合成
合成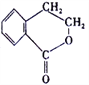 (其他无机原料自选,用反应流程图表示,并注明反应条件)。_______。示例:原料
(其他无机原料自选,用反应流程图表示,并注明反应条件)。_______。示例:原料![]() ……产物
……产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把铁片放入盛有过量稀硫酸的试管中,不影响氢气产生速率的因素是( )
A. 硫酸的浓度B. 铁片的表面积
C. 溶液的温度D. 加少量Na2SO4固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关加热操作正确的是( )
A.将烧杯放置在铁架台的铁圈上,直接用酒精灯火焰加热
B.将试管直接用酒精灯火焰加热
C.将蒸发皿放置在铁架台的铁圈上,并垫石棉网加热
D.将烧瓶放置在铁架台的铁圈上,直接用酒精灯火焰加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C在周期表中的位置如下图所示,其中B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C是
A | ||
B | C |
A. B、Mg、Si B. Be、Na、Al C. O、P、Cl D. C、Al、P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
A | 有三个电子层,K、M层电子数之和等于L层电子数 |
B | 短周期中金属性最强 |
C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
D | 元素最高正价是+7价 |
回答下列问题:
(1)A元素在周期表中的位置_______________;
(2)B元素原子结构示意图_______________;
(3)A、B、D按原子半径从大到小排序依次为_______________(用元素符号表示);
(4)元素D与元素A相比,非金属性较强的是_______________(用元素符号表示),下列表述中不能证明这一事实的是_______________(填选项序号)。
a 一定条件下D和A的单质都能与钠反应
b D的氢化物比A的氢化物稳定
c D单质能与A的氢化物反应生成A单质
d A的最高价含氧酸酸性弱于D的最高价含氧酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别向10 mL 0.1 molL1的NaOH 溶液中逐滴加入0.1 molL1的一元酸HA和HB溶液,用pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是
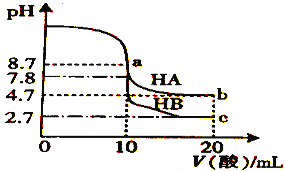
A. HA的酸性强于HB的酸性
B. V(酸)=10mL时,两份溶液中c(B)=c(A)
C. a 点时,c(A)>c(Na+)>c(OH)>c(H+)
D. b、c点时,c(A)+c(HA)=2c(Na+)=c(HB)+c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的化合物在生产、生活中广泛存在。
(1)我国长征系列运载火箭用肼(N2H4)作燃料。N2H4与NH3有相似的化学性质。
①写出肼与盐酸反应的离子方程式:_______________________________。
②在火箭推进器中装有液态肼和双氧水,当它们混合时迅速反应生成氮气和水蒸气,写出反应的化学方程式:_____________________________________。
③火箭发射时以肼为燃料,也可以用一氧化氮作氧化剂,反应过程中若转移2mol电子则消耗燃料肼的质量为______________。
(2)汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。

写出净化过程中总反应的化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表短周期的一部分:
① | ||||||||
⑨ | ② | ③ | ④ | |||||
⑤ | ⑥ | ⑦ | ⑧ | |||||
(1) ①-⑦元素中非金属性最强的元素位于周期表中的位置为______________________。
(2) ③与⑤形成的化合物与水反应产生气体,该反应的化学方程式 _______________ 。该化合物的电子式为______
(3) ④所形成的单质与水反应的方程式 _____________。
(4) ②、③、⑨的最高价含氧酸的酸性由弱到强的顺序是__________________(用化学式表示)。
(5) 表中元素⑤和⑥的最高价氧化物的水化物之间相互反应的离子方程式为____________。
(6) ②的气态氢化物的实验室制法的反应原理:____________________;(写出化学方程式)
②的气态氢化物和它的最高价氧化物的水化物反应的产物为______________(“离子”或“共价”)化合物。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com