
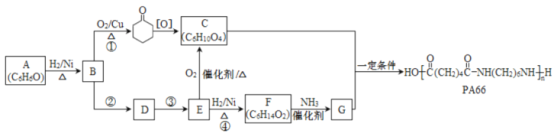
【题目】高分子化合物PA66的合成路线如下:
已知: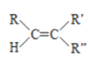
![]() RCHO+
RCHO+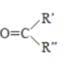
(1)A属于芳香化合物,其结构简式是____________。
(2)①的化学方程式是______________。
(3)D的结构简式是________________。
(4)④的化学方程式是______________。
(5)反应①~④中属于氧化反应的是____________(填序号)。
(6)C和G生成PA66的化学方程式是_____________。
(7)![]() 有多种同分异构体,符合下列条件的有_________种,其中任意一种同分异构体的结构简式是________。
有多种同分异构体,符合下列条件的有_________种,其中任意一种同分异构体的结构简式是________。
i. 为链状化合物且无支链; ii. 为反式结构; iii. 能发生银镜反应。
【答案】![]() 2
2![]() +O2
+O2![]() 2
2 ![]() +2H2O
+2H2O ![]() OHC(CH2)4CHO+2H2
OHC(CH2)4CHO+2H2![]() HO(CH2)6OH ①③ nHOOC(CH2)4COOH+nH2N(CH2)6NH2
HO(CH2)6OH ①③ nHOOC(CH2)4COOH+nH2N(CH2)6NH2![]() (2n-1)H2O+
(2n-1)H2O+![]() 3
3 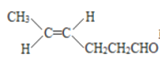
【解析】
由B的氧化产物![]() 可逆推出B为
可逆推出B为![]() ,再利用A的分子式可逆推出A的结构简式为
,再利用A的分子式可逆推出A的结构简式为![]() ;由PA66可逆推出C为HOOC(CH2)4COOH,G为H2N(CH2)6NH2;由F的分子式,可确定F为HO(CH2)6OH;则E为OHC(CH2)4CHO,借助信息,可确定D为
;由PA66可逆推出C为HOOC(CH2)4COOH,G为H2N(CH2)6NH2;由F的分子式,可确定F为HO(CH2)6OH;则E为OHC(CH2)4CHO,借助信息,可确定D为![]() 。
。
(1)A属于芳香化合物,由以上分析可得,其结构简式是![]() 。答案为:
。答案为:![]() ;
;
(2)①为![]() ,发生氧化生成
,发生氧化生成![]() ,化学方程式是2
,化学方程式是2![]() +O2
+O2![]() 2
2 ![]() +2H2O。答案为:2
+2H2O。答案为:2![]() +O2
+O2![]() 2
2 ![]() +2H2O;
+2H2O;
(3)D的结构简式是![]() 。答案为:
。答案为:![]() ;
;
(4)④中,OHC(CH2)4CHO被H2还原为HO(CH2)6OH,化学方程式是OHC(CH2)4CHO+2H2![]() HO(CH2)6OH。答案为:OHC(CH2)4CHO+2H2
HO(CH2)6OH。答案为:OHC(CH2)4CHO+2H2![]() HO(CH2)6OH;
HO(CH2)6OH;
(5)反应①~④中反应类型依次为氧化、消去、氧化、还原,属于氧化反应的是①③。答案为:①③;
(6)C和G生成PA66的化学方程式是nHOOC(CH2)4COOH+nH2N(CH2)6NH2![]() (2n-1)H2O+
(2n-1)H2O+![]() 。答案为:nHOOC(CH2)4COOH+nH2N(CH2)6NH2
。答案为:nHOOC(CH2)4COOH+nH2N(CH2)6NH2![]() (2n-1)H2O+
(2n-1)H2O+![]() ;
;
(7)![]() 有多种同分异构体,符合下列条件:i. 为链状化合物且无支链;ii. 为反式结构;iii. 能发生银镜反应,共有3种,其中任意一种同分异构体的结构简式是
有多种同分异构体,符合下列条件:i. 为链状化合物且无支链;ii. 为反式结构;iii. 能发生银镜反应,共有3种,其中任意一种同分异构体的结构简式是 、
、 、
、 。
。
答案为:3;  、
、 、
、 。
。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案科目:高中化学 来源: 题型:
【题目】向某Na2CO3、NaHCO3的混合溶液中加入少量的BaCl2固体(溶液体积变化、温度变化忽略不计),测得溶液中离子浓度的关系如图所示,下列说法正确的是( )
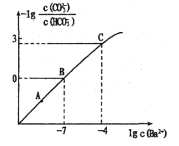
已知:Ksp(BaCO3)=2.40![]() 10-9
10-9
A.A、B、C三点对应溶液pH的大小顺序为:A>B>C
B.A点对应的溶液中存在:c(CO32-)< c(HCO3-)
C.B点溶液中 c(CO32-)=0.24mol/L
D.向C点溶液中通入CO2可使C点溶液向B点溶液转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莫尔盐[(NH4)2Fe(SO4)26H2O,Mr=392]是一种重要的还原剂,在空气中比一般的亚铁盐稳定。某学习小组设计如下实验制备少量的莫尔盐并测定其纯度。回答下列问题:
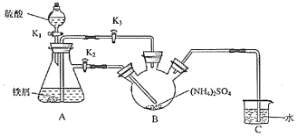
Ⅰ.制取莫尔盐:
(1)连接装置,检査装置气密性。将0.1mol(NH4)2SO4,晶体置于玻璃仪器中__________(填仪器名称),将6.0g洁浄铁屑加入锥形瓶中。
(2)①打开分液漏斗瓶塞,关闭活塞K3,打开K2、K1,加完55.0mL2molL-1稀硫酸后关闭K1.A装置中反应的离子方程式为______________。
②待大部分铁粉溶解后,打开K3、关闭K2,此时可以看到的现象为___________________________________。
③关闭活塞K2、K3,采用100℃水浴蒸发B中水分,液面产生晶膜时,停止加热,冷却结晶、___、用无水乙醇洗涤晶体。该反应中硫酸需过量,保持溶液的pH在1~2之间,其目的为_______________________________。
④装置C的作用为___________________,装置C存在的缺点是____________________。
Ⅱ.测定莫尔盐样品的纯度
(3)称取所得莫尔盐样品10.0g,用煮沸后冷却的蒸馏水配成100mL溶液,取20.00mL溶液加入稀硫酸,用0.1molL-1的KMnO4溶液滴定,达到滴定终点时消耗10.00mLKMnO4溶液。滴定反应的离子方程式为_______________________,该样品的纯度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为了验证SO2的还原性并测定产生SO2的质量,组装了下图装置。回答下列问题:
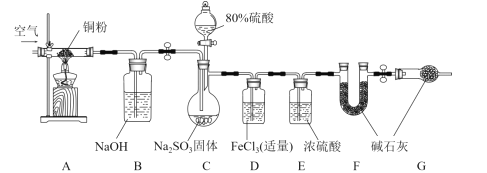
(1)C中发生反应的化学方程式是________,B装置的名称是_________,关于该套装置说法正确的是_________(填标号)。
a 组装仪器、加入药品后检查气密性 b 实验开始和最后时均需要通入空气
c 利用A、B装置是为了减小实验误差 d F、G中的碱石灰可以换为无水CaCl2
(2)甲同学认为很快可以看到D装置的现象,他的依据是_________(用离子方程式表示)。乙同学做实验时发现和甲同学预测的现象不一样,先出现棕红色,经过一段时间后变为浅绿色。于是查阅资料发现反应分为两步:
第一步:![]() (快反应)
(快反应)
第二步:![]() (慢反应)
(慢反应)
如果需要验证第一步反应是快反应,可以事先在D装置中滴加数滴_________试剂,相应的实验现象是________。
(3)学习小组通过实验后D和F装置中的数据来计算SO2的质量。D中加入足量的BaCl2溶液充分反应,经过________操作,测得沉淀为m1g,F的质量差为m2g,C中产生SO2的体积(标准状况下)为_________L。该实验的设计中,仍然存在系统误差的可能原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列“烧杯中的物质”和“向烧杯中分别加入的试剂”不能完成“实验目的”的是
① ②
② 
实验目的 | 烧杯中的物质 | 向烧杯中分别加入的试剂 | |
A | 醋酸的酸性强于苯酚 | ①醋酸 ②苯酚溶液 | 碳酸氢钠溶液 |
B | 羟基对苯环的活性有影响 | ①苯 ②苯酚溶液 | 饱和溴水 |
C | 甲基对苯环的活性有影响 | ①苯 ②甲苯 | 酸性高锰酸钾溶液 |
D | 乙醇羟基中的氢原子不如水分子中的氢原子活泼 | ①水 ②乙醇 | 金属钠 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用该矿石制备BaCl22H2O的流程如图,且三次滤渣的主要成分各不相同:
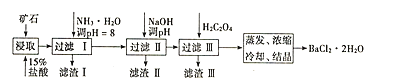
如表为常温时各离子转化为氢氧化物沉淀时的pH:
Fe3+ | Mg2+ | Ca2+ | |
开始沉淀时的pH | 1.9 | 9.1 | 11.9 |
完全沉淀时的pH | 3.2 | 11.1 | 13.9 |
(1)用15%盐酸浸取前需充分研磨,目的是______。
(2)滤渣Ⅰ的主要成分为______;加入NaOH调pH的范围为______;加入H2C2O4时应避免过量的原因是______。[已知难溶物质:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9]
(3)已知:25℃时,Ksp(BaCO3)=5.4×10-9,Ksp(CaCO3)=2.7×10-9。向CaCO3固体的溶液中加入高浓度的BaCl2溶液,有BaCO3沉淀生成,请写出该反应的离子方程式______,该反应的平衡常数K=______。
(4)取制得的BaCl22H2O(含少量杂质)2.5g配成100mL溶液,取10.00mL该溶液于烧杯中,加入足量(NH4)2C2O4溶液,过滤,洗涤,将得到的BaC2O4沉淀用过量稀硫酸溶液溶解,过滤除去BaSO4沉淀,将所得的H2C2O4溶液移入锥形瓶,用0.05mol/L高锰酸钾标准液滴定至终点。
已知:Ba2++C2O42-═BaC2O4↓
BaC2O4+2H++SO42-═BaSO4↓+H2C2O4
5H2C2O4+2MnO4-+16H+═10CO2↑+2Mn2++8H2O
①滴定中盛放高锰酸钾标准液的仪器为______,滴入最后一滴高锰酸钾溶液,锥形瓶中溶液颜色______,即说明达到滴定终点。
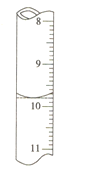
②若滴定前滴定管的读数为1.80mL,滴定终点时滴定管中液面如图,请计算BaCl22H2O的纯度为______(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物与Cu+结合形成如图所示的离子,则下列说法错误的是( )
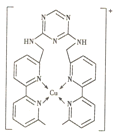
A.Cu+的核外电子排布式为[Ar]3d9
B.该离子中含有极性键、非极性键和配位键
C.该离子中碳原子的杂化方式有sp2、sp3两种
D.该离子中无手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁[Fe(C5H5)2]可用作火箭燃料添加剂、汽油的抗爆剂和橡胶的熟化剂,也可作紫外线吸收剂。可由环戊二烯(![]() )和FeCl2在三乙胺[(C2H5)3N]存在下反应制得。
)和FeCl2在三乙胺[(C2H5)3N]存在下反应制得。
(1)在元素周期表中,与Fe既同周期又同族且价层电子总数为10的元素是_____(填元素符号),该元索基态原子核外N层电子的自旋状态_______(填“相同”或“相反”)。
(2)三乙胺中电负性最小的元素是________(填元素符号);C元素的_______杂化轨道与H元素的________轨道形成_______键。
(3)下列状态的Cl中,电离最外层一个电子所需能量最大的是______(填序号)。
A. [Ne]![]() B. [Ne]
B. [Ne] ![]()
C. [Ne] ![]() D. [Ne]
D. [Ne] ![]()
(4)已知:分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成的大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成的大π键的电子数(如苯分子中的大π键可表示为![]() ),则环戊二烯负离子(
),则环戊二烯负离子(![]() )中的大π键应表示为________。
)中的大π键应表示为________。
(5)二茂铁易升华且可溶于有机溶剂中,其晶体类型为________,二茂铁的晶胞结构如图所示(未画出微粒),密度为pg·cm-3,则一个晶胞中Fe(C5H5)2。数目的计算表达式为______(设阿伏加德罗常数的值为NA)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:某温度下,铁的难溶化合物FeS在溶液中存在溶解平衡FeS(s)Fe2+ (aq) + S2-(aq),FeS在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
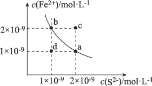
A.a点对应的Ksp(FeS)等于b点对应的Ksp(FeS)
B.c、d两点有沉淀析出的是c点
C.向d点溶液中加入FeCl3溶液,溶液中的离子浓度可实现由d点到b点的变化
D.该温度下,Ksp (FeS) =2×10-18
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com