
【题目】在一定条件下的恒容密闭容器中发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化。下列有关说法正确的是( )
CH3OH(g)+H2O(g),图1表示反应过程中能量的变化,图2表示反应过程中物质浓度的变化。下列有关说法正确的是( )

A.该反应的焓变和熵变:ΔH>0,ΔS<0
B.温度降低,该反应的平衡常数K增大
C.升高温度,n(CH3OH)/n(CO2)增大
D.从反应开始到平衡,用氢气表示的平均反应速率为2.25 mol/(L·min)
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镀作为一种新兴材料日益被重视,有“超级金属![]() 尖端金属
尖端金属![]() 空间金属”之称。工业上常用绿柱石
空间金属”之称。工业上常用绿柱石![]() 主要成分
主要成分![]() ,还含有铁等杂质
,还含有铁等杂质![]() 冶炼镀,一种简化的工艺流程如下:
冶炼镀,一种简化的工艺流程如下:
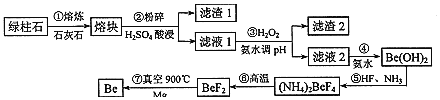
按元素周期表的对角线规则,Be和Al性质相似;几种金属阳离子的氢氧化物沉淀时的pH如表。回答下列问题:
|
|
|
| |
开始沉淀时 |
|
|
|
|
沉淀完全时 |
|
|
|
|
![]() 步骤
步骤![]() 中将熔块粉碎的目的是______;滤渣1的主要成分是_____。
中将熔块粉碎的目的是______;滤渣1的主要成分是_____。
![]() 步骤
步骤![]() 加入
加入![]() 时发生反应的离子方程式为______,从滤液1中得到沉淀的合理pH为______
时发生反应的离子方程式为______,从滤液1中得到沉淀的合理pH为______![]() 填序号
填序号![]() 。
。
A![]() 8
8![]() C
C![]()
![]()
![]() 步骤
步骤![]() 不宜使用NaOH溶液来沉淀
不宜使用NaOH溶液来沉淀![]() 的原因是______。从溶液中得到
的原因是______。从溶液中得到![]() 的实验操作是______、过滤、洗涤、干燥。
的实验操作是______、过滤、洗涤、干燥。
![]() 步骤
步骤![]() 的反应类型是______,步骤
的反应类型是______,步骤![]() 需要隔绝空气的环境,其原因是______。
需要隔绝空气的环境,其原因是______。
![]() 若绿柱石中Be0的含量为
若绿柱石中Be0的含量为![]() ,上述过程生产Be昀产率为
,上述过程生产Be昀产率为![]() ,则1t该绿柱石理论上能生产含镀量
,则1t该绿柱石理论上能生产含镀量![]() 的镀铜台金______t。
的镀铜台金______t。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列叙述正确的是( )
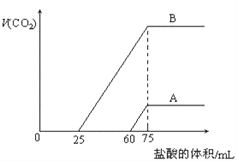
A. A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3和NaHCO3
B. B曲线中消耗盐酸0<v(HCl)<25mL时发生的离子反应为:OH-+H+=H2O H++CO32-=HCO3-
C. B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为224mL
D. 原NaOH溶液的物质的量浓度为1.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
甲 | 乙 | 丙 | |
A |
| HCl | NaOH |
B |
| NaOH | HF |
C | HCl | NaOH |
|
D |
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应A+2B![]() 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断( )
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断( )
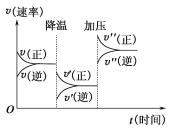
A.温度越高,该反应的化学平衡常数越大B.若A、B是气体,则D是液体或固体
C.逆反应是放热反应D.A、B、C、D均为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一选修5:有机化学基础]
聚对苯二甲酸丁二醇酯(PBT)是一种性能优异的热塑性高分子材料。PBT的一种合成路线如图所示:
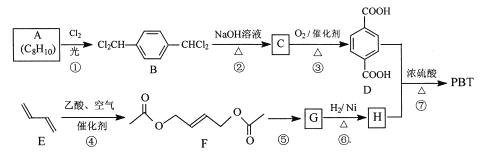
回答下列问题:
(1)A的结构简式是_________,C的化学名称是_________。
(2)⑤的反应试剂和反应条件分别是__________。
(3)F的分子式是_________,⑥的反应类型是_________。
(4)⑦的化学方程式是_________。
(5)M是H的同分异构体,同时符合_列条件的M可能的结构有_________种。
a.0.1 molM与足量金属钠反应生成氢气2.24 L(标准状况)
b.同一个碳原子上不能连接2个羟基
其中核磁共振氢谱显不3组峰,且峰而积之比为3:1:1的结构简式是_________。
(6)以2一甲基-1-3一丁二烯为原料(其它试剂任选),设计制备![]() 的合成路线:_________
的合成路线:_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2O![]() H++OH﹣△H>0,下列叙述正确的是( )
H++OH﹣△H>0,下列叙述正确的是( )
A.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
B.向水中加入氨水,平衡逆向移动,c(OH﹣)降低
C.向水中加入金属钠,平衡正向移动,c(H+)增大
D.将水加热,KW增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠是一种高效氧化剂漂白剂,主要用于棉纺、亚麻纸浆等漂白。亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2具有漂白作用,但ClO2是有毒气体。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列说法正确的是( )
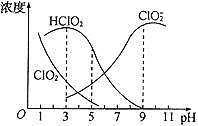
A.亚氯酸钠在酸性条件下较稳定
B.25℃时,HClO2的电离平衡常数的数值Ka=10-6
C.pH越大,该漂白剂的漂白性能越好
D.25℃,pH=3时,NaClO2溶液中:c(Na+)+c(H+)=c(ClO2-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com