
【题目】目前,回收溴单质的方法主要有水蒸气蒸馏法和萃取法等。某兴趣小组通过查阅相关资料拟采用如下方案从富马酸废液(含溴0.27%)中回收易挥发的Br2:

(1)操作X所需要的主要玻璃仪器为 ;该仪器使用前须检漏,检验方法为 。
(2)反萃取时加入20%的NaOH溶液,其离子方程式为 。
(3)反萃取所得水相酸化时,需缓慢加入浓硫酸,并采用冰水浴冷却的原因是 。
(4)溴的传统生产流程为先采用氯气氧化,再用空气水蒸气将Br2吹出;与传统工艺相比,萃取法的优点是 。
(5)我国废水三级排放标准规定:废水中苯酚的含量不得超过1.00mg·L―1,实验室可用一定浓度的溴水测定某废水中苯酚的含量,其原理如下:

①请完成相应的实验步骤:
步骤1:准确量取25.00mL待测废水于250mL锥形瓶中。
步骤2:将4.5mL 0.02mol·L―1溴水迅速加入到锥形瓶中,塞紧瓶塞,振荡。
步骤3:打开瓶塞,向锥形瓶中加入过量的0.1mol·L―1 KI溶液,振荡。
步骤4: ,再用0.01mol·L―1 Na2S2O3标准溶液滴定至终点,消耗 Na2S2O3溶液15mL(反应原理:I2+2Na2S2O3=2NaI+Na2S4O6)。
步骤5:将实验步骤1~4重复2次。
②该废水中苯酚的含量为 mg·L―1。
③步骤3若持续时间较长,则测得的废水中苯酚的含量 (填“偏高”、“偏低”或“无影响”)。
【答案】
(1)分液漏斗 (1分)
向分液漏斗中加入少量蒸馏水,检查旋塞处是否漏水,将漏斗倒转过来,检查玻璃塞是否漏水 (2分)
(2)Br2+2OH―==Br―+BrO―+H2O (2分)
(3)减少Br2的挥发 (2分)
(4)没有采用有毒气体Cl2,更环保,产品更纯净 (2分)
(5)滴入2~3滴淀粉溶液 (2分) 18.8 (2分) 偏低 (2分)
【解析】
试题分析:从实验方案可知:富马酸废液中含有Br―,电解生成Br2,加入CCl4萃取后分液,再加入NaOH溶液反萃取得到含Br―和BrO―的溶液,加入硫酸酸化发生氧化还原反应生成Br2。
(1)操作X为萃取分液,需要烧杯、分液漏斗等仪器;分液漏斗的检漏方法是:向分液漏斗中加入少量蒸馏水,检查旋塞处是否漏水,将漏斗倒转过来,检查玻璃塞是否漏水。
(2)反萃取时加入20%的NaOH溶液反应生成 NaBr、NaBrO和H2O,反应的离子方程式为:Br2+2OH― ==Br―+BrO―+H2O。
(3)反萃取所得水相酸化时,需加入浓硫酸,使Br―和BrO―转化为Br2,因为溴单质易挥发,且浓硫酸溶解时放热,所以需缓慢加入浓硫酸,并采用冰水浴冷却。
(4)氯气是有毒气体,且空气吹出的溴单质易混有氯气,使溴不纯净,所以萃取法的优点是:没有采用有毒气体Cl2,更环保,产品更纯净。
(5)①硫代硫酸钠溶液滴定碘单质,加入淀粉溶液做指示剂;滴入2~3滴淀粉溶液,再用0.01 mol·L―1 Na2S2O3标准溶液滴定至终点。
②依据定量关系Br2~I2~2Na2S2O3可求出与KI反应的溴为:0.015L×0.01 mol·L―1×![]() =7.5× 10―5 mol,则25mL废水中苯酚的物质的量为=(0.02 mol·L―1×0.0045 L―7.5×10―5mol)×
=7.5× 10―5 mol,则25mL废水中苯酚的物质的量为=(0.02 mol·L―1×0.0045 L―7.5×10―5mol)×![]() =5×10―6mol,故该废水中苯酚的含量为=
=5×10―6mol,故该废水中苯酚的含量为=![]() =0.0188g·L―1=18.8 mg·L―1。
=0.0188g·L―1=18.8 mg·L―1。
③步骤3持续的时间较长,空气中的O2也会把I―氧化为I2,造成滴定时消耗的标准溶液的体积偏大,计算所得剩余溴的物质的量偏大,则与苯酚反应的溴的物质的量偏小,最终测定的苯酚含量偏低。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】下图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336 mL(标准状况)气体。回答:

(1)直流电源中,M为____________极。
(2)Pt电极上生成的物质是____________,其质量为____________g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为:2∶_______∶________∶_________。
(4)AgNO3溶液的浓度(填“增大”“减小”或“不变”。下同)____________,H2SO4溶液的浓度____________。
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”(Funiulele)。有一种有机物的键线式也酷似牛形(下图所示),故称为牛式二烯炔醇。下列有关说法正确的是( )

A.牛式二烯炔醇含有4种官能团
B.牛式二烯炔醇不能使酸性KMnO4溶液褪色
C.1 mol牛式二烯炔醇最多可跟4mol Br2发生加成反应
D.该有机物的化学式为C29H44O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是制备NH4NO3和Na2S2O4的一种工艺流程:(已知HNO2为弱酸)

(1)装置Ⅰ的作用为 ,写出该装置中反应的离子方程式 。
(2)若装置Ⅱ中产生的硝酸根和亚硝酸根的物质的量比为1∶1,写出反应的离子方程式_______;区别硝酸钠和亚硝酸钠晶体的方法是(写一种)______。
(3)装置Ⅳ中不通入氧气会产生的后果是________。
(4)若起始时通入等物质的量的NO和SO2,则通入n(NH3)∶ n(O2)=_________(假设过步骤中均完全转化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 | |
沸点/℃ | 64.7 | 249 | 199.6 | |
密度/g.cm-3 | 0.792 | 1.2659 | 1.0888 | |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2 g苯甲酸和20 mL甲醇(密度约为0.79 g·cm-3),再小心加入3 mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是______________;若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式:_________________________________________。
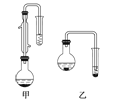
(2)甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用__________装置(填“甲”或“乙”)
(3)反应物CH3OH应过量,理由是__________________________。
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称。

(5)通过计算,苯甲酸甲酯的产率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳整理是科学学习的重要方法之一。氧族元素的部分性质归纳整理如下:
|
|
|
|
|
单质熔点/℃ | -218,4 | 113 | ? | 450 |
单质沸点/℃ | -183 | 444.6 | 685 | 989 |
主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | ? |
原子半径/nm | 0.074 | 0.102 | ? | 0.136 |
单质与氢化合的难易程度 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接 |
请根据上表数据以及数据变化趋势,回答下列问题:
(1)硒的熔点范围可能是:________________;
(2)碲(Te)可能的化合价有:___________________;
(3)硒(Se)的原子半径可能在_______________________之间。
(4)从单质与氢化合的难易程度可以推测出,O、S、Se、Te的非金属性逐渐_________(增强、减弱)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热法炼铬废渣主要成分为Al2O3和Cr2O3,还含有MgO、FeO、Fe2O3等杂质,以下是以炼铬废渣为原料回收Al2O3和Cr2O3的流程图:

已知:
①“焙烧”涉及的主要反应:Na2CO3+Al2O3![]() 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
Cr2O3+Na2CO3+O2![]() Na2CrO4+CO2↑(未配平);
Na2CrO4+CO2↑(未配平);
②滤液2中涉及的反应:8CrO42--+3S2O32-+34H+===6SO42-+8Cr3++17H2O
③Ksp[Cr(OH)3]=8×10-32
根据题意回答下列问题:
(1)请完成下列化学方程式的配平:
Cr2O3+ Na2CO3+ O2 ![]() Na2CrO4+ CO2↑;
Na2CrO4+ CO2↑;
(2)炼铬废渣在焙烧前需球磨粉碎,其目的是 。
(3)滤渣1的主要成分是 。
(4)流程中可以循环利用的物质是 。
(5)写出步骤Ⅲ“碳分”的离子反应方程式: 。
(6)滤液2还原后的溶液中为使Cr3+沉淀完全,溶液pH应小于 。(已知:lg5=0.7;当溶液中离子浓度不大于1×10-5mol/L时,可以认为不含该离子)
(7)滤液2经多步操作还可以获得K2Cr2O7晶体,其操作依次是:加入稀硫酸酸化,加入KCl固体、蒸发浓缩、操作a、过滤、操作b、干燥。
①加硫酸酸化的目的是 。
②操作a、操作b分别是 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能.已知部分化学键的键能如下:
化学键 | N—H | N—N | O=O | N≡N | O—H |
键能(kJ·mol-1) | 386 | 167 | 498 | 946 | 460 |
(1)发射神舟飞船的长征火箭用了肼(N2H4,气态)为燃料,若它在氧气(气态)中燃烧,生成N2(气态)和H2O(液态)。1 mol肼完全燃烧时放出的热量为________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH 溶液。肼-空气燃料电池放电时,正极的电极反应式是______________________________________。
(3)已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构。试推测1个N60的结构含有________个N—N键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式 。
(2)298 K时,在2L的密闭容器中,发生可逆反应:2NO2(g)![]() N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题。

①298K时,该反应的平衡常数为________。
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 。

a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol 、n(N2O4)=1.2mol,
则此时V(正) V(逆)(填“>”、“<”或“=”)。
 (3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,

①水的电离程度最大的是 ;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数
K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com