
【题目】含硫烟气(主要成分为SO2)的处理备受关注,主要有以下两种方法。请回答:
I .碱液吸收法
步骤1:用足量氨水吸收SO2
步骤2:再加入熟石灰,发生反应2NH4++Ca2++2OH-+SO32-=CaSO3↓+2NH3·H2O
(1)步骤1中反应的离子方程式为_______________________。
(2)已知:25°C时,Ksp(CaSO3)=b,步骤2中反应的平衡常数K=a。该温度下,Kb( NH3·H2O)=__________________(用含a、b的代数式表示)。
II.水煤气还原法
己知:①2CO(g)+SO2(g)![]() S(l)+2CO2(g) △H1=-37.0 kJ·mol-1
S(l)+2CO2(g) △H1=-37.0 kJ·mol-1
②2H2(g)+ SO2(g)![]() S(l)+2H2O(g) △H2=+45.4 kJ·mol-1
S(l)+2H2O(g) △H2=+45.4 kJ·mol-1
③CO的燃烧热△H3=-283 kJ·mol-1
(3)1molS(l)在O2(g)中完全燃烧生成SO2(g)的热化学方程式为____________。
(4)反应②的正反应的活化能为E1 kJ·mol-1,其逆反应的活化能E2=_____ kJ·mol-1。
(5)在一定压强下,发生反应②。平衡时,α(SO2)与原枓气投料比[![]() ]和温度(T) 的关系如图所示。
]和温度(T) 的关系如图所示。

①α(H2):N_____M (填“>”、“<”或 “ = ”)。
②逆反应速率:M_____Q(填“>”、“<”或 “ = ”)。
(6)t℃时,向10L恒容密闭容器中充入2 molCO(g)、2 mol SO2(g)和2 mol H2(g)。发生反应①和反应②。5mim达到平衡时,SO2(g)和CO2(g) 的物质的量分别为0.4mol、1.6mol。该温度下,反应②的平衡常数K=__________。
【答案】 2NH3·H2O+ SO2= 2NH4++ SO32-+ H2O ![]() S(l)+O2(g)=SO2(g) △Hl=-529.0 kJ·mol-1 E1-45.4 < > 400
S(l)+O2(g)=SO2(g) △Hl=-529.0 kJ·mol-1 E1-45.4 < > 400
【解析】(1)步骤1中用足量氨水吸收SO2反应生成亚硫酸铵,反应的离子方程式为2NH3·H2O+ SO2= 2NH4++ SO32-+ H2O,故答案为:2NH3·H2O+ SO2= 2NH4++ SO32-+ H2O;
(2) 反应2NH4++Ca2++2OH-+SO32-=CaSO3↓+2NH3·H2O的平衡常数K= =
=![]() ,因此Kb( NH3·H2O)=
,因此Kb( NH3·H2O)= ![]() ,故答案为:
,故答案为: ![]() ;
;
II. (3)①2CO(g)+SO2(g)![]() S(l)+2CO2(g) △H1=-37.0 kJ·mol-1 ,②2H2(g)+ SO2(g)
S(l)+2CO2(g) △H1=-37.0 kJ·mol-1 ,②2H2(g)+ SO2(g)![]() S(l)+2H2O(g) △H2=+45.4 kJ·mol-1 ,③CO的燃烧热△H3=-283 kJ·mol-1 即CO(g)+
S(l)+2H2O(g) △H2=+45.4 kJ·mol-1 ,③CO的燃烧热△H3=-283 kJ·mol-1 即CO(g)+ ![]() O2(g)═CO2(g)△H2=-283KJmol-1,根据盖斯定律,将③×2-①得S(l)+O2(g)=SO2(g) △Hl=(-283KJmol-1)×2-(-37.0 kJ·mol-1)=-529.0 kJ·mol-1,故答案为:S(l)+O2(g)=SO2(g) △Hl=-529.0 kJ·mol-1;
O2(g)═CO2(g)△H2=-283KJmol-1,根据盖斯定律,将③×2-①得S(l)+O2(g)=SO2(g) △Hl=(-283KJmol-1)×2-(-37.0 kJ·mol-1)=-529.0 kJ·mol-1,故答案为:S(l)+O2(g)=SO2(g) △Hl=-529.0 kJ·mol-1;
⑷反应②2H2(g)+ SO2(g)![]() S(l)+2H2O(g) △H2=+45.4 kJ·mol-1,的正反应的活化能为E1 kJ·mol-1,则其逆反应的活化能E2= E1-45.4kJ·mol-1,故答案为:E1-45.4;
S(l)+2H2O(g) △H2=+45.4 kJ·mol-1,的正反应的活化能为E1 kJ·mol-1,则其逆反应的活化能E2= E1-45.4kJ·mol-1,故答案为:E1-45.4;
(5)①根据图像,α(SO2)一定时,![]() 越大,氢气的转化率越大,α(H2):N<M,故答案为:<;
越大,氢气的转化率越大,α(H2):N<M,故答案为:<;
②该反应属于吸热反应,升高温度,平衡正向移动,反应物的转化率增大,根据图像,相同![]() 条件下,T1时α(SO2)大于T2时的α(SO2),说明T1>T2,温度越高,反应速率越快,逆反应速率:M>Q,故答案为:>;
条件下,T1时α(SO2)大于T2时的α(SO2),说明T1>T2,温度越高,反应速率越快,逆反应速率:M>Q,故答案为:>;
(6) ① 2CO(g)+SO2(g)![]() S(l)+2CO2(g)
S(l)+2CO2(g)
起始(mol/L) 0.2 0.2 0
反应 0.16 0.08 0.16
平衡
② 2H2(g)+ SO2(g)![]() S(l)+2H2O(g)
S(l)+2H2O(g)
起始(mol/L)0.2 0.12 0
反应 0.16 0.08 0.16
平衡 0.04 0.04 0.16
反应②的平衡常数K=![]() =400,故答案为:400。
=400,故答案为:400。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】填写下列空白[第(1)~(4)小题用元素符号填写]。
(1)第三周期原子半径最小的元素________。
(2)第一电离能最大的元素________。
(3)电负性最大的元素________。
(4)第四周期中第一电离能最小的元素________。
(5)含有8个质子,10个中子的原子的化学符号________。
(6)最外层电子排布为4s24p1的原子的核电荷数为________。
(7)周期表中最活泼的非金属元素原子的轨道表示式为___________________。
(8)某元素核外有三个电子层,最外层电子数是核外电子总数的![]() ,写出该元素原子的电子排布式是__________________。
,写出该元素原子的电子排布式是__________________。
(9)写出铜元素在周期表中的位置________________,它位于________区。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F对花香和果香具有提升作用,故常用于化妆品工业和食品工业。有机物F可以用下面的设计方案合成。

请回答下列问题:
(1)写出A的结构简式:_________________。
(2)①的反应类型:_______________。
(3)写出反应③的化学方程式:_________________________________________。
(4)F的同分异构体中含有—COO—的一取代苯结构有多个。请写出其中能发生银镜反应的两种物质的结构简式______________、___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )

A. 原子半径:Z>W>X>Y
B. 元素X、Z的最高化合价分别与其主族序数相等
C. 最高价氧化物对应水化物的酸性:Y>X>W
D. 最简单气态氢化物的热稳定性:Y>X>W>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用 98%、密度为1.84g/cm3的浓硫酸配制0.2mol/L的 H2SO4溶液1000mL.
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、 、 。
(2)其操作步骤可分解为以下几步:
A.用量筒量取 mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,
并用玻璃棒搅拌。
B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里。
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里。
D.检查容量瓶是否漏水。
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处。
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液。
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切。
请据此填写:
①完成上述步骤中的空白处。
②补充完成正确的操作顺序(用字母填写):
( D )→( A )→( C )→( )→( )→( )→( F )。
③将浓硫酸在烧杯中稀释后移入容量瓶时,必须_________________方可移液.
(3)试分析下列操作对所配溶液的浓度有何影响
①量取浓硫酸时眼睛俯视刻度线,会导致所配溶液浓度会 ;(填:偏高、偏低、或无影响,下同)
②定容时,眼睛俯视刻度线,所配溶液浓度会 ;
③定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度。所配溶液浓度会 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7·10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3 、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取的七水硫酸镁在印染、造纸和医药等工业上都有广泛的应用。硼镁泥制取七水硫酸镁的工艺流程如下:

回答下列问题:
(1)Na2B4O7·10H2O中B的化合价为________________。
(2)Na2B4O7易溶于水,也较易发生水解:B4O72-+7H2O![]() 4H3BO3(硼酸)+2OH-,(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:_________________________________。
4H3BO3(硼酸)+2OH-,(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:_________________________________。
(3)滤渣B中含有不溶于稀盐酸但能溶于浓盐酸的黑色固体,写出生成黑色固体的离子方程式_________________。
(4)加入MgO的目的是_____________________。
(5)己知MgSO4、CaSO4的溶解度如下表:
温度(℃) 溶解度(g) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
操作“A”是将MgSO4:和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明“操作A”步骤为____________________。
(6)Na2B4O7·10H2O失去全部结晶水后的硼砂与金属钠、氢气及石英砂一起反应可制备有机化学中的“万能还原剂——NaBH4”(该过程B的化合价不变)。
①写出NaBH4的电子式_____________。
②“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克H2的还原能力。NaBH4的有效氢含量为_____(计算结果保留两位小数)。
③在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应3A(g)![]() 3B(?)+C(?) △H>0达到化学平衡后,
3B(?)+C(?) △H>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
①若B、C都是气体,气体的平均相对分子质量 ;
②若B、C都不是气体,气体的平均相对分子质量 ;
③若B是气体,C不是气体,气体的平均相对分子质量 ;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是 态,C是 态。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂。某课题组经查阅资料后设计合成铝氢化钠的简易流程如图所示。

已知:①AlCl3、NaH、NaAlH4遇水都能迅速发生反应。
②常温下,可用高锰酸钾、氯酸钾、重铬酸钾、次氯酸钙等与浓盐酸反应制取氯气。
(1)铝氢化钠遇水发生剧烈反应,甚至可能发生爆炸,其原因是_______________。写出铝氢化钠与水反应的化学方程式_____________________。
(2)甲同学设计实验制备无水氯化铝的装置如图所示。
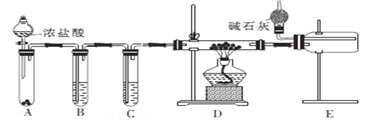
①装置E中干燥管的作用是_______________________。
②点燃装置D处酒精灯之前 需先排尽装置内的空气,其操作方法是________________。
(3)乙同学分析甲同学设计的装置后,认为只改变A、B、D中的试剂就可以用甲同学设计的装置制备NaH。
①试管B中的试剂改为____________________。
②若操作不当,则制得的NaH产品中可能含有的杂质有_________________。
(4)丙同学设计以下4种装置测定铝氢化钠样品的纯度(假设杂质不参与反应)。




从易操作性、准确性角度考虑,宜选装置________。铝氢化钠与水完全反应,冷却至室温的标志是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com