
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂。某课题组经查阅资料后设计合成铝氢化钠的简易流程如图所示。

已知:①AlCl3、NaH、NaAlH4遇水都能迅速发生反应。
②常温下,可用高锰酸钾、氯酸钾、重铬酸钾、次氯酸钙等与浓盐酸反应制取氯气。
(1)铝氢化钠遇水发生剧烈反应,甚至可能发生爆炸,其原因是_______________。写出铝氢化钠与水反应的化学方程式_____________________。
(2)甲同学设计实验制备无水氯化铝的装置如图所示。
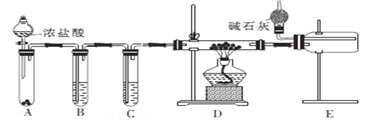
①装置E中干燥管的作用是_______________________。
②点燃装置D处酒精灯之前 需先排尽装置内的空气,其操作方法是________________。
(3)乙同学分析甲同学设计的装置后,认为只改变A、B、D中的试剂就可以用甲同学设计的装置制备NaH。
①试管B中的试剂改为____________________。
②若操作不当,则制得的NaH产品中可能含有的杂质有_________________。
(4)丙同学设计以下4种装置测定铝氢化钠样品的纯度(假设杂质不参与反应)。




从易操作性、准确性角度考虑,宜选装置________。铝氢化钠与水完全反应,冷却至室温的标志是______。
【答案】 反应放出大量热量使生成的H2迅速膨胀而爆炸 NaAlH4+2H2O═NaAlO2+4H2↑ 吸收剩余的氯气并避免空气中的水蒸气进入D中 先将装置A中的分液漏斗打开,反应一段时间,使D中玻璃管充满黄绿色气体 NaOH溶液(或其他合理答案) Na2O2(或Na等其他合理答案) 乙 连续两次读取的H2体积相等
【解析】(1)NaAlH4与水反应生成NaAlO2和H2,化学方程式为:NaAlH4+2H2O=NaAlO2+4H2↑;由已知①可得,NaAlH4遇水能迅速发生反应,放出大量热使生成的H2迅速膨胀而可能引起爆炸。
(2)由制备无水氯化铝的装置可知,A为“固-液![]() ”制Cl2装置,B为除去Cl2中HCl的装置,C为吸水干燥装置,D为Al和Cl2反应装置,E为收集AlCl3装置。①因为AlCl3遇水能迅速反应,所以E中碱石灰的作用是:吸收剩余氯气和防止空气中的水蒸气进入D中。②点燃装置D处酒精灯之前,先打开装置A中的分液漏斗,反应一段时间,使D中玻璃管充满黄绿色气体,从而排尽装置内的空气。
”制Cl2装置,B为除去Cl2中HCl的装置,C为吸水干燥装置,D为Al和Cl2反应装置,E为收集AlCl3装置。①因为AlCl3遇水能迅速反应,所以E中碱石灰的作用是:吸收剩余氯气和防止空气中的水蒸气进入D中。②点燃装置D处酒精灯之前,先打开装置A中的分液漏斗,反应一段时间,使D中玻璃管充满黄绿色气体,从而排尽装置内的空气。
(3)①若用上述装置制备NaH,只要将A中试剂改为金属锌,B中用NaOH等碱性溶液除去挥发出的HCl气体,D中试剂改为金属钠,就可以达到目的。②该装置无法隔绝氧气,,若操作不当,可能会使NaH中含有Na2O2杂质;若氢气不足,Na会有剩余。
(4)丙同学是用测氢气体积的方法来测定NaH样品纯度的,甲装置会导致内部压强大于大气压强,丙装置无法测氢气的体积,丁装置与甲装置类似,会导致结果偏大,故选乙装置;若两次测得的氢气体积相同,则说明已冷却至室温。


科目:高中化学 来源: 题型:
【题目】含硫烟气(主要成分为SO2)的处理备受关注,主要有以下两种方法。请回答:
I .碱液吸收法
步骤1:用足量氨水吸收SO2
步骤2:再加入熟石灰,发生反应2NH4++Ca2++2OH-+SO32-=CaSO3↓+2NH3·H2O
(1)步骤1中反应的离子方程式为_______________________。
(2)已知:25°C时,Ksp(CaSO3)=b,步骤2中反应的平衡常数K=a。该温度下,Kb( NH3·H2O)=__________________(用含a、b的代数式表示)。
II.水煤气还原法
己知:①2CO(g)+SO2(g)![]() S(l)+2CO2(g) △H1=-37.0 kJ·mol-1
S(l)+2CO2(g) △H1=-37.0 kJ·mol-1
②2H2(g)+ SO2(g)![]() S(l)+2H2O(g) △H2=+45.4 kJ·mol-1
S(l)+2H2O(g) △H2=+45.4 kJ·mol-1
③CO的燃烧热△H3=-283 kJ·mol-1
(3)1molS(l)在O2(g)中完全燃烧生成SO2(g)的热化学方程式为____________。
(4)反应②的正反应的活化能为E1 kJ·mol-1,其逆反应的活化能E2=_____ kJ·mol-1。
(5)在一定压强下,发生反应②。平衡时,α(SO2)与原枓气投料比[![]() ]和温度(T) 的关系如图所示。
]和温度(T) 的关系如图所示。

①α(H2):N_____M (填“>”、“<”或 “ = ”)。
②逆反应速率:M_____Q(填“>”、“<”或 “ = ”)。
(6)t℃时,向10L恒容密闭容器中充入2 molCO(g)、2 mol SO2(g)和2 mol H2(g)。发生反应①和反应②。5mim达到平衡时,SO2(g)和CO2(g) 的物质的量分别为0.4mol、1.6mol。该温度下,反应②的平衡常数K=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列组成细胞的化合物与其功能不符的是
A. 无机盐——维持细胞的渗透压
B. 葡萄糖——细胞主要的能源物质
C. 蛋白质——生命活动的主要体现者
D. 脱氧核糖核酸——所有生物的遗传物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2与以SO2能发生反应:NO2(g)+SO2(g)![]() SO3(g)+NO(g)。
SO3(g)+NO(g)。
(1)上述反应涉及的四种氧化物中,_________(填化学式)属于酸性氧化物。
(2)已知:2NO(g)+O2(g)=2NO2(g)△H1=-113.0kJ·mol-1
2SO2(g)+O2(g) ![]() 2SO3(g)△H2=-196.6kJ·mol-1
2SO3(g)△H2=-196.6kJ·mol-1
则NO2(g)+SO2(g)![]() SO3(g)+NO(g)△H=__________
SO3(g)+NO(g)△H=__________
(3)在一恒容密闭容器中,改变原料气配比[n0(NO2):n0(SO2)]进行多组实验(每次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如图所示。

① 当容器内____(填字母)不再随时间的变化而改变时,可以判断反应达到了化学平衡状态。
a.气体的压强 b.气体的平均摩尔质量 c.气体的密度 d. NO2的体积分数
② 若A点对应的实验中,SO2(g)的起始浓度为c0mol/L,经过t min后反应达到平衡,则反应从起始至t min 内的化学反应速率v(NO2)=_____mol/(L·min)。
③ 若要使图中C点的平衡状态变为B 点的平衡状态,则应采取的措施是_________,若要使图中A点的平衡状态变为B 点的平衡状态,则应采取的措施是___________。
(4)将NO2与SO2的混合气体[n0(NO2):n0(SO2)=1]通入2mL0.1mol/L氯化钡溶液中,只生成一种白色沉淀物M,M的化学式为_______,当溶液中的Ba2+恰好完全沉淀(Ba2+的浓度等于1.0×10-5mol/L),通入的混合气体在标准状况下的体积约为______L。(M的Kap=1.0×10-9)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是 ( )

①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol
A.①②③ B.①②⑤ C.①②⑤⑥ D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是
A. Al2O3熔点高,可用作耐高温材料
B. FeCl3溶液呈酸性,可用于腐蚀电路板上的Cu
C. 石墨具有导电性,可用于制铅笔芯
D. 浓硫酸具有强氧化性,可用于干燥CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
Ⅰ、现有下列5种有机物:①CH2 = CH2 ②CH3 C≡CH ③CH3CH2CH2OH
④CH3 O CH2CH3 ⑤![]()
请回答:
(1)属于烃类的是____________(填序号,下同),与①互为同系物的是___________,与③互为同分异构体的是____________.
(2)用系统命名法给⑤命名,其名称为_________________________.
Ⅱ、(1)分子式为C4Hl0O的同分异构体共有____________种;
(2)分子式为C3H6O2的链状有机物,核磁共振氢谱上峰的数目及强度比分别为:①3∶3;②2∶2∶1∶1,则它们可能的结构简式依次为:
①_______________________;② ________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在50 mL过氧化氢溶液中加入1 g MnO2粉末,标准状况下放出气体的体积和时间的关系如图所示,下列说法不正确的是( )

A. 标准状况下,实验放出一半气体所需的时间为1 min
B. A、B、C、 D各点反应速率中A点最慢,D点快
C. 0~2 min内产生O2的平均反应速率为22.5 mL·min-1
D. 本实验中影响反应速率的因素只有催化剂和H2O2的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com