
【题目】氨在国防、工农业等领域发挥着重要作用。工业以甲烷为原料生产氨气的过程如下:![]()
(1)过程Ⅰ中,有关化学反应的能量变化如下图所示

反应①为___________(“吸热”或“放热”),CH4(g)与H2O(g)反应生成CO(g)和H2 (g)的热化学方程式是________________。
(2)CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ )溶液吸收,其反应原理为:[Cu(NH3)2CH3COO](aq)+CO(g)+NH3(g)![]() [Cu(NH3)3]CH3COOCO(1),
[Cu(NH3)3]CH3COOCO(1), ![]()
①N元素在周期表中的位置为__________,NH3的电子式为__________。
②所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是__________(选填字母)。
a.高温、高压 b.高温、低压 c.低温、低压 d.低温、高压
(3)合成NH3的反应为放热反应,如果该反应平衡时,只改变一个条件,再次达到新平衡时,平衡常数K值变大。关于该反应的说法正确的是__________(填字母序号)。
A.一定向正反应方向移动 B.在平衡移动时正反应速率先增大再减小
C.一定向逆反应方向移动 D.在平衡移动时逆反应速率先减小再增大
(4)400℃,28MPa时,将1molN2和3mol H2混合充入体积可变的密闭容器中,加入催化剂,10分钟后反应达到平衡时N2转化率为60%。该温度下的平衡常数Kp=__________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。

(5)一种直接供氨式固体氧化物燃料电池能量转化率达85%,其结构示意图如图所示:
①负极的电极反应式是_____________。
②用该电池电解300mL的饱和食盐水。一段时间后,溶液pH=13(忽略溶液体积的变化),则消耗NH3溶液的体积是_____L。(标准状况)
【答案】 吸热 CH4(g) + H2O(g) = CO(g) + 3H2 (g) △ H = +118.1kJ/mol 第二周期第ⅤA族 ![]() b AD 0.021(MPa)-2 或
b AD 0.021(MPa)-2 或![]() (MPa)-2 2NH3 -6e- + 3O2- =N2 + 3H2O 0.224L
(MPa)-2 2NH3 -6e- + 3O2- =N2 + 3H2O 0.224L
【解析】(1)由图可得热化学方程式为:①CH4(g) + 2H2O(g) = CO2(g) + 4H2 (g) H = +76.9kJ/mol,②CO(g) + H2O(g) = CO2(g) + H2 (g) H = -41.2kJ/mol,根据盖斯定律①-②得:CH4(g) + H2O(g) = CO(g) + 3H2 (g) H = +118.1kJ/mol,故答案为:吸热;CH4(g) + H2O(g) = CO(g) + 3H2 (g) H = +118.1kJ/mol。
(2)①N元素在元素周期表中位于第二周期第VA族,NH3的电子式为:![]() ,故答案为:第二周期第VA族;
,故答案为:第二周期第VA族;![]() ;②吸收CO后的乙酸二氨合铜溶液经过适当处理后又可再生,回复其吸收CO的能力以供循环使用,依据化学平衡[Cu(NH3)2CH3COO](aq)+CO(g)+NH3(g)
;②吸收CO后的乙酸二氨合铜溶液经过适当处理后又可再生,回复其吸收CO的能力以供循环使用,依据化学平衡[Cu(NH3)2CH3COO](aq)+CO(g)+NH3(g)![]() [Cu(NH3)3]CH3COOCO(1),H<0,反应是气体体积减小的放热反应,平衡逆向进行是再生原理,故再生适宜条件是高温低压,答案为:b。
[Cu(NH3)3]CH3COOCO(1),H<0,反应是气体体积减小的放热反应,平衡逆向进行是再生原理,故再生适宜条件是高温低压,答案为:b。
(3)化学平衡常数只与温度有关,合成氨反应为放热反应,该反应平衡时,如果只改变一个条件,再次达到平衡时,平衡常数K值变大,说明温度降低,平衡向正反应方向移动,逆反应速率先减小再增大,故AD正确
(4)10分钟后反应达到平衡时N2转化率为60%,则反应的N2的物质的量为0.6mol,列三段式:

氮气、氢气、氨气的平衡分压分别为![]() ×28MPa=4MPa,12MPa,12MPa,所以平衡常数Kp=
×28MPa=4MPa,12MPa,12MPa,所以平衡常数Kp=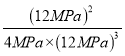 =
=![]() (MPa)-2。
(MPa)-2。
(5)①此燃料电池中,负极为NH3发生氧化反应,与固体电解质中的O2-生成N2和H2O,电极反应式:2NH3-6e-+3O2-=N2+3H2O。②电解后溶液pH=13,则OH-浓度为0.1mol/L,溶液体积0.3L,则OH-物质的量为0.03mol,故电解过程中转移的电子为0.03mol,由电子守恒和电极反应式2NH3-6e-+3O2-=N2+3H2O可知,消耗的NH3为0.01mol,标准状况下的体积为0.224L。


科目:高中化学 来源: 题型:
【题目】在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现。铁片腐蚀过程中发生的总化学方程式:2Fe+2H2O+O2===2Fe(OH)2,Fe(OH)2进一步被氧气氧化为Fe(OH)3,再在一定条件下脱水生成铁锈,其原理如图。下列说法正确的是( )

A. 铁片发生还原反应而被腐蚀
B. 铁片腐蚀最严重区域应该是生锈最多的区域
C. 铁片腐蚀中负极发生的电极反应:2H2O+O2+4e-===4OH-
D. 铁片里的铁和碳与食盐水形成无数微小原电池,发生了电化学腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铁矿为原料制硫酸会产生大量的废渣,合理利用废渣可以减少环境污染,变废为宝。工业上利用废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下:

(1)在废渣溶解操作时,应选用________溶解(填字母)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.硫酸
(2) 为了提高废渣的浸取率,可采用的措施有哪些?_______________(至少写出两点)。

(3)物质A是一种氧化剂,工业上最好选用________(供选择使用的有:空气、Cl2、MnO2),其理由是_______________。氧化过程中发生反应的离子方程式为_________________。
(4)根据如图有关数据,你认为工业上氧化操作时应控制的条件(从温度、pH和氧化时间三方面说明)是:______________________________________________________。
(5) 铵黄铁矾中可能混有的杂质有Fe(OH)3、________。
(6) 铵黄铁矾的化学式可表示为(NH4)xFey(SO4)z(OH)w,其化学式可通过下列实验测定:
① 称取一定质量的样品加入稀硝酸充分溶解,将所得溶液转移至容量瓶并配制成100.00 mL溶液A。
② 量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体9.32 g。
③ 量取25.00 mL溶液A,加入足量NaOH溶液,加热,收集到标准状况下气体448mL,同时有红褐色沉淀生成。
④ 将步骤③所得沉淀过滤、洗涤、灼烧,最终得固体4.80 g。
通过计算,可确定铵黄铁矾的化学式为___________________________。(已知铵黄铁矾的摩尔质量为960gmol-1,计算过程中不考虑固体损失和气体溶解。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在浓度均为4.0 mol·L-1的盐酸和硫酸各100 mL溶液中,分别加入等质量的锌粉,充分反应后生成气体体积比为2∶3,则加入锌粉的质量是
A. 6.5 g B. 13.0 g C. 19.5 g D. 26.0 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境监察局常用“定电位”NOx传感器来监测化工厂的氮氧化物气体是否达到排放标准,其工作原理如图所示。下列说法不正确的是( )

A. “对电极”是负极
B. “工作电极”上发生的电极反应为NO2+2e-+2H+═NO+H2O
C. 传感器工作时H+由工作电极移向对电极
D. 对电极的材料可能为活泼金属锌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.尿黑酸症是一种引起酪氨酸在人体内非正常代谢的遗传病,酪氨酸在体内有如图转化:

下列说法错误的是(____)
A.酪氨酸既能与盐酸反应,又能与NaOH溶液反应
B.1mol尿黑酸与足量浓溴水反应,最多消耗3molBr2
C.对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个
D.对羟基苯丙酮酸分子核磁共振氢谱有4个峰,有1个手性碳原子
II.1,6一己二酸(G)是合成尼龙的主要原料之一,可用烃A氧化制备。制备G的合成路线如图1:

回答下列问题:
(1)化合物A的质谱图如图2,则A的化学名称为___________。
(2)B→C的反应类型为___________。D→E的反应类型为______________。
(3)F的结构简式为____________。
(4)由G合成尼龙的化学方程式为_______________,与G含有相同官能团的同分异构体有_______种,其中核磁共振氢谱为4组峰,且峰面积比为1:1:2:6的结构简式是___________(写出一种即可)。
由A通过两步反应制备1,3-环己二烯的合成路线为_____________________。
(其它试剂任选,合成路线常用的表示方式为:CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497 kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。则相同条件下破坏1molNO中化学键需要吸收的能量为_______kJ。
(2)25℃时,pH=5的CH3COOH溶液中,由水电离出的氢离子浓度c(H+)=____ kJ·mol-1;若加入少量NaOH固体,则溶液中 _____(填“增大”、“减小”或“不变”)。
_____(填“增大”、“减小”或“不变”)。
(3)25℃下,向某Na2CO3溶液中加入稀盐酸,其含碳元素的微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。

①在同一溶液中,H2CO3、HCO3-、CO32-______(填“能”或“不能”)大量共存。
②当pH =7时,溶液中含碳元素的微粒主要为________。溶液中各种离子的物质的量浓度大小关系为______________。
③反应的CO32-+H2O![]() HCO3-+OH-的平衡常数Kh=______。
HCO3-+OH-的平衡常数Kh=______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com