
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 | I5 |
| Y | 584 | 1823 | 2751 | 11584 | 14837 |
| ||
| ||


科目:高中化学 来源: 题型:
| A、200mL 2mol/L MgCl2溶液 |
| B、1000mL 2.5mol/L NaCl溶液 |
| C、300mL 5mol/L KCl溶液 |
| D、250mL 1mol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | ①2由C、H、O三种元素组成; ②球棍模型为: 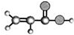 ; ;③能与NH3在一定条件下反应生成丙烯酰胺CH2=CHCONH2; ④能使溴水褪色. |
| B | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与A反应生成相对分子质量为100的酯. |
| C | ①密度是相同条件下氢气密度的30倍; ②能与NaHCO3溶液反应放出CO2气体 |
| D | ①能使溴的四氯化碳溶液褪色; ②能与水在一定条件下反应生成B; ③属于石油裂解气的成份之一. |
| E | ①2由C、H两种元素组成; ②分子球棍模型为: 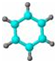 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数编号 | 盐酸溶液体积 V(mL) | 氢氧化钠溶液 体积V(mL) |
| 1 | 19.90 | 10.00 |
| 2 | 20.10 | 10.00 |
| 3 | 22.00 | 10.00 |
| 4 | 20.00 | 10.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO3的分解率为20% |
| B、10分钟内ν(SO2)=0.01mol/(L?min) |
| C、容器内气体的密度为40g/L |
| D、加压,容器内固体的质量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
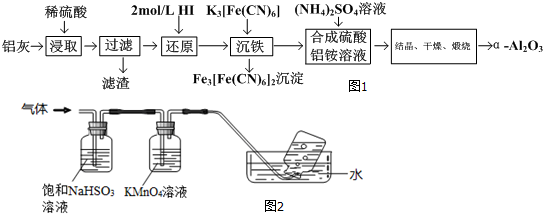
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com