
【题目】以丁烯二醛和肼为原料经过DielsAlder反应合成哒嗪,合成关系如图:
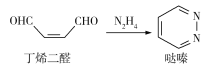
下列说法正确的是
A. 哒嗪与氢气加成后的产物分子式为C4H6N2
B. 聚丁烯二醛因无碳碳双键不能使溴水褪色
C. 丁烯二醛与N2H4可以在一定条件下加成后再消去可制得哒嗪
D. 物质的量相等的丁烯二醛和哒嗪分别与氢气完全加成,消耗氢气的量不同
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是
2SO3(g) △H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如下图所示投料,并在400℃条件下开始反应。达到平衡时,下列说法正确的是

A. 容器I、Ⅲ中平衡常数相同
B. 容器II、Ⅲ中正反应速率相同
C. SO3的体积分数:Ⅱ>III
D. 容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和大于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钾的冶炼可采用如下方法:2KF+CaC2![]() CaF2+2K↑+2C,下列有关说法合理的是( )
CaF2+2K↑+2C,下列有关说法合理的是( )
A.该反应的氧化剂是KF,氧化产物是K
B.该反应能说明C的还原性大于K
C.电解KF溶液不可能制备金属钾
D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C(s) + H2O(g) ![]() CO(g) +H2(g) △H=+131.3 kJ·mol-1。
CO(g) +H2(g) △H=+131.3 kJ·mol-1。
(1)该反应的平衡常数K随温度的升高而___________(选填“增大”“ 减小”或“不变”)
(2)上述反应达到平衡后,将体系中的C(s)部分移走,平衡____________(选填“向左移”“向右移”或“不移动”)。
(3)下列事实能说明该反应在一定条件下已达到平衡状态的有___________(填序号)。
A.单位体积内每消耗1 mol CO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
(4)某温度下,将4.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应,C(s)+ H2O(g) ![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为_____。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为_____。
(5)己知:① C(s)+H2O(l) =CO(g)+H2(g) △H1
② 2CO(g)+O2(g)=2CO2 (g) △H2
③ H2O (l)=H2 (g)+1/2 O2 (g) △H3
则C(s)+O2 (g)=CO2 (g)的△H=_____________________。
(6)若设计以一氧化碳为燃料的碱性燃料电池,则正极为通入_______(填化学式)的一极,其电极反应式是:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯加水,则灯泡会亮起来:
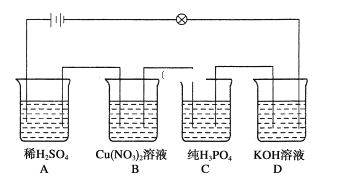
则:(1)加水的烧杯为__________。
(2)写出下列离子方程式:
硝酸铜溶液与氢氧化钾溶液混合_________,稀硫酸溶液与碳酸钠溶液混合_________
(3)若在A烧杯中加入Ba(OH)2溶液后,溶液的导电性________。(填“变强”“变弱”“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种化合物是很多表面涂层的重要成分,其结构如图所示,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,只有X、Y在同一周期,Y无最高正价,Z的含氧酸均具有氧化性,下列有关说法正确的是
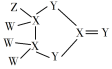
A. WZ沸点高于W2Y的沸点
B. 含Z的两种酸反应可制得Z的单质
C. W2Y2是由极性键和非极性键构成的非极性分子
D. X的含氧酸一定为二元弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用系统命法写出下列物质名称或结构简式
(1)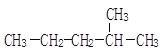 __________;
__________;
(2) ____________;
____________;
(3)![]() ___________;
___________;
(4)![]() ____________;
____________;
(5)2,6-二甲基-4-乙基辛烷_______;
(6)2-甲基-1-戊烯____________;
(7)3-甲基-1-丁炔:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。
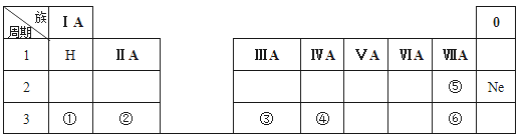
(1)元素④的符号是_______;②的最高价氧化物对应水化物的化学式为_______;⑤和⑥两种元素原子半径的大小关系:⑤_____⑥(填“>”或“<”);
(2)①和②两种元素金属性强弱关系:①_____②(填“>”或“<”);
(3)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2O为国际公认的高效安全灭菌消毒剂之一,实验室可利用氯气和空气(氯气与空气体积比为1:3,空气不参与反应)的混合气与含水8%的碳酸钠反应制备,并用水吸收Cl2O制备次氯酸溶液:
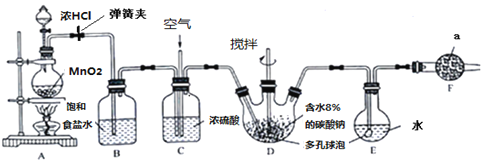
已知:Cl2O极易溶于水并与水反应生成次氯酸;Cl2O沸点为3.8℃,42℃以上分解为Cl2和O2。回答下列问题:
(1)检查装置A的气密性的方法是______;写出装置A中发生反应的离子方程式是:______。
(2)装置C的主要作用是______。
(3)装置D、E中都用到多孔球泡,其作用是______。
(4)写出装置D生成Cl2O的化学方程式:______。
(5)装置E中采用棕色圆底烧瓶是因为:______。
(6)仪器a的名称为______,所盛放的药品是______。
(7)制备Cl2O装置中存在缺陷,请提出改进措施:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com