
【题目】Cl2O为国际公认的高效安全灭菌消毒剂之一,实验室可利用氯气和空气(氯气与空气体积比为1:3,空气不参与反应)的混合气与含水8%的碳酸钠反应制备,并用水吸收Cl2O制备次氯酸溶液:
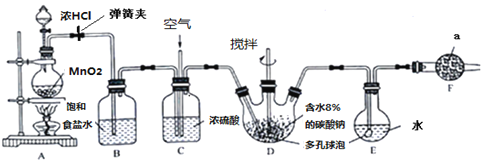
已知:Cl2O极易溶于水并与水反应生成次氯酸;Cl2O沸点为3.8℃,42℃以上分解为Cl2和O2。回答下列问题:
(1)检查装置A的气密性的方法是______;写出装置A中发生反应的离子方程式是:______。
(2)装置C的主要作用是______。
(3)装置D、E中都用到多孔球泡,其作用是______。
(4)写出装置D生成Cl2O的化学方程式:______。
(5)装置E中采用棕色圆底烧瓶是因为:______。
(6)仪器a的名称为______,所盛放的药品是______。
(7)制备Cl2O装置中存在缺陷,请提出改进措施:______。
【答案】关闭弹簧夹,向分液漏斗加水,当液面没过分液漏斗下端,再加水出现液面差,说明装置气密性良好 MnO2+4H++2Cl-![]() Mn2++Cl2↑+H2O 控制氯气与空气的体积比 增大反应物接触面积,使反应充分进行 2Cl2+2Na2CO3+H2O=2NaCl+Cl2O+2NaHCO3 次氯酸光照易分解 干燥管 碱石灰 将装置D放在冰水浴中,控制三颈烧瓶内的温度不超过42℃
Mn2++Cl2↑+H2O 控制氯气与空气的体积比 增大反应物接触面积,使反应充分进行 2Cl2+2Na2CO3+H2O=2NaCl+Cl2O+2NaHCO3 次氯酸光照易分解 干燥管 碱石灰 将装置D放在冰水浴中,控制三颈烧瓶内的温度不超过42℃
【解析】
根据实验原理及装置分析装置的作用及反应的离子方程式;根据装置特点分析装置的缺陷并提出改进措施。
(1)根据装置特点,采用的气密性检查方法为:关闭弹簧夹,向分液漏斗加水,当液面没过分液漏斗下端,再加水出现液面差,说明装置气密性良好;装置A为用二氧化锰与浓盐酸反应制备氯气的反应,离子方程式为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+H2O,故答案为:关闭弹簧夹,向分液漏斗加水,当液面没过分液漏斗下端,再加水出现液面差,说明装置气密性良好;MnO2+4H++2Cl-
Mn2++Cl2↑+H2O,故答案为:关闭弹簧夹,向分液漏斗加水,当液面没过分液漏斗下端,再加水出现液面差,说明装置气密性良好;MnO2+4H++2Cl-![]() Mn2++Cl2↑+H2O;
Mn2++Cl2↑+H2O;
(2)C中盛有浓硫酸便于空气和氯气混合均匀,同时控制氯气和空气的体积比,有利于氯气的反应,故答案为:控制氯气和空气的体积比;
(3)装置D、E中都用到多孔球泡,能增大反应物的接触面积,使反应充分进行,故答案为:增大接触面积,使反应充分进行;
(4)氯气与空气体积比为1:3的混合气体与含水8%的碳酸钠在装置D中发生氧化还原反应生成Cl2O,反应的方程式为:2Cl2+2Na2CO3+H2O=2NaCl+Cl2O+2NaHCO3,答案为:2Cl2+2Na2CO3+H2O=2NaCl+Cl2O+2NaHCO3;
(5)装置E中制取次氯酸,次氯酸光照易分解,所以采用棕色圆底烧瓶,故答案为:次氯酸光照易分解;
(6)仪器a的名称为球形干燥管,盛有碱石灰吸收尾气,防止污染空气,故答案为:球形干燥管;碱石灰;
(7)Cl2O在4242℃以上,分解为Cl2和O2,因此装置D中的温度不能过高,所以将装置D放在冰水浴中,以控制三颈烧瓶内的温度不超过42℃,故答案为:将装置D放在冰水浴中,控制三颈烧瓶内的温度不超过42℃。


科目:高中化学 来源: 题型:
【题目】以丁烯二醛和肼为原料经过DielsAlder反应合成哒嗪,合成关系如图:
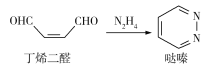
下列说法正确的是
A. 哒嗪与氢气加成后的产物分子式为C4H6N2
B. 聚丁烯二醛因无碳碳双键不能使溴水褪色
C. 丁烯二醛与N2H4可以在一定条件下加成后再消去可制得哒嗪
D. 物质的量相等的丁烯二醛和哒嗪分别与氢气完全加成,消耗氢气的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.标况下,11.2 L甲烷(CH4)和乙烯(C2H4)的混合气体中含氢原子的物质的量为2 mol
B.标况下,0.1 mol CCl4所占的体积为2.24 L
C.等质量的N2和CO含有的分子数均约为6.02×1023个
D.常温常压下,1 mol任何气体所占的体积均为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七铝十二钙(12CaO7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
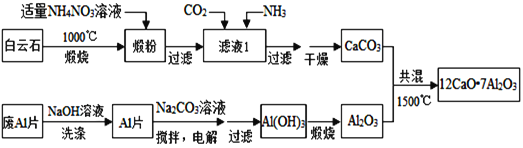
(1)锻粉主要含______和______,用适量NH4NO3溶液浸取煅粉后,镁化合物几乎不溶。该工艺中不能用(NH4)2SO4代替NH4NO3,原因是_______________________________________________.
(2)滤液Ⅰ中阴离子有______(忽略杂质成分的影响);若滤液Ⅰ中仅通入CO2,会生成______,从而导致CaCO3产率降低.
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为______________________.
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,则铝片接外电源的____极,电解时阴极发生的反应为:______.
(5)一种可超快充电的新型铝电池,充放电时AlCl4﹣和Al2Cl7﹣两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为______________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据所给条件推出的结论不正确的是( )
选项 | 条件 | 结论 |
A | 在水溶液或熔融状态下可以导电的化合物,称为电解质 | 水中存在: |
B | 凡是能给出质子的分子或离子称为酸,凡是能接受质子的分子或离子称为碱 |
|
C | 联氨为二元弱碱,在水中的电离方式与氨相似 | 联氨与硫酸形成的酸式盐的化学式为: |
D | 发生化学反应时,接受电子对的物质为酸,提供电子对的物质为碱 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是氢氧燃料电池的示意图,按图中提示,下列叙述不正确的是( )

A. a电极是负极,b电极是正极
B. a电极的电极反应式为H2-2e-===2H+
C. b电极的电极反应式为4OH--4e-===2H2O+O2↑
D. 氢氧燃料电池不需要将还原剂和氧化剂全部储藏在电池内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊二烯(![]() )可用于制备二茂铁(
)可用于制备二茂铁(![]() ,结构简式为
,结构简式为![]() ),后者广泛用于航天、化工等领域。二茂铁的电化学制备原理如图所示,下列说法正确的是( )
),后者广泛用于航天、化工等领域。二茂铁的电化学制备原理如图所示,下列说法正确的是( )
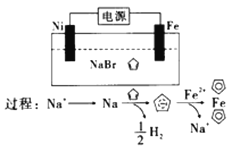
A. ![]() 为电解池的阳极
为电解池的阳极
B. 电解质溶液可以是![]() 的水溶液
的水溶液
C. 电解池的总反应方程式为:![]()
D. 电解质溶液中,当有![]() 的
的![]() 向
向![]() 电极移动时,同时在
电极移动时,同时在![]() 电极上产生了
电极上产生了![]() 的氢气
的氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某有机物A的结构,做如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1∶2∶3。试回答下列问题:
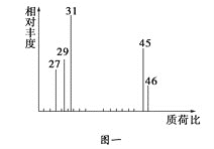
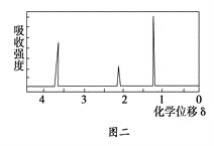
(1)有机物A的相对分子质量是________。
(2)有机物A的实验式是________。
(3)A的分子式是_______________________________________。
(4)A的结构简式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1
C. -330kJ·mol-1 D. +330kJ·mlo-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com