
【题目】七铝十二钙(12CaO7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
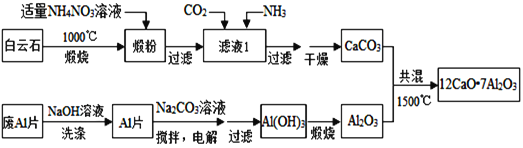
(1)锻粉主要含______和______,用适量NH4NO3溶液浸取煅粉后,镁化合物几乎不溶。该工艺中不能用(NH4)2SO4代替NH4NO3,原因是_______________________________________________.
(2)滤液Ⅰ中阴离子有______(忽略杂质成分的影响);若滤液Ⅰ中仅通入CO2,会生成______,从而导致CaCO3产率降低.
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为______________________.
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,则铝片接外电源的____极,电解时阴极发生的反应为:______.
(5)一种可超快充电的新型铝电池,充放电时AlCl4﹣和Al2Cl7﹣两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为______________________________________.
【答案】MgO CaO CaSO4微溶于水,用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀引起Ca2+的损失; NO3-,OH- Ca(HCO3)2 Al2O3 +2 OH-= 2 AlO2-+ H2O; 正 2H2O + 2e- = 2OH- + H2 ; Al - 3 e- + 7 AlCl4- =4 Al2Cl7-;
【解析】
(1)白云石煅烧发生反应:CaCO3 = CaO + CO2↑,MgCO3 = MgO+CO2↑,用(NH4)2SO4代替NH4NO3,生成CaSO4,微溶于水,造成Ca的损失,从而导致CaCO3产率降低;
(2)在锻粉中加入适量的NH4NO3溶液后,镁化合物几乎不溶,由于NH4NO3溶液水解显酸性,与CaO反应生成Ca(NO3)2和NH3H2O,故过滤后溶液中含Ca(NO3)2和NH3H2O,将CO2和NH3通入滤液I中后发生反应:
Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,据此分析滤液中的阴离子;若滤液Ⅰ中仅通入CO2,会造成CO2过量,据此分析产物;
(3)NaOH溶液可以与Al2O3反应偏铝酸钠和水,可用NaOH溶液可除去废Al片表面的氧化膜;
(4)用Al片和石墨作电极来制备Al(OH)3,故Al做阳极,石墨做阴极,阴极为水中氢离子放电;
(5)放电时负极电极本身Al放电,失电子,根据AlCl4-和Al2Cl7-中铝元素和氯元素的比例来确定做AlCl4-做反应物而生成Al2Cl7-。
(1)白云石煅烧发生反应:CaCO3 = CaO + CO2↑,MgCO3 = MgO + CO2↑,故所得煅粉主要含有CaO和MgO,用(NH4)2SO4代替NH4NO3,生成CaSO4,微溶于水,造成Ca的损失;
故答案为:CaO、MgO; CaSO4微溶于水,用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀引起Ca2+的损失;
(2)在锻粉中加入适量的NH4NO3溶液后,镁化合物几乎不溶,由于NH4NO3溶液水解显酸性,与CaO反应生成Ca(NO3)2和NH3H2O,故过滤后溶液中含Ca(NO3)2和NH3H2O,将CO2和NH3通入滤液I中后发生反应:
Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,故滤液Ⅰ中阴离子有NO3-,OH-;若滤液Ⅰ中仅通入CO2,会造成CO2过量,会生成Ca(HCO3)2,从而导致CaCO3产率降低;
故答案为:NO3-,OH-;Ca(HCO3)2;
(3)NaOH溶液可以与Al2O3反应偏铝酸钠和水,可用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为:Al2O3 +2 OH-= 2 AlO2 - + H2O;
故答案为:Al2O3 +2 OH-= 2 AlO2 - + H2O;
(4)用Al片和石墨作电极来制备Al(OH)3,故Al做阳极,石墨做阴极,则铝片接外电源的正极,阴极为水中氢离子放电,电极反应式为:2H2O + 2e- = 2OH- + H2 ;
故答案为:正;2H2O + 2e- = 2OH- + H2 ;
(5)放电时负极电极本身Al放电,失电子,由于AlCl4-中氯元素的含量高于Al2Cl7-中氯元素的含量,故AlCl4-做反应物,而Al2Cl7-为生成物,由于其它离子不参与电极反应,故电极反应式为:Al - 3 e- + 7 AlCl4- =4 Al2Cl7-;


科目:高中化学 来源: 题型:
【题目】水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C(s) + H2O(g) ![]() CO(g) +H2(g) △H=+131.3 kJ·mol-1。
CO(g) +H2(g) △H=+131.3 kJ·mol-1。
(1)该反应的平衡常数K随温度的升高而___________(选填“增大”“ 减小”或“不变”)
(2)上述反应达到平衡后,将体系中的C(s)部分移走,平衡____________(选填“向左移”“向右移”或“不移动”)。
(3)下列事实能说明该反应在一定条件下已达到平衡状态的有___________(填序号)。
A.单位体积内每消耗1 mol CO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
(4)某温度下,将4.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应,C(s)+ H2O(g) ![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为_____。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为_____。
(5)己知:① C(s)+H2O(l) =CO(g)+H2(g) △H1
② 2CO(g)+O2(g)=2CO2 (g) △H2
③ H2O (l)=H2 (g)+1/2 O2 (g) △H3
则C(s)+O2 (g)=CO2 (g)的△H=_____________________。
(6)若设计以一氧化碳为燃料的碱性燃料电池,则正极为通入_______(填化学式)的一极,其电极反应式是:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。
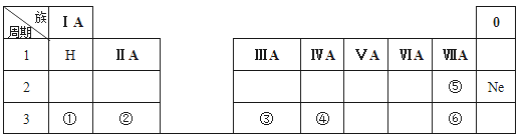
(1)元素④的符号是_______;②的最高价氧化物对应水化物的化学式为_______;⑤和⑥两种元素原子半径的大小关系:⑤_____⑥(填“>”或“<”);
(2)①和②两种元素金属性强弱关系:①_____②(填“>”或“<”);
(3)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设一个12C原子的质量为a g,一个16O原子的质量为b g,阿伏加德罗常数为NA,则12C16O2的相对分子质量与以下哪些数值相同
①a+2b ②(a+2b)NA ③![]() ④
④![]()
A.①③B.②③C.①④D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的氨氮废水中主要含有![]() ,可用电化学氧化法加以处理。
,可用电化学氧化法加以处理。
(1)图1是电化学氧化法的原理示意图。a的电极反应式是_____________。
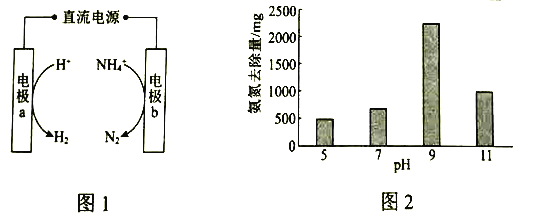
(2)研究显示,其他条件不变时,不同![]() 下氨氮的去除量如图2所示。已知:
下氨氮的去除量如图2所示。已知:![]() 与
与![]() 相比,在电极表面的吸附效果更好。结合平衡移动原理和图中数据,解释
相比,在电极表面的吸附效果更好。结合平衡移动原理和图中数据,解释![]() 从5到9时氨氮去除量增大的原因:______________。
从5到9时氨氮去除量增大的原因:______________。
(3)在电解废水的过程中,![]() 会经历“
会经历“![]() ”的过程。其他条件相同、
”的过程。其他条件相同、![]() 的浓度不同时,废水中氨氮脱除效率的实验结果如下:
的浓度不同时,废水中氨氮脱除效率的实验结果如下:
| 400 | 100 |
电解时间/h | 0.5 | 0.5 |
氨氮脱除效率/( | 2.40.8 |
①其它条件相同、适当提高![]() 的浓度,可以显著增大废水中
的浓度,可以显著增大废水中![]() 的脱除效率。
的脱除效率。
用化学用语解释原因:____________、![]() 。
。
②图2中,![]() 时,废水中
时,废水中![]() 去除量下降,可能的原因是:_______________。
去除量下降,可能的原因是:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案正确且能达到实验目的的是( )
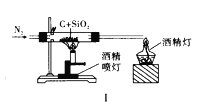
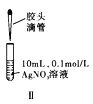
A. 图Ⅰ比较碳、硅两元素非金属性的强弱
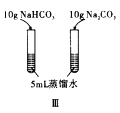
B. 图Ⅱ先滴加5滴![]() 的
的![]() 溶液,再滴加5滴
溶液,再滴加5滴![]() 的
的![]() 溶液。比较
溶液。比较![]() 与
与![]() 溶解度的大小
溶解度的大小
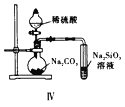
C. 图Ⅲ已知溶解度(20℃)![]() :
:![]() ;
;![]() :
:![]() 。室温下,比较
。室温下,比较![]() 和
和![]() 溶解度的大小
溶解度的大小
D. 图Ⅳ证明碳酸的酸性比硅酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2O为国际公认的高效安全灭菌消毒剂之一,实验室可利用氯气和空气(氯气与空气体积比为1:3,空气不参与反应)的混合气与含水8%的碳酸钠反应制备,并用水吸收Cl2O制备次氯酸溶液:
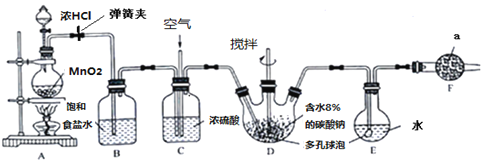
已知:Cl2O极易溶于水并与水反应生成次氯酸;Cl2O沸点为3.8℃,42℃以上分解为Cl2和O2。回答下列问题:
(1)检查装置A的气密性的方法是______;写出装置A中发生反应的离子方程式是:______。
(2)装置C的主要作用是______。
(3)装置D、E中都用到多孔球泡,其作用是______。
(4)写出装置D生成Cl2O的化学方程式:______。
(5)装置E中采用棕色圆底烧瓶是因为:______。
(6)仪器a的名称为______,所盛放的药品是______。
(7)制备Cl2O装置中存在缺陷,请提出改进措施:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
C.向氯水中加入Na2CO3粉末,有气泡产生,说明氯水中含有H+
D.氯水的性质很稳定,保存在无色试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的化学用语表达正确的是( )
A. 乙烯的结构简式:CH2CH2 B. 羟基的电子式:![]()
C. 甲醇的球棍模型:![]() D. 乙酸的实验式:CH3COOH
D. 乙酸的实验式:CH3COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com