
【题目】常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害,某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源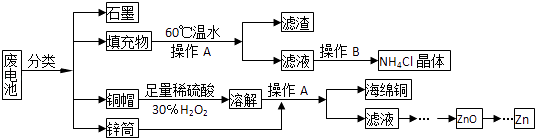
(1)填充物用60℃温水溶解,目的是 .
(2)操作A的名称为 .
(3)铜帽溶解时加入H2O2的目的是(用化学方程式表示).铜帽溶解完全后,可采用方法除去溶液中过量的H2O2 .
(4)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2 , 其负极的电极反应式为 .
(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.①当1molMnO2参加反应时,整个反应共有mol电子发生转移.
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出该反应的化学方程式: .
【答案】
(1)加快溶解速率
(2)过滤
(3)Cu+H2O2+H2SO4=CuSO4+2H2O;加热
(4)Zn+2OH﹣﹣2e﹣=Zn(OH)2
(5)4;2MnO(OH)+6HCl(浓) ![]() 2MnCl2+Cl2↑+4H2O
2MnCl2+Cl2↑+4H2O
【解析】解:废旧干电池含有铜、石墨、二氧化锰以及填充物等,填充物用60℃充分溶解,过滤,滤液中含有氯化铵,蒸发、浓缩、结晶可得到氯化铵晶体;铜与稀硫酸在过氧化氢作用发生氧化还原反应生成硫酸铜,加入锌可置换出铜,过滤分离,硫酸锌溶液最终可生成氢氧化锌、氧化锌,冶炼可得到锌,(1)加热适当温度,可促进溶解,所以答案是:加快溶解速率;(2)分离不溶性固体和溶液采用过滤的方法,所以该操作名称是过滤,所以答案是:过滤;(3)酸性条件下,双氧水能将铜氧化生成铜离子反应的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O;加热条件下,双氧水易分解生成水和氧气,所以除去双氧水的方法是加热,所以答案是:Cu+H2O2+H2SO4=CuSO4+2H2O;加热;(4)负极发生氧化反应,由方程式可知Zn被氧化生成Zn(OH)2 , 则电极方程式为Zn+2OH﹣﹣2e﹣=Zn(OH)2 , 所以答案是:Zn+2OH﹣﹣2e﹣=Zn(OH)2;(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.其主要反应为2 MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.①该反应中,氧化剂是MnO(OH)、MnO2 , 还原剂是草酸,当1mol MnO2参加反应时,转移电子的物质的量= ![]() ×2×2×(4﹣3)=4mol,所以答案是:4;②MnO(OH)与浓盐酸在加热条件下也可发生反应生成氯化锰、氯气和水,反应方程式为:2MnO(OH)+6HCl(浓)
×2×2×(4﹣3)=4mol,所以答案是:4;②MnO(OH)与浓盐酸在加热条件下也可发生反应生成氯化锰、氯气和水,反应方程式为:2MnO(OH)+6HCl(浓) ![]() 2MnCl2+Cl2↑+4H2O, 所以答案是:2MnO(OH)+6HCl(浓)
2MnCl2+Cl2↑+4H2O, 所以答案是:2MnO(OH)+6HCl(浓) ![]() 2MnCl2+Cl2↑+4H2O.
2MnCl2+Cl2↑+4H2O.


科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的叙述错误的是
A.甲烷和乙烯可以用溴水鉴别
B.煤油是石油的分馏产品,可用于保存少量的钠
C.棉花、蛋白质和油脂都是高分子化合物,水解产物均为电解质
D.用饱和碳酸钠溶液可除去乙酸乙酯中混有的乙酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法正确的是( )
A. 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
B. 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
C. 除短周期外,其它周期均为18种元素
D. 周期表中所有元素都是从自然界中发现的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B、C、D、E、F在常温下均为气体,它们有以下转化关系(部分反应条件、产物已略去).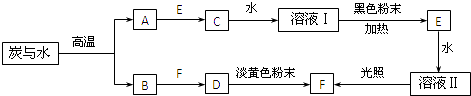
请回答下列问题:
(1)将A点燃后伸入到装有E的集气瓶中,可观察到的现象是 .
(2)C的浓溶液与黑色粉末反应生成E的化学方程式为 .
(3)若将溶液Ⅱ滴入到碘化钾溶液中,发生反应的离子方程式为 , 向反应后的溶液中加入适量CCl4 , 充分振荡后静置,可以观察到的现象是 .
(4)与溶液Ⅰ比较,溶液Ⅱ中多出的物质是(填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验编号 | HA物质的量 浓度(mol·L-1) | NaOH物质的量 浓度(mol·L-1) | 混合溶 液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
请根据要求回答:
(1)②组情况表明,c________ (选填“大于”、“小于”或“等于”)0.2。混合液中离子浓度c(A-)与c(Na+)的大小关系是______________________________________。
(2)从③组实验结果分析,说明HA的电离程度________(选填“大于”、“小于”或“等于”)NaA的水解程度,该混合溶液中离子浓度由大到小的顺序是_____________________________。
(3)①组实验所得混合溶液中由水电离出的c(OH-)=____________mol·L-1。写出该混合溶液中下列算式的结果(不能作近似计算)。c(Na+)-c(A-)=________mol·L-1; c(OH-)-c(HA)=________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于弱电解质的说法中正确的是( )
A. 弱电解质需要通电才能发生电离
B. 醋酸溶液达到电离平衡时,不存在CH3COO-+H+![]() CH3COOH
CH3COOH
C. H2SO4是共价化合物,所以它是弱电解质;NaOH是离子化合物,所以它是强电解质
D. 弱电解质溶液中,既有溶质分子,又有溶质电离出来的离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mL
B.45mL
C.30mL
D.15mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、稀硝酸、澄清石灰水、氯化铜溶液是中学化学中的常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A,B,C,D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( ) 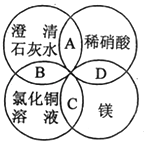
A.OH﹣+HNO3═H2O+NO ![]()
B.Ca(OH)2+Cu2+═Ca2++Cu(OH)2
C.Mg+Cu2+═Cu+Mg2+
D.Mg+2H+=Mg2++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列有关叙述不正确的是( )
A.在熔融状态下,1 mol Na2O2 完全电离出的离子数目为3 NA
B.将CO2通过Na2O2使固体质量增加mg,反应中转移的电子数 ![]()
C.在标准状况下,22.4LCH4与18 gH2O所含有的电子数均为10NA
D.含1mol Cl﹣的NH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液中NH![]() 数为 NA
数为 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com