
����Ŀ��������Ҫ�İ뵼����ϣ��ǹ����ִ����ӹ�ҵ�Ļ������輰�仯�����ڹ�ҵ��Ӧ�ù㷺���ڹ�ҵ�ϣ��ߴ������ͨ������������ȡ��
![]()
����������:
��1����ԭ�Ӻ�����_______�ֲ�ͬ�����ĵ��ӣ���ԭ�ӵĺ�������Ų�ʽ��_______________��
��2��̼�������ͬ����Ԫ�أ��۷е�SiO2 ________CO2 (��д��>������<����=��)����ԭ����_____________________________________________________��
��3����������SiO2�ƴֹ�ķ�Ӧ����˵��̼�ķǽ�����ǿ�ڹ裬ԭ����_________________����д��һ����˵��̼�ķǽ�����ǿ�ڹ�Ļ�ѧ����ʽ______________________________��
��4��SiHCl3(g) + H2(g)![]() Si(s) + 3HCl(g) ��Q ��Q>0��
Si(s) + 3HCl(g) ��Q ��Q>0��
��������Ӧ��ƽ�ⳣ������ʽK��_____________����ʹK����Ĵ�ʩ��_______________��
��һ�������£��ڹ̶��ݻ����ܱ������У��ܱ�ʾ������Ӧ�ﵽƽ��״̬����________��ѡ���ţ���
a��3v��(SiHCl3)��v��(HCl) b����������ѹǿ����
c��K���ֲ��� d��c(SiHCl3)��c(H2)��c(HCl)��1��1��3
��һ���¶��£���2L�ܱ������н���������Ӧ��5min��ﵽƽ�⣬�˹����й�����������0.28g����ʱHCl�Ļ�ѧ��Ӧ����Ϊ ________________ ��
���𰸡�5 1s22s22p63s23p2 > SiO2��ԭ�Ӿ��壬�ڻ�ʱ��Ҫ�˷����ۼ���CO2�Ƿ��Ӿ��壬�ڻ�ʱֻ��Ҫ�˷����Ӽ�������������SiO2���۷е��CO2���۷е�ߡ� �ǽ�������ָ�ǽ���Ԫ�صĵ����ڻ�ѧ��Ӧ�еõ����ӵ���������̼��������跴Ӧ�����ֳ�������̼ʧȥ���ӵ���������ԭ�ԣ�����˲���˵��̼�ķǽ����Աȹ�ǿ Na2SiO3+2CO2+2H2O ��2NaHCO3+H4SiO4����CO2+Na2SiO3+H2O ��H2SiO3��+Na2CO3 K=c(HCl)3/ c (SiHCl3) c (H2) ���� a b 0.003 mol/(L��min)
��������
��1��ԭ�Ӻ�������м����ܼ����м���������ͬ�Ĺ����Siԭ������Ϊ14����3�����Ӳ㣬����������Ϊ4��
��2���۵�һ��Ϊԭ�Ӿ��壾���Ӿ��壾�������壾���Ӿ��壻
��3��̼��������跴Ӧ���ɹ赥�ʺ�һ����̼��ֻ��˵��̼�Ļ�ԭ�Աȹ�ǿ��ǿ�ᷴӦ��ȡ���
��4������ƽ�ⳣ������д������������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ�ȵ��ݴη��˻��õ���ƽ�ⳣ�����¶ȱ仯��
��5���ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�ٷֺ������䣬�Լ��ɴ�����������һЩ�����䣬�ݴ˷�����
��6�����ݷ���ʽ�����������������0.28gʱ���ɵ��Ȼ�������ʵ���������![]() ���㡣
���㡣
����1����ԭ�Ӻ�����1s��2s��2p��3s��3p�����ܼ���������ԭ�Ӻ�����5�ֲ�ͬ�����Ĺ����Siԭ������Ϊ14����3�����Ӳ㣬����������Ϊ4���ʹ�ԭ�ӵĺ�������Ų�ʽ��1s22s22p63s23p2��
�ʴ�Ϊ��5��1s22s22p63s23p2��
��2���۵�һ��Ϊԭ�Ӿ��壾���Ӿ��壾�������壾���Ӿ��壬SiO2Ϊԭ�Ӿ��壬�ڻ�ʱ��Ҫ�˷����ۼ���CO2Ϊ���Ӿ��壬�ڻ�ʱֻ��Ҫ�˷����Ӽ������������۷е㣺SiO2��CO2��
�ʴ�Ϊ������SiO2��ԭ�Ӿ��壬�ڻ�ʱ��Ҫ�˷����ۼ���CO2�Ƿ��Ӿ��壬�ڻ�ʱֻ��Ҫ�˷����Ӽ�������������SiO2���۷е��CO2���۷е�ߣ�
��3��̼��������跴Ӧ���ɹ赥�ʺ�һ����̼��![]() ��ֻ��˵��̼�Ļ�ԭ�Աȹ�ǿ���ǽ�������ָ�ǽ���Ԫ�صĵ����ڻ�ѧ��Ӧ�еõ����ӵ���������̼��������跴Ӧ�����ֳ�������̼ʧȥ���ӵ���������ԭ�ԣ�����˲���˵��̼�ķǽ����Աȹ�ǿ��̼�ķǽ����Աȹ�ǿ����̼������Ա�ԭ���ᣨ���ᣩǿ���ɷ�����Na2SiO3+2CO2+2H2O=2NaHCO3+H4SiO4����CO2+Na2SiO3+H2O=H2SiO3��+Na2CO3��
��ֻ��˵��̼�Ļ�ԭ�Աȹ�ǿ���ǽ�������ָ�ǽ���Ԫ�صĵ����ڻ�ѧ��Ӧ�еõ����ӵ���������̼��������跴Ӧ�����ֳ�������̼ʧȥ���ӵ���������ԭ�ԣ�����˲���˵��̼�ķǽ����Աȹ�ǿ��̼�ķǽ����Աȹ�ǿ����̼������Ա�ԭ���ᣨ���ᣩǿ���ɷ�����Na2SiO3+2CO2+2H2O=2NaHCO3+H4SiO4����CO2+Na2SiO3+H2O=H2SiO3��+Na2CO3��
�ʴ�Ϊ���ǽ�������ָ�ǽ���Ԫ�صĵ����ڻ�ѧ��Ӧ�еõ����ӵ���������̼��������跴Ӧ�����ֳ�������̼ʧȥ���ӵ���������ԭ�ԣ�����˲���˵��̼�ķǽ����Աȹ�ǿ��Na2SiO3+2CO2+2H2O=2NaHCO3+H4SiO4����CO2+Na2SiO3+H2O=H2SiO3��+Na2CO3��
��4��![]() -Q��Q��0��������ƽ�ⳣ��������д��ע�����ʹ�Һ�岻д�����ʽ������ʽΪK=c(HCl)3/ c (SiHCl3) c (H2)���÷�Ӧ����ӦΪ���ȷ�Ӧ�����������¶�ƽ�����ƶ���ƽ�ⳣ������
-Q��Q��0��������ƽ�ⳣ��������д��ע�����ʹ�Һ�岻д�����ʽ������ʽΪK=c(HCl)3/ c (SiHCl3) c (H2)���÷�Ӧ����ӦΪ���ȷ�Ӧ�����������¶�ƽ�����ƶ���ƽ�ⳣ������
�ʴ�Ϊ��K=c(HCl)3/ c (SiHCl3) c (H2)�����£�
��5��a��3v����SiHCl3��=v����HCl�������淴Ӧ������ȣ���a��ȷ��
b���淴Ӧ����������ѹǿ����������ѹǿ���䣬˵������ƽ�⣬��b��ȷ��
c��ƽ�ⳣ�����¶ȱ仯���¶Ȳ���K���ֲ��䣬����˵�����淴Ӧ������ȣ���c����
d��c��SiHCl3����c��H2����c��HCl��=1��1��3����˵�����淴Ӧ������ȣ���d����
�ʴ�Ϊ��ab��
��6��![]() ���˹����й�����������0.28g�������Ȼ�������ʵ���Ϊ0.03mol��
���˹����й�����������0.28g�������Ȼ�������ʵ���Ϊ0.03mol��![]() =0.003mol/��Lmin����
=0.003mol/��Lmin����
�ʴ�Ϊ��0.003mol/��Lmin����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
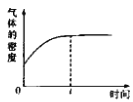
����Ŀ������ͼ��ʾ��ͼ���Ǻ�ѹ�ܱ�������ͼ���Ǻ����ܱ�������������������ͬʱ�����������зֱ����2mol![]() ��2mol
��2mol![]() ����ʼʱ�����������ΪVL���������·�Ӧ���ﵽƽ��״̬
����ʼʱ�����������ΪVL���������·�Ӧ���ﵽƽ��״̬![]() ��ʾ������X��Y��״̬��δ֪������Z��״̬Ϊ��̬)��2X(?)+Y(?)
��ʾ������X��Y��״̬��δ֪������Z��״̬Ϊ��̬)��2X(?)+Y(?)![]() aZ(g)��ʱ����X��Y��Z�����ʵ���֮��Ϊ1:3:2�������ж���ȷ����
aZ(g)��ʱ����X��Y��Z�����ʵ���֮��Ϊ1:3:2�������ж���ȷ����![]()
![]()
�� ��
�� ��
��
A.����Z�Ļ�ѧ������ a= 2
B.��X��Y��Ϊ��̬������ƽ��ʱX��ת���ʣ���<��
C.������������ܶ���ͼ����ʾ����X��Y��ֻ��һ��Ϊ��̬
D.��XΪ��̬��YΪ��̬�����������дӿ�ʼ��ƽ�������ʱ�䣺��>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z��ԭ�������������ӡ�m��p��r������ЩԪ����ɵĶ�Ԫ�����q��Ԫ��Y�ĵ�����Ϊ����ɫ���壬n��Ԫ��Z�ĵ��ʣ�0.01mol��L-1r��Һ��pHΪ2��sͨ����������ˮ�Ļ����������ʵ�ת����ϵ��ͼ��ʾ������˵��һ����ȷ����
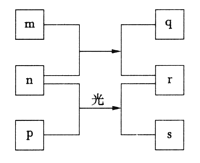
A.Ԫ�صķǽ����ԣ�Z>Y
B.ԭ�Ӱ뾶�Ĵ�С��Z>Y>X>W
C.���⻯����ȶ��ԣ�Z>Y>X
D.������Ķ�Ӧˮ��������ԣ�Z>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ8NH3��3Cl2��N2��6NH4Cl�������������ȷ����
A.N2�ĵ���ʽ�� ![]()
B.��Ӧ���������Ļ�ѧ��������ͬ
C.ÿ����11.2 L N2��ת�Ƶ�����Ϊ3 NA
D.��ԭ���뻹ԭ��������ʵ���֮����1��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ļ������ڹ�ũҵ�����������о�����ҪӦ�á���ش��������⣺
(1)���������г���N2H4��Ϊ����������ȼ����N2H4�백�����ƣ���һ�ּ������壬������ˮ����������N2H4��H2O���õ��뷽��ʽ��ʾN2H4��H2O�Լ��Ե�ԭ���ǣ�____________________________________________��
(2)�ں��������£�1 mol NO2������C������Ӧ2NO2(g)+2C(s)![]() N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
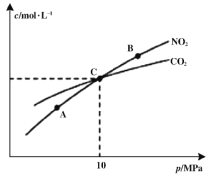
��A��B�����Ũ��ƽ�ⳣ����ϵ��Kc(A) ___________Kc(B)(�<����>����=��)
��A��B��C������NO2��ת������ߵ���___________(�A����B����C��)�㡣
������C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp=___________MPa(Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
(3)��֪��������(HNO2)���ʺ��������ƣ�������һ�����ᡣ������������ĵ���ƽ�ⳣ��Ka=5.1��10��4��H2CO3��Ka1=4.2��10��7��Ka2=5.61��10��11���ڳ���������2mol̼���Ƶ���Һ�м���1mol��HNO2������Һ��CO32����HCO3����NO2��������Ũ���ɴ�С��˳����______________________��
(4)��֪�������¼װ�(CH3NH2)�ĵ��볣��ΪKb����pKb=��lgKb=3.4ˮ��Һ����CH3NH2+H2OCH3NH3++OH������������CH3NH2��Һ�μ�ϡ������c(CH3NH2)=c(CH3NH3+)ʱ������ҺpH=_______��
(5)һ��ú̿������������Ԫ����CaSO4���γɹ̶���������������CO�ֻ���CaSO4������ѧ��Ӧ����ص��Ȼ�ѧ����ʽ���£�
��CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) ��H=+210.5kJ�� mol��1
��CaSO4(s)+4CO(g) CaS(s)+ 4CO2(g) ��H=��189.2 kJ�� mol��1
��ӦCaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) ��H=___________ kJ�� mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����̶���������CO2����Ч�ؼ���������ЧӦ����
I����ҵ�������о�����CO2�������״�ȼ�ϵķ������÷����Ļ�ѧ����ʽ�ǣ�CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ��H=-49.0kJmol��1��ij��ѧʵ�齫6molCO2��8 molH2����һ�ݻ�Ϊ2L���ܱ�������(�¶ȱ��ֲ���)�����H2�����ʵ�����ʱ��仯����ͼ��ʵ����ʾ��ͼ����ĸ������ֱ�ʾ��Ӧ�����꣩��
CH3OH(g)+H2O(g) ��H=-49.0kJmol��1��ij��ѧʵ�齫6molCO2��8 molH2����һ�ݻ�Ϊ2L���ܱ�������(�¶ȱ��ֲ���)�����H2�����ʵ�����ʱ��仯����ͼ��ʵ����ʾ��ͼ����ĸ������ֱ�ʾ��Ӧ�����꣩��
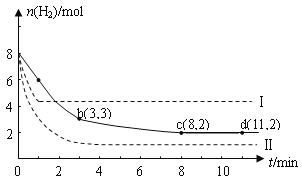
�ش��������⣺
��1������˵������ȷ������__________��
A��0��1min��ƽ����Ӧ���ʴ���3��4min��ƽ����Ӧ����
B���ﵽƽ��ʱH2��ת����Ϊ75%
C�� ��������������ʱ������߷�Ӧ���¶�����Ӧ���������淴Ӧ���ʼ�С
��2���÷�Ӧ��0 ��8 min��CO2��ƽ����Ӧ������_______��
��3���÷�Ӧ��ƽ�ֳ���K=______________��
��4�����ı�ijһ�����ٽ���ʵ�飬���H2�����ʵ�����ʱ��仯��ͼ��������ʾ����ʵ����ȣ�����I�ı������������_________����ʵ�߶�Ӧ������ƽ�ⳣ��ΪK������I��Ӧ������ƽ�ⳣ��ΪK1������II��Ӧ������ƽ�ⳣ��ΪK2����K��K1��K2�Ĵ�С��ϵ��____��
II����֪25��ʱ�������̼��ĵ���ƽ�ⳣ�����±���
���ʵĻ�ѧʽ | CH3COOH | H2CO3 | |
����ƽ�ⳣ�� | K=1.8��10��5 | K1=4.3��10��7 | K2=5.6��10��11 |
��1���ñ��Ͱ�ˮ����CO2�ɵõ�NH4HCO3��Һ������֪CH3COONH4��ҺpH=7����(NH4)2CO3��Һ��_____(������������������������������)��
��2��25��ʱ����0��lmolL��1������Һ�м���һ������NaHCO3�������¶Ȳ��䣬���û��Һ��pH=6����ô���Һ��![]() =_______���û����Һ�е�����Ũ���ɴ�С��˳��Ϊ��________________��
=_______���û����Һ�е�����Ũ���ɴ�С��˳��Ϊ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���ӦN2+3H22NH3����2L�ܱ������н��У�5min�ڰ�������������1.7g����Ӧ����Ϊ�� ��
A.v(H2)=0.03mol/��L��min��
B.v(N2)=0.02mol/(L��min)
C.v(NH3)=0.17mol/(L��min )
D.v(NH3)=0.01mol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���Ӿ��徧������ͼ��ʾ����Ħ������ΪM�������ӵ�����ΪNA��������ܶ�Ϊd g/cm3������˵������ȷ����

A. ���徧�������������ӵĸ�����Ϊ1
B. �þ������������������ͬ�����ӵĺ˼��Ϊ![]() cm
cm
C. �������������ӵ���λ������4
D. �þ���������NaCl�ľ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. ��Ȼ����ˮú����Һ��ʯ�������������г��õ�ȼ�ϣ����ǵ���Ҫ�ɷֶ��ǻ�����
B. ���й������������ۿ����Ǹ�����ɵ�Ȧ�������ڽ�������
C. �Ʋ�����ˮ�Ҫ�õ�ʯ��ʯԭ��
D. 1996���˹��ϳ��˵�112��Ԫ���(Cn)��ʢ��抵�������Ӧ�����ı�ǩ��![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com