
【题目】已知阿伏加德罗常数的值为NA。下列说法正确的是
A. 常温下,14 g的![]() C含中子数目为6NA
C含中子数目为6NA
B. 将含3NA个离子的Na2O2固体溶于水配成1L溶液,所得溶液中Na+的浓度为2mol/L
C. 用铂电极电解100 mL 1 mol L-1的CuSO4溶液足够长时间,转移电子数一定为0.2NA
D. 标准状况下,2.24LCCl4含有的共价键数为0.4NA
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料,可用来制备肼、硝酸、硝酸铵和氯胺等。
(1)N2和H2以物质的量之比为1∶3在不同温度和压强下发生反应:N2+3H2![]() 2NH3,测得平衡体系中NH3的物质的量分数如右图。
2NH3,测得平衡体系中NH3的物质的量分数如右图。

① 下列途径可提高氨气产率的是________(填字母)。
a. 采用常温条件 b. 采用高温条件
c. 将原料气加压 d. 将氨液化,不断移去液氨
② 右图中所示的平衡体系中NH3的物质的量分数为0.549和0.478时,该反应的平衡常数分别为K1、K2,则K1________(填“>”“<”或“=”)K2。
(2)肼(N2H4)是一种火箭燃料。已知:
N2(g)+2O2(g)===2NO2(g);ΔH=+67.7 kJ·mol-1
N2H4(g)+O2(g)===N2(g)+2H2O(g);ΔH=-534.0 kJ·mol-1
NO2(g)===1/2N2O4(g);ΔH=-28.0 kJ·mol-1
① 反应2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g)的ΔH=________kJ·mol-1。
② 氨气与次氯酸钠溶液反应生成肼的离子方程式为__________________________。
(3)电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如右图。

① 阴极的电极反应式为____________________________________。
② 将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为________。
(4)饮用水消毒时,氯胺(NH2Cl等)在酸性条件下具有良好的效果(已知:NH2Cl+H2O≒NH3+HClO),其原因是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6. 0 mol L-1 H2SO4溶液由10 mL稀释至200 mL,再从中取出10 mL,这10 mL溶液中SO42-的物质的量浓度是
A. 0.05 mol L-1 B. 0.30 mol L-1
C. 0.15 mol L-1 D. 0.5 mol L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种气态烃,标况下的密度为1.25g/L,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示. 
(1)写出A的结构简式 .
(2)B、D分子中所含官能团的名称分别是、 .
(3)物质B可以直接氧化为D,需要加入的试剂是 .
(4)写出下列反应的化学方程式:
反应②的化学方程式:;反应类型: .
反应④的化学方程式:;反应类型: .
(5)B可由含淀粉的农产品如玉米、小麦、薯类等经发酵、蒸馏而得.请写出淀粉水解的化学方程式.
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铅蓄电池为电源,石墨为电极电解CuSO4溶液,装置如下图。若一段时间后Y电极上有6.4 g红色物质析出,停止电解。下列说法正确的是

A. a为铅蓄电池的负极
B. 电解过程中,铅蓄电池的负极增重30.3g
C. 电解结束时,左侧溶液质量增重8g
D. 铅蓄电池工作时正极电极反应式为:PbSO4+2e-=Pb+SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用如图所示装置制备并检验Cl2的性质.下列说法正确的是( ) 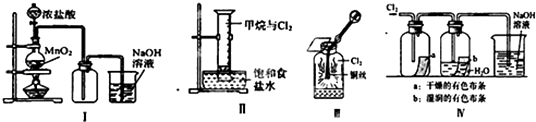
A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部被消耗
B.Ⅱ图中:量筒中发生了加成反应
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙两种溶液:甲 pH=2(c(H+)=10-2 mol/L)的醋酸溶液乙 pH=2(c(H+)=10-2 mol/L)的盐酸,请根据下列操作回答问题:
(1)取10mL的甲溶液,加入等体积的水,醋酸的电离平衡___移动(填“向左”、“向右”或“不”);另取10mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将___(填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其溶液中大小关系为:c(H+)(甲) ___c(H+) (乙)(填“大于”、“小于”或“等于”)。
(3)各取25mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)___________V(乙)(填“大于”、“小于”或“等于”)。
(4)下列事实能证明乙酸(CH3COOH)是弱电解质的是___.

A. 用乙酸(CH3COOH)溶液做导电性试验灯光较暗
B. 乙酸(CH3COOH)是共价化合物
C. 常温下,0.1 mol/L乙酸(CH3COOH)溶液的pH为2.2
D. 乙酸(CH3COOH)溶液不与NaCl反应
(5)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则Ka(HX) ______ Ka(CH3COOH)(填>、<或=)
(6)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO)-c(Na+)=_________mol·L-1(填精确值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣迸行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如下:

己知石油裂解己成为生产H的主要方法,E的溶液能发生银镜反应,G是具有香味的液体,试回答下列问题。
(1)G的结构简式为___________________。
(2)H→D的化学反应类型为_________________________。
(3)D→E的化学方程式:_______________________。
(4)己知:B在乳酸菌的催化作用下,可以生成乳酸,其分子式是C3H6O3;乳酸溶液能使紫色石蕊溶液变红色;乳酸能够在加热、浓硫酸作催化剂的条件下与乙酸进行酯化反应。
①乳酸中含有的官能团的名称是:_____________________。
②若乳酸中还含有一个甲基(-CH3),则乳酸的结构简式为____________________。
③乳酸可以分子间酯化形成六元环酯,则该环酯的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝—空气燃料电池具有原料易得、能量密度高等优点,装置如图所示,电池的电解质溶液为KOH溶液。下列说法正确的是

A. 放电时,消耗氧气22.4 L(标准状况),有4 mol OH-从左往右通过阴离子交换膜
B. 充电时,电解池阳极区的电解质溶液中c(OH-)逐渐增大
C. 放电过程的负极反应式:Al+3OH--3e-=Al(OH)3↓
D. 充电时,铝电极上发生还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com