
【题目】下列有关有机物的说法正确的是( )
A. C2H5COOC2H5存在C4H9COOH时可以加入饱和Na2CO3溶液后分液除去
B. 异戊烷也叫2-甲基戊烷
C. 分子式为C5H12O且能与金属钠反应产生气体的有机物,其同分异构体共有9种
D. 不能用溴水鉴别苯、乙醇、四氯化碳
【答案】A
【解析】
A.C2H5COOC2H5不溶于饱和Na2CO3溶液,C4H9COOH具有酸性,可以与碳酸钠溶液反应,所以C2H5COOC2H5存在C4H9COOH时可以加入饱和Na2CO3溶液后分液除去,故A正确;
B.戊烷有3种结构,正戊烷、异戊烷和新戊烷;其中异戊烷的结构简式:CH3-CH2-CH(CH3)CH3,其名称为:2-甲基丁烷,B错误;
C. 戊烷的同分异构体有CH3-CH2-CH2-CH2-CH3、![]() 、
、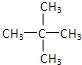 ,分子式为C5H12O且可与金属钠反应放出氢气的有机物为醇,有1-戊醇、2-戊醇、3-戊醇、2-甲基-1-丁醇、2-甲基-2-丁醇、3-甲基-2-丁醇、3-甲基-1-丁醇、2,2-二甲基-1-丙醇,所以有8种同分异构体,故C错误;
,分子式为C5H12O且可与金属钠反应放出氢气的有机物为醇,有1-戊醇、2-戊醇、3-戊醇、2-甲基-1-丁醇、2-甲基-2-丁醇、3-甲基-2-丁醇、3-甲基-1-丁醇、2,2-二甲基-1-丙醇,所以有8种同分异构体,故C错误;
D. 苯、乙醇溶液和四氯化碳分别与溴水混合的现象为:分层后有机层在上层、不分层、分层后有机层在下层,现象不同,可鉴别,故D错误;
综上所述,本题选A。


科目:高中化学 来源: 题型:
【题目】25℃时,SO2与NaOH反应后的溶液中存在含硫微粒H2SO3、HSO3-和SO32-,三者中各自所占的物质的量分数随溶液pH变化的关系如图所示。下列说法正确的是

A. a表示SO32-物质的量分数随溶液pH变化的曲线
B. pH=8昀溶液中:c(HSO3-)>c(SO32-)
C. pH=7的溶液中:c(Na+)= c(HSO3-)+2c(SO32-)
D. 1mol/L的NaHSO3溶液中存在: c(H2SO3)=c(H+)+c(OH-)+c(SO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2和NaClO2均具有漂白性,工业上用ClO2气体制备NaClO2的工艺流程如下图所示:

下列说法不正确的是
A. 工业上可将ClO2制成NaClO2固体,便于贮存和运输
B. 通入空气的目的是驱赶出ClO2,使其被吸收器充分吸收
C. 吸收器中生成 NaClO2的离子方程式:2ClO2+H2O2=2ClO2-+O2↑+2H+
D. 步骤a的操作包括过滤、洗涤和干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】儿种短周期元素的原子半径及主要化合价如下表

下列说法不正确的是
A. 由元素X和Q组成的化合物可能含有共价键
B. X、Z、R的最高价氧化物对应水化物可彼此反应
C. 离子半径:r(M2-)<r(R3-)
D. Z和Y形成的化合物为离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.1 g Na2X含有Na+ 0.1 mol,则Na2X的摩尔质量为________,X的相对原子质量为________。
(2)同温同压下,同体积的甲烷和氢气分子数之比为_______,原子个数之比为_____,质量之比为_________,电子数之比为________。
(3)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、Al2(SO4)3三种溶液中的SO42-都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知我们所学的烃和烃的衍生物具有下列转化关系,请回答有关问题

(1)写出以上三个反应的化学方程式(需注明反应所需的条件)
②_______________________________________________________
③_______________________________________________________
④_______________________________________________________
(2)在有机反应类型分类中,反应①属于__________,;
(3)含有4个碳原子,与C2H6互为同系物的物质的分子式为______,写出该组成互为同分异构体的化合物的结构简式________,________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据信息书写指定反应的方程式。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:稀硫酸、KCl、K2CO3、KI、Br2、CuCl2
①Ba(OH)2→KOH的化学方程式:___;
②Fe2+→Fe3+的离子方程式:___。
(2)B2O3可发生如图所示的转化:

①“置换”反应在高温下进行,写出该反应的化学方程式:___;
②写出“氧化”反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室根据反应:TiO2(s)+CCl4(g)![]() TiCl4(g)+CO2(g),在无氧无水条件下制备TiCl4,实验装置如下图所示(CCl4、TiCl4的沸点分别为76℃、136℃,且两者互溶)。
TiCl4(g)+CO2(g),在无氧无水条件下制备TiCl4,实验装置如下图所示(CCl4、TiCl4的沸点分别为76℃、136℃,且两者互溶)。

下列说法不正确的是
A. ③中反应完成后,先停止通N2,再停止加热
B. ①、⑤装置中分别盛有无水氯化钙、浓硫酸
C. ②中热水使CCl4气化,④中冰水使TiCl4冷凝
D. ④中分离TiCl4、CCl4混合物的方法是精馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二醚水蒸气重整制氢过程涉及的主要反应如下:
i CH3OCH3(g)+H2O(g)===2CH3OH(g) △H=+23. 6 kJ·mol-1
ii CH3OH (g)+ H2O (g)=CO2(g)+3H2(g) △H=+49. 5 kJ·mol-1
iii CH3OH (g)==CO(g)+2H2(g) △H=+90.7 kJ·mol-1
iv H2O (g)+ CO (g)= CO 2(g)+ H2(g) △H=-41.2 kJ·mol-1
各反应平衡常数与温度变化关系如下表:

(1)重整反应CH3OCH3(g)+3H2O(g)===2CO2(g)+6H2(g) △H=x kJ·mol-1,回答下列问题:
①x=___________
②有利于提高重整反应中CH3OCH3平衡转化率的条件为___________(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
③若在恒温刚性容器中进行重整反应,达到平衡时[CH3OCH3]=10mol·L-1,[H2O]=0.2mol·L-1,[H2]=10 mol·L-1,[CO2]=40 mol·L-1则反应温度约为___________。
④723K时,v=k·[c(CH3OCH3)]2·[c(CO2)]-1.5为重整反应速率方程。在相同条件下,c(CO2)分别为a、b、c时,H2产率随时间的变化关系如图,则a、b、c由小到大的顺序为___________。

(2)CO会造成燃料电池催化剂中毒,重整反应体系中CO体积分数随水醚比与温度的变化关系如右图。

①相同温度下,水醚比为___________时CO体积分数最高。
②实际生产中选择反应温度为250℃的原因为___________;选择水醚比为3~6的原因为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com