
【题目】新型锂-空气电池具有能量密度高的优点,可以用作新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过。下列说法正确的是
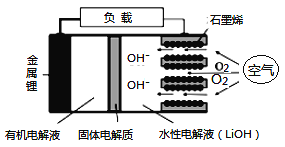
A. Li+穿过固体电解质向正极移动而得到LiOH溶液
B. 放电时,当外电路中有1 mol e-转移时,水性电解液离子总数增加NA
C. 应用该电池电镀铜,阴极质量增加64 g,理论上将消耗11.2 L O2
D. 放电时,负极反应式:Li-e-+OH-=LiOH
【答案】A
【解析】A项,由图示可得,放电时铝在负极失电子,氧气在正极得电子,固体电解质只允许Li+通过,所以Li+穿过固体电解质向正极移动而得到LiOH溶液,故A正确;B项,放电时正极反应为:O2+2H2O+4e-=4OH-,当外电路中有1mole-转移时,生成1mol OH-,同时1molLi+穿过固体电解质进入水性电解液,所以离子总数增加2NA,故B错误;C项,根据电子守恒,应用该电池电镀铜,阴极质量增加64g,即生成1mol铜,则电路中通过2mol电子,理论上消耗0.5molO2,在标准状况下体积为11.2 L,若不是标准状况则不一定,故C错误;D项,因为固体电解质只允许Li+通过,所以放电时,负极反应式:Li-e-=Li+,故D错误。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为________。
(2)硫化氢(H2S)分子的空间构型为________;二氧化碳(CO2)分子的空间构型为________;甲烷(CH4)分子的空间构型为________。
(3)由于氨水和次氯酸盐溶液在弱碱性介质中反应可生成氯胺(H2NCl),分子结构类似于NH3,H2NCl分子的空间构型为________,电子式为________,H2NCl中氯的化合价为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】印染工业常用亚氯酸钠(NaClO2)漂白织物。用过氧化氢法生产亚氯酸钠的工艺流程如下:
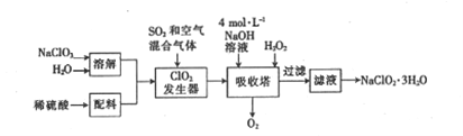
已知:①NaClO2的溶解度随温度的升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②Ksp(FeS)=6.3×10-18;Ksp(CuS)= 6.3×10-36;Ksp(PbS)=2.4×10-28。
(1)发生器中反应的还原剂是_________(填化学式,下同)。吸收塔内ClO2在碱性条件下与H2O2生成NaClO2 的离子方程式为_______
(2)从滤液中得到的NaClO2·3H2O的操作依次是_______、(填字母)、洗染、干燥。
a.蒸馏 b.灼烧 c.冷却结晶 d.蒸发浓缩 e.过滤
(3)亚氯酸钠漂白织物时真正起作用的是HClO2。下表是25℃时HClO2及几种常见弱酸的电离平衡常数。
弱酸 | HClO2 | HF | HCN | H2S |
Ka/mol·L-1 | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
①常温下,物质的量浓度相同的NaF、NaCN 两种溶液的PH由大到小的顺序为________。
②等体积等物质的量浓度的HClO2与NaOH溶液充分反应后,溶液中各离子浓度由大到小的顺序为_____。
③Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+,滴加Na2S溶液后最先析出的沉淀是______;当最后一种离子沉淀完全时(该离子浓度为10-5 mol·L-l),此时体系中S2-的浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有NaCl、NaOH、AgNO3三种溶液,只用一种试剂就可把它们鉴别开来,该试剂是( )
A.FeCl3溶液
B.Na2CO3溶液
C.MgCl2溶液
D.盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机材料,广泛应用于电子、陶瓷等工业领域.在一定条件下,AlN可通过反应Al2O3+N2+3C![]() 2AlN+3CO合成.已知AlN可与NaOH溶液反应放出有刺激性气味的气体.下列叙述正确的是
2AlN+3CO合成.已知AlN可与NaOH溶液反应放出有刺激性气味的气体.下列叙述正确的是
A. 上述反应中,N2是还原剂,Al2O3是氧化剂
B. 上述反应中,每生成1molAlN需转移6mol电子
C. AlN中氮元素的化合价为+3
D. AlN与NaOH溶液反应的化学方程式为:AlN+NaOH+H2O═NaAlO2+NH3↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案能达到目的的是( )
A. 用品红溶液检验SO2
B. 用焰色反应鉴别KNO3和KCl
C. 用澄清石灰水鉴别MgCl2溶液和NaHCO3溶液
D. 用丁达尔效应区分FeCl3溶液和Fe2(SO4)3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碳酸钠样品中含有少量氯化钠杂质,为测定该样品中碳酸钠的质量分数,进行了如下实验:

请回答下列问题:
(1)操作A用到的玻璃仪器除烧杯外还必需有_______________、_______________;
(2)在实验过程中加入饱和石灰水后发生反应的离子方程式是_____________________。
(3)为探究上述反应后滤液中的溶质成分,甲同学向滤液中滴加过量稀盐酸,发现无气泡产生,说明滤液中一定不含 _________________(填溶质的化学式,下同),若有气泡产生,那么测定的样品中碳酸钠的质量分数___________(填偏大、偏小、无影响)。
(4)在(3)探究中,滴加盐酸前滤液中的溶质除氯化钠外,一定还含有的溶质是________;滴加盐酸的过程中一定发生反应的离子方程式为 ___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,碳素钢腐蚀与表面水膜pH的关系如下:
pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
腐蚀快慢 | 较快 | 慢 | 较快 | ||||
主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO |
下列说法不正确的是
A. 在pH<4的溶液中,主要发生析氢腐蚀
B. 在pH>6的溶液中,主要发生吸氧腐蚀
C. 在pH>14的溶液中,正极反应为O2+4OH-+4e-===2H2O
D. 在煮沸除氧气后的碱性溶液中,腐蚀速率会减慢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com