
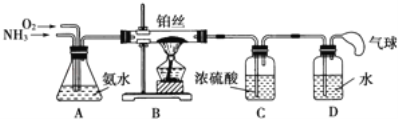
【题目】学生设计的用氨催化法制取少量HNO3溶液的实验装置如图所示:
(1)实验室制备NH3,下列方法中适宜选用的是 (填序号).
①固态氯化铵与熟石灰混合加热 ②固态氯化铵加热分解
③碱石灰中滴加浓氨水 ④氯化铵溶液与氢氧化钠溶液共热
(2)装置B中发生反应的化学方程式为 .
(3)装置C的作用是 ;
装置C中的现象是 ;为确保装置D中尽可能多地生成HNO3,所通入O2和NH3的体积比应大于 .
(4)装置D中发生的反应化学方程式为 .
【答案】(1)①③;(2)4NH3+5O2![]() 4NO+6H2O(3)吸收未反应的NH3;有气泡从浓硫酸中冒出,且装置C内的上部呈红棕色; 2:1;(4)3NO2+H2O═2HNO3+NO
4NO+6H2O(3)吸收未反应的NH3;有气泡从浓硫酸中冒出,且装置C内的上部呈红棕色; 2:1;(4)3NO2+H2O═2HNO3+NO
【解析】
试题分析:(1)①固态氯化铵与熟石灰混合加热,是实验室制氨气的主要方法,①正确;②固态氯化铵加热分解,成氨气和氯化氢,氯化氢和氨气遇冷反应会生成氯化铵,不能用于制备氨气,②错误;③碱石灰中滴加浓氨水,是实验室制氨气的方法之一,③正确;④氯化铵溶液与氢氧化钠溶液共热,能制备氨气,但量少,不是实验室制备氨气的方法,④错误;答案选:①③;
(2)装置B中发生氨催化氧化生成一氧化氮和水,方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(3)装置C浓硫酸的作用是吸收未反应的NH3,装置B中产生的NO通过浓硫酸时,可看到浓硫酸中有气泡冒出,同时NO在装置C的上部与O2迅速反应生成红棕色的NO2;为确保装置D中尽可能多地生成HNO3,也就是说NH3通过转化后最好全部生成HNO3,由4NH3+5O2![]() 4NO+6H2O及4NO+3O2+2H2O=4HNO3可得:NH3+2O2=HNO3+H2O,可知通入O2和NH3的体积比应大于2:1;
4NO+6H2O及4NO+3O2+2H2O=4HNO3可得:NH3+2O2=HNO3+H2O,可知通入O2和NH3的体积比应大于2:1;
(4)装置D中发生NO2与H2O的反应,方程式为:3NO2+H2O═2HNO3+NO。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】水是一种重要的自然资源,水质优劣直接影响人体健康,水处理技术在生产、生活中应用广泛。聚合硫酸铁(PFS)是水处理中重要的絮凝剂。以黄铁矿的烧渣(主要成分为Fe2O3、FeO、SiO2等)和废铁屑为原料制取聚合硫酸铁([Fe2(OH)x(SO4)3-![]() ]m)的工艺流程如图:
]m)的工艺流程如图:
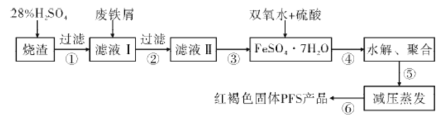
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有______(填标号)。
a.容量瓶 b.烧杯 c.玻璃棒 d.分液漏斗
(2)废铁屑表面附有铁锈,铁锈的主要成分为______,步骤③的具体实验操作有____。
(3)水解、聚合要严控pH和温度。pH偏小时Fe3+水解程度弱,pH偏大时则______。写出水解、聚合反应生成PFS的化学方程式:_________。
(4)步骤⑥相对于常压蒸发,减压蒸发的优点是_________。
(5)污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀。下列物质能作为沉淀剂的是_______(填标号)。
a.氨水 b.硫化氢气体 c.硫酸钠溶液 d.纯碱溶液
(6)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO)。若某天然水中c(Ca2+)=1.5×10-3mol/L,c(Mg2+)=6.4×10-4mol/L,则此水的硬度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢原子个数之比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯能使酸性KMnO4溶液褪色
D.乙烯易与溴水发生加成反应,且1mol乙烯完全加成消耗1mol溴单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZnSe是一种光电性能优异的半导体材料,某研究小组用如图1方法制备了ZnSe.

![]() 溶于水生成
溶于水生成![]() ,下列物质与水反应,跟此反应类型相同的是 ______
,下列物质与水反应,跟此反应类型相同的是 ______
![]()
![]()
![]()
![]()
![]()
![]() 硒酸
硒酸![]() 的水溶液按下式发生一级和二级电离:
的水溶液按下式发生一级和二级电离:![]() ;
;![]() ,
,![]()
![]() 溶液显 ______
溶液显 ______ ![]() 填“酸性”、“中性”、“碱性”
填“酸性”、“中性”、“碱性”![]() .
.
![]() 向
向![]() 溶液中滴加少量氨水,该反应的离子方程式为 ______ .
溶液中滴加少量氨水,该反应的离子方程式为 ______ .
![]() 已知
已知![]() 的两级电离常数分别为
的两级电离常数分别为![]() ,
,![]() ,则
,则![]() 和
和![]() 两溶液混合后反应的离子方程式为 ______ .
两溶液混合后反应的离子方程式为 ______ .
![]() 肼
肼![]() 与
与![]() 反应的氧化产物是
反应的氧化产物是![]() 氧化剂与还原剂的物质的量之比为 ______ .
氧化剂与还原剂的物质的量之比为 ______ .
![]() 电化学降解法可用于治理水中硝酸盐的污染,所得产物可直接排入大气.其原理如图2所示,其中B为电源的 ______ 极,乙池中电极反应式为 ______ ,为使反应持续进行,须适时向甲池中添加 ______ .
电化学降解法可用于治理水中硝酸盐的污染,所得产物可直接排入大气.其原理如图2所示,其中B为电源的 ______ 极,乙池中电极反应式为 ______ ,为使反应持续进行,须适时向甲池中添加 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
I. 甲醇可以替代汽油和柴油作为内燃机燃料。
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃、101 kPa时,1 mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518 kJ热量。该反应的热化学方程式为______。
(2)已知:25℃、101 kPa时,CH3OH(l) + 3/2 O2(g) ==== CO2 (g) + 2H2O(l) Δ H=-726.5 kJ/mol。相同质量的甲醇和辛烷分别完全燃烧时,放出热量较多的是______。
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如右所示。
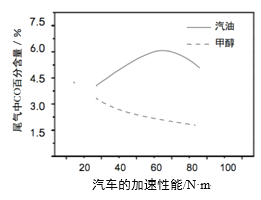
根据图信息分析,与汽油相比,甲醇作为燃料的优点是______。
II. 甲醇的合成
(4)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

① 补全上图:图中A处应填入______。
② 该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH______(填“变大”“变小”或“不变”)。
(5)已知: CO(g)+1/2 O2(g) ==== CO2(g) ΔH1=-283 kJ/mol
H2(g)+1/2 O2(g) ==== H2O(g) ΔH2=-242 kJ/mol
CH3OH(g) + 3/2 O2(g) ==== CO2 (g) + 2H2O(g) ΔH3=-676 kJ/mol
以CO(g)和H2(g)为原料合成甲醇的反应为CO(g) + 2H2(g) ==== CH3OH(g) 。该反应的ΔH为_____ kJ/mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0,降低温度产生的影响为( )
2SO3(g) ΔH<0,降低温度产生的影响为( )
A.v正 增大,v逆减小B.v正减小,v逆增大
C.v正和v逆同程度的增大D.v正和v逆不同等程度的减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种短周期元素,它们的结构、性质等信息如下表所示:
元素 | 结构、性质等信息 |
A | 是元素周期表中(除稀有气体外)原子半径最大的元素,该元素某种合金是原子反应堆导热剂 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
E | L层上有2对成对电子 |
请根据表中信息填写:
(1)B原子的简化电子排布式_____。
(2)A元素在周期表中的位置_____;离子半径:A_____B(填>、=或< )。
(3)E原子的价电子排布图是____,其原子核外有______个未成对电子,能量最高的电子为_____轨道上的电子,其轨道呈_____形。
(4)D原子的外围电子排布式为____,D-的离子结构示意图是_____。
(5)C、E元素的第一电离能的大小关系是_____(用元素符号表示,下同)。
(6)已知CD3分子中D元素为+1价,则C、D的电负性大小关系是____,CD3的中心原子杂化轨道类型是___,CD3与水反应的化学方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用软锰矿浆烟气脱硫吸收液制取电解锰,并利用阳极液制备高纯碳酸锰、回收硫酸铵的工艺流程如下(软锰矿的主要成分是MnO2,还含有硅、铁、铝的氧化物和少量重金属化合物等杂质):

(1)一定温度下,“脱硫浸锰”主要产物为MnSO4,该反应的化学方程式为______________________。
(2)“滤渣2”中主要成分的化学式为______________________。
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是_______________________________________。
(4)“电解”时用惰性电极,阳极的电极反应式为____________________________。
(5)“50℃碳化”得到高纯碳酸锰,反应的离子方程式为_______________________________________。“50℃碳化”时加入过量NH4HCO3,可能的原因是______________________________________(写两种)。
(6)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O![]() NH3·H2O+H+,则该反应的平衡常数为____________________。
NH3·H2O+H+,则该反应的平衡常数为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在绝热恒容密闭容器一定条件下使反应2A(g)+B(s)![]() 3C(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
3C(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
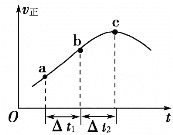
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应ΔH>0
D.Δt1=Δt2时,a~b段消耗A的量小于b~c段
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com