
【题目】工业上利用软锰矿浆烟气脱硫吸收液制取电解锰,并利用阳极液制备高纯碳酸锰、回收硫酸铵的工艺流程如下(软锰矿的主要成分是MnO2,还含有硅、铁、铝的氧化物和少量重金属化合物等杂质):

(1)一定温度下,“脱硫浸锰”主要产物为MnSO4,该反应的化学方程式为______________________。
(2)“滤渣2”中主要成分的化学式为______________________。
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是_______________________________________。
(4)“电解”时用惰性电极,阳极的电极反应式为____________________________。
(5)“50℃碳化”得到高纯碳酸锰,反应的离子方程式为_______________________________________。“50℃碳化”时加入过量NH4HCO3,可能的原因是______________________________________(写两种)。
(6)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O![]() NH3·H2O+H+,则该反应的平衡常数为____________________。
NH3·H2O+H+,则该反应的平衡常数为____________________。
【答案】 MnO2+SO2===MnSO4或H2O+SO2 ===H2SO3、MnO2+H2SO3===MnSO4+H2O Fe(OH)3、Al(OH)3 Na2S会增大回收的(NH4)2SO4中Na+含量 4OH--4e-=== O2↑+2H2O Mn2++2HCO3- ![]() MnCO3↓+CO2↑+H2O 使MnSO4充分转化为MnCO3; NH4HCO3受热易分解,造成损失;NH4HCO3能与H+反应,防止MnCO3沉淀溶解损失 5.7×10-10
MnCO3↓+CO2↑+H2O 使MnSO4充分转化为MnCO3; NH4HCO3受热易分解,造成损失;NH4HCO3能与H+反应,防止MnCO3沉淀溶解损失 5.7×10-10
【解析】由流程可知,“脱硫浸锰”环节:二氧化硫与软锰矿浆作用生成硫酸锰和少量的硫酸铝、硫酸亚铁等,二氧化硅不反应经过滤成为滤渣Ⅰ;氧化环节:双氧水可将亚铁离子氧化为铁离子;加氨水调节溶液的pH=5~6把铁离子和铝离子转化为沉淀除去;加硫化铵把重金属转化为沉淀除去;通过电解得到金属锰;在阳极液中加碳酸氢铵得碳酸锰和硫酸铵等,据此分析解答。
(1)“脱硫浸锰”生成MnSO4的反应的化学方程式为 MnO2+SO2=MnSO4或H2O+SO2=H2SO3、MnO2+H2SO3=MnSO4+H2O;(2)加入氨水沉淀金属阳离子,“滤渣2”中主要成分的化学式为Fe(OH)3、Al(OH)3;(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是 加Na2S会引入钠离子,增大回收的(NH4)2SO4中Na+含量;(4)“电解”时用惰性电极,阳极应该是水电离出的氢氧根离子放电,电极反应式为 2H2O-4e-=O2↑+4H+或4OH--4e-=O2↑+2H2O;(5)“50℃碳化”得到高纯碳酸锰,反应的离子方程式为 Mn2++2HCO3- ![]() MnCO3↓+CO2↑+H2O;原溶液显酸性,且碳酸氢铵受热易分解,故“50℃碳化”时加入过量NH4HCO3,可能的原因是NH4HCO3与H+反应,防止MnCO3沉淀溶解损失,以及防止NH4HCO3受热分解损失;(6)根据方程式NH4++H2O
MnCO3↓+CO2↑+H2O;原溶液显酸性,且碳酸氢铵受热易分解,故“50℃碳化”时加入过量NH4HCO3,可能的原因是NH4HCO3与H+反应,防止MnCO3沉淀溶解损失,以及防止NH4HCO3受热分解损失;(6)根据方程式NH4++H2O![]() NH3·H2O+H+可知反应的平衡常数=
NH3·H2O+H+可知反应的平衡常数=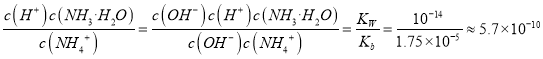 。
。


科目:高中化学 来源: 题型:
【题目】已知碳碳单键可以绕键轴自由旋转,结构简式为如下图所示的烃,下列说法中正确的是( )

A. 分子中处于同一直线上的碳原子最多有6个
B. 分子中至少有12个碳原子处于同一平面上
C. 该烃苯环上的一氯代物共有 3种
D. 该烃苯环上一氯代物共有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 HF(aq) + BF3(aq) = H+(aq) + BF4-(aq) 能够发生的原因是( )
A. 强氧化剂制弱氧化剂 B. 强酸制弱酸
C. “熵增效应(熵判据)” D. 产物中形成了配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
A. 容器内的总压强不随时间变化
B. 断裂4molH—O键的同时,断裂4molH—H键
C. 混合气体的平均相对分子质量不变
D. 反应不再进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s) ![]() yC(g) ΔH<0,一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
yC(g) ΔH<0,一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:

(1)用A的浓度变化表示该反应在0~10 min内的平均反应速率v(A)=______________________。
(2)根据图示可确定x∶y=________。
(3)0~10 min容器内压强________(填“变大”、“不变”或“变小”)。
(4)推测第10 min引起曲线变化的反应条件可能是______________________;第16min引起曲线变化的反应条件可能是________________________。
①减压 ②增大A的浓度 ③增大C的量 ④升温⑤降温 ⑥加催化剂
(5)若平衡Ⅰ的平衡常数为K1,平衡Ⅱ平衡常数为K2,则K1________K2(填“>”、“=”或“<”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com