
【题目】常温下,向lL0.lmol·L-1一元酸HR溶液中逐渐通人氨气[已知常温下Kb(NH3H2O)=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如右图所示。下列叙述正确的是

A. 0.1 mol·L-1HR溶液的pH约为3
B. HR为弱酸,常温时Ka (HR) =1×l0-7
C. 当通入0.1molNH3 时,c(R-) >c(NH4+)
D. 当c(HR) =c(R-)时,溶液必为中性
【答案】A
【解析】A.pH=5时,lg![]() =0,则
=0,则![]() = 1,说明HR在溶液中不能完全电离,HR是弱酸,根据HR
= 1,说明HR在溶液中不能完全电离,HR是弱酸,根据HR![]() H++R-可知,Ka(HR) =
H++R-可知,Ka(HR) = ![]() ,pH=5时,Ka(HR)=c(H+)=10-5mol/L,因溶液温度不变,则Ka始终不变。设0.1 mol·L-1HR溶液中H+的浓度为xmol/L,则Ka =
,pH=5时,Ka(HR)=c(H+)=10-5mol/L,因溶液温度不变,则Ka始终不变。设0.1 mol·L-1HR溶液中H+的浓度为xmol/L,则Ka = ![]() =
=![]() =10-5mol/L,解得x=10-3mol/L,则pH=-lgc(H+)=3,故A正确;B.根据A项分析可知,HR是弱酸,常温时Ka(HR)=10-5mol/L,故B错误;C. lL0.lmol·L-1一元酸HR溶液中n(HR)=0.1mol,当通入0.1molNH3 时,恰好与HR完全反应,得NH4R溶液,因Ka(HR)<Kb(NH3H2O),所以R-的水解程度大于NH4+的水解程度,则c(R-)<c(NH4+),故C错误;D.据图可知,当c(HR) =c(R-)时,lg
=10-5mol/L,解得x=10-3mol/L,则pH=-lgc(H+)=3,故A正确;B.根据A项分析可知,HR是弱酸,常温时Ka(HR)=10-5mol/L,故B错误;C. lL0.lmol·L-1一元酸HR溶液中n(HR)=0.1mol,当通入0.1molNH3 时,恰好与HR完全反应,得NH4R溶液,因Ka(HR)<Kb(NH3H2O),所以R-的水解程度大于NH4+的水解程度,则c(R-)<c(NH4+),故C错误;D.据图可知,当c(HR) =c(R-)时,lg![]() =0,pH=5,溶液成酸性,故D错误;答案选A。
=0,pH=5,溶液成酸性,故D错误;答案选A。


科目:高中化学 来源: 题型:
【题目】已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1mol H﹣O键形成时放出热量463kJ,则氢气中1mol H﹣H键断裂时吸收热量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于非金属元素Si、N、S、Cl的叙述,正确的是
A. 通常情况下,它们的单质均为气体 B. 它们在自然界中都存在游离态的单质
C. 它们都有对应的含氧酸 D. 每种元素都只有一种氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,将足量的BaSO4固体溶于50mL水中,充分搅拌,慢慢加入Na2CO3固体,搅拌,溶液中随c(CO32-)增大时c(Ba2+)变化曲线如下图。则下列说正确的是
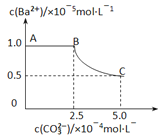
A. 20℃时Ksp(BaSO4)>Ksp(BaCO3)
B. 加入Na2CO3固体立即有BaCO3固体生成
C. BaCO3的Ksp=2.5×10-10
D. 曲线BC段内,c(CO32-):c(SO42-)=25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组为了测定某(CuCl22H2O)样品的纯度,设计了如下方案:称取1.0 g样品溶解于适量水中,向其中加入含AgNO3 2.38 g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2 mol·L-1的KSCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定样品的纯度。请回答下列问题:
(1)判断滴定达到终点的现象是___________________。
(2)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果_____________(选填“偏高”、“偏低”或“无影响”)。
(3)若到达滴定终点时,用去KSCN标准溶液20.00mL,求此样品的纯度__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关铁及其化合物的说法中正确的是
A. 赤铁矿的主要成分是FeO
B. 除去FeCl2溶液中的FeCl3杂质可以向溶液中加铁粉,然后过滤
C. 铁与水蒸气在高温下反应的产物为Fe2O3和H2
D. Fe3+与KSCN反应产生红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用H++OH-=H2O来表示的化学反应是
A.固体Cu(OH)2和H2SO4溶液反应B.澄清石灰水和HNO3溶液反应
C.KOH溶液和醋酸溶液反应D.Ba(OH)2溶液和H2SO4溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( ) 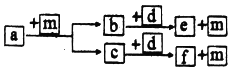
A.简单离子半径:Z<Y
B.非金属性:X>Y
C.简单气态氢化物的热稳定性:Y>X
D.W2Y2中含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是( )
A.制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+
B.H2SO4溶液中投入锌粒:2H++Zn═H2↑+Zn2+
C.用NaHCO3 治疗胃酸过多:HCO3﹣+H+═CO2↑+H2O
D.氯化铁和氢氧化钾溶液混合:Fe3++3OH﹣═Fe(OH)3↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com