
【题目】铬元素(Cr)的化合物存在下列转化关系:

下列判断错误的是
A.反应①表明Cr2O3,具有酸性氧化物的性质
B.反应②利用了H2O2的氧化性
C.反应③发生的反应为2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O
D.反应①②③中铬元素的化合价均发生了变化
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)在①![]() Li ②石墨 ③C60 ④
Li ②石墨 ③C60 ④![]() Mg ⑤ CH3CH2OH ⑥
Mg ⑤ CH3CH2OH ⑥![]() C ⑦
C ⑦![]() Li ⑧ CH3OCH3 中:____互为同位素; ____互为同分异构体;___互为同素异形体(填序号)
Li ⑧ CH3OCH3 中:____互为同位素; ____互为同分异构体;___互为同素异形体(填序号)
(2)现有①CaCl2 ②金刚石 ③NH4Cl ④Na2SO4 ⑤冰 等五种物质,按下列要求回答:
①熔化时不需要破坏化学键的是___________,熔点最高的是_______。(填序号)
②只含有离子键的物质是______,晶体以分子间作用力结合的是______。(填序号)
(3)写出下列物质的电子式
①H2O______
②NaOH______
③NH3______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“>”、“<”或“=”填空:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),光照和点燃条件的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1______ΔH2;
(2)相同条件下,2mol氢原子所具有的能量____1mol氢分子所具有的能量;
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1_____ΔH2。
①4P(白磷,s) +5O2(g)=2P2O5(s) ΔH1,②4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;
(4)已知:101 kPa时,2C(s) +O2(g)=2CO(g) ΔH=-221kJ·mol-1,则碳的燃烧热数值____110.5 kJ·mol-1;
(5)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1 mol水,放出的热量________57.3 kJ;
(6)可逆反应:aA(气)+bB(气)![]() cC(气)+dD(气);ΔH=Q,根据图回答:
cC(气)+dD(气);ΔH=Q,根据图回答:

P1______ P2;②(a+b)______(c+d);③t1℃______ t2℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关键环节题组:有机合成路线设计
(1)用丙醛(CH3—CH2—CHO)制取聚丙烯的过程中发生的反应类型为________
①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原
A.⑥②③ B.⑤②③ C.②④⑤ D.①④⑥
(2)以CH2==CHCH2OH为主要原料(无机试剂任用)设计CH2==CHCOOH的合成路线流程图(已知CH2=CH2可被氧气催化氧化为 ![]() )_________________
)_________________
学法题:通过此题的解答,总结设计有机合成路线需注意(至少写2条)___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子.在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2·2CO·2H2O
(1)X基态原子的电子排布式为__________________.
(2)C、H、O三种原子的电负性由大到小的顺序为__________.
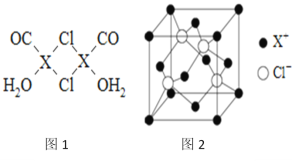
(3)X2Cl2·2CO·2H2O是一种配合物,其结构如图1所示:
①与CO为互为等电子体的分子是_________.
②该配合物中氯原子的杂化方式为__________.
③在X2Cl22CO2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键_____________.
(4)阿伏加德罗常数的测定有多种方法,X射线衍射法就是其中的一种。通过对XCl晶体的X射线衍射图象的分析,可以得出XCl的晶胞如图2所示,则距离每个X+最近的Cl﹣的个数为____________,若X原子的半径为a pm,晶体的密度为ρg/cm3,试通过计算阿伏加德罗常数NA=___________________(列计算式表达)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法中不正确的是
A. CO2是氧化产物
B. H2C2O4在反应中被氧化
C. H2C2O4的氧化性强于ClO2的氧化性
D. 1mol KClO3参加反应,转移的电子为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组进行Cu和Fe2(SO4)3溶液的实验。实验探究过程如下:
实验装置:
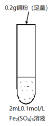
实验操作与现象: ⅰ.加入Cu粉后充分振荡,静置,溶液变成浅蓝绿色;
ⅱ.取少量ⅰ中清液于试管中,滴加3滴0.1mol/L KSCN溶液,立即出现白色沉淀,溶液局部变为红色,振荡后红色迅速褪去。
查阅资料:
Ⅰ.Cu2+可与SCN-反应生成CuSCN(白色沉淀)和(SCN)2: (SCN)2的性质与Cl2相似。
Ⅱ.CuSCN能与稀硝酸反应:CuSCN+HNO3→CuSO4+N2↑+CO2+H2O(未配平)。
回答下列问题:
(1)Cu和Fe2(SO4)3溶液反应的离子方程式为________。
(2)根据表中实验现象推断白色沉淀为___________。为验证该白色沉淀,取少量白色沉淀于试管中,加入___,若____即可证明(补充所加试剂及实验现象)。
(3)试解释ⅱ中溶液局部变为红色的原因是______。
(4)根据ⅱ中实验现象可推知SCN-更易与_______结合(填“Fe3+”或“Cu+”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向等物质的量浓度的![]() 、
、![]() 混合溶液中滴加稀盐酸。
混合溶液中滴加稀盐酸。
①在滴加盐酸过程中,溶液中![]() 与含硫各物质浓度的大小关系为______(选填字母)。
与含硫各物质浓度的大小关系为______(选填字母)。
a. ![]()
b. ![]()
c. ![]()
d. ![]()
②![]() 溶液中所有阴离子浓度由大到小排列是____________;
溶液中所有阴离子浓度由大到小排列是____________;![]() 溶液呈碱性,若向溶液中加入
溶液呈碱性,若向溶液中加入![]() 溶液,恰好完全反应,所得溶液呈强酸性,其原因是____________(用离子方程式表示)。
溶液,恰好完全反应,所得溶液呈强酸性,其原因是____________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. Ba(HCO3)2溶液与少量的NaOH溶液反应:Ba2++HCO![]() +OH-=BaCO3↓+H2O
+OH-=BaCO3↓+H2O
B. 次氯酸钙溶液中通入过量的二氧化碳 Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
C. 用氨水吸收少量二氧化硫 OH-+SO2=HSO3-
D. 硫酸与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com