
【题目】有关水在人体中的作用,正确的说法是( )
A. 水是一种很好的溶剂 B. 水在人体内没有调节体温的作用
C. 饮用水越纯净越好 D. 没有污染的水就是纯净水
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.漂白粉、漂粉精是纯净物
B.漂白粉中含有次氯酸,所以漂白粉能使染料等有机色素褪色
C.工业上将氯气通入澄清石灰水制取漂白粉
D.次氯酸能杀死病菌,所以氯气可用于自来水的消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料。氯化水解法生产三氯氧磷的流程如下:

(1)氯化水解法生产三氯氧磷的化学方程式为___________________________。
(2)氯化水解法生产三氯氧磷时,会产生含磷(主要为H3PO3、H3PO4等)废水,已知H3PO3是一种淡黄色晶体,且易溶于水的二元弱酸。
①若用20 mL H3PO3溶液与同浓度的NaOH溶液40mL恰好完全反应,生成的盐为___________________(填“正盐”或“酸式盐”)。
②H3PO3中,P元素的化合价为_______________________。H3PO3可以将溶液中的Ag+还原,从而用于化学镀银,写出该离子方程式_________________________。
③处理废水时,先在其中加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸钙沉淀并回收,加入漂白粉的作用是______________________________________。
④若处理后的废水中c(PO43ˉ)=4×10ˉ7mol·Lˉ1,溶液中c(Ca2+)=________mol·Lˉ1。(已知Ksp[Ca3(PO4)2]=2×10ˉ29)
(3)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取a g产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 mol·Lˉ1的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用c mol·Lˉ1 NH4SCN溶液滴定过量Ag+至终点,记下所用体积。
已知:Ksp(AgCl)=3.2×10ˉ10,Ksp(AgSCN)=2×10ˉ12
①滴定选用的指示剂是__________(选填字母)。
a.FeCl2b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②实验过程中若未加入硝基苯这项操作,所测Cl元素含量将会_______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于某有机物的性质叙述不正确的是
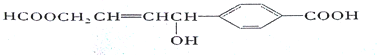
A. 1 mol该有机物完全燃烧可生成12molCO2
B. lmol该有机物分别与足量Na或NaHCO3反应,产生的气体分子数目相等
C. 1 mol该有机物可以与5mol H2发生加成反应
D. 1 mol该有机物可以与2 molNaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素X、Y的核电荷数分别是a和b,它们的离子Xm+和Yn-的核外电子排布相同,则下列关系式正确的是( )
A. a=b+m+n B. a=b-m+n C. a=b+m-n D. a=b-m-n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用烃A合成高分子化合物N的流程如下图:
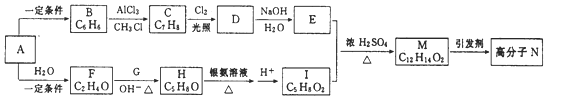
经测定烃A在标准状况下的密度为1.16g·L-1,F和G是同系物,核磁共振氢谱显示有机物H中有四种峰,且峰值比为3:3:1:1。
已知:Ⅰ. 
Ⅱ. ![]()
Ⅲ. 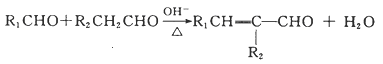 (R1、R2、R3代表烃基或氢原子)。
(R1、R2、R3代表烃基或氢原子)。
回答下列问题:
(1)写出A的结构简式:___________________。
(2)H中所含官能团的名称是___________________。
(3)H→I、M→N的反应类型分别是____________、______________。
(4)写出F和G反应生成H的化学方程式______________________。
(5)E和I反应生成M的化学方程式为_______________________。
(6)芳香族化合物Q是M的同分异构体,与M具有相同官能团,且水解可以生成2-丙醇,则Q的种类有___________种。(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分燃烧2.8g某有机物A,生成8.8g CO2和3.6g H2O,这种有机物蒸气的相对密度是相同条件下N2的2倍。
(1)求该有机物的分子式。
(2)该有机物链状同分异构体的结构简式为: 。
(3) 若有机物A在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),则用键线式表示的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8,下列说法不正确的是 ( )
A. 与W相邻的同主族元素可制成重要的半导体材料
B. X单质不可能置换出W单质
C. 元素原子半径从大到小的顺序是X、Y、Z
D. W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是HZO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是一种新型的燃料电池,它是以固体氧化钇(Y2O3)、氧化锆(ZrO2)为解质,这种电解质在高温熔融状态下允许氧离子(O2-)在其间通过。某甲醇燃料电池的工作原理如右图所示,两个多孔电极均不参与电极反应。下列有关该燃料电池的说法错误的是(已知每摩尔电子所携带的电量为9.65×104C/mol)

A. 该燃料电池的负极反应式为CH3OH-6e-+3O2-=CO2↑+2H2O
B. 若有16g甲醇发生反应,该电池理论上提供的电量最多为2.895×105C
C. 氧气在负极发生还原反应
D. O2-在电解质中的移动方向为:正极![]() 负极
负极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com