
【题目】(1)基态Fe原子有________个未成对电子,Fe3+的电子排布式为 ________。可用硫氰化钾检验Fe3+,形成的配合物的颜色为________。
(2)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍, d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________。
(3)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。
请回答下列问题:
Y基态原子的电子排布式是_____;Z所在周期中第一电离能最大的主族元素是______。
(4)基态硼原子的电子排布式为______。Ga基态原子的核外电子排布式是______。Cu+基态核外电子排布式为________。
【答案】 4 1s22s22p63s23p63d5 血红色 N  1s22s22p4 Cl 1s22s22p1 1s22s22p63s23p63d104s24p1 1s22s22p63s23p63d10
1s22s22p4 Cl 1s22s22p1 1s22s22p63s23p63d104s24p1 1s22s22p63s23p63d10
【解析】(1)基态Fe原子有4个未成对电子,Fe3+的电子排布式为1s22s22p63s23p63d5 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为血红色。
(2)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,则a可能为H元素;b的价电子层中的未成对电子有3个,则b可能为N元素;c的最外层电子数为其内层电子数的3倍,c可能为O元素; d与c同族则d可能为S元素;e的最外层只有1个电子,但次外层有18个电子,则e一定是Cu元素。综合以上信息,a、b、c、d、e分别为H、N、O、S、Cu,所以b、c、d中第一电离能最大的是N,e的价层电子轨道示意图为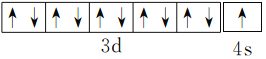 。
。
(3)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3,则X为N元素、Y为O元素。Z基态原子的M层与K层电子数相等,则Z为Mg元素;R2+离子的3d轨道中有9个电子,则R为Cu元素。所以Y基态原子的电子排布式是1s22s22p4;Z所在周期中第一电离能最大的主族元素是Cl。
(4)基态硼原子的电子排布式为1s22s22p1。Ga基态原子的核外电子排布式是1s22s22p63s23p63d104s24p1 。Cu+基态核外电子排布式为1s22s22p63s23p63d10。


科目:高中化学 来源: 题型:
【题目】关于材料的下列说法中正确的是
A. 废旧轮胎均可直接在室外焚烧处理
B. 具有网状结构的酚醛树脂可溶于酒精
C. 复合材料玻璃钢具有强度高、质量轻等优点
D. 合成纤维、人造纤维和光导纤维均为有机高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ) 下列叙述正确的有________
A.第四周期元素中,锰原子价电子层中未成对电子数最多
B.第二周期主族元素的原子半径随核电荷数增大依次减小
C.卤素氢化物中,HCl的沸点最低的原因是其分子间的范德华力最小
D.价层电子对相斥理论中,π键电子对数不计入中心原子的价层电子对数
(Ⅱ)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为_______,晶体中原子间通过_______ 作用形成面心立方密堆积,其中M原子的配位数为______。
(2)元素Y基态原子的核外电子排布式为________,其同周期元素中,第一电离能最大的是______(写元素符号)。元素Y的含氧酸中,酸性最强的是________(写化学式),该酸根离子的立体构型为________。
(3)M与Y形成的一种化合物的立方晶胞如图所示。

①该化合物的化学式为_______,已知晶胞参数a=0.542 nm,此晶体的密度为_______g·cm–3。(写出计算式,不要求计算结果。阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是________。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,最终一定有白色沉淀生成的是( )
①向AlCl3溶液中加入过量的氨水②向Na2SiO3溶液中通入过量的CO2;
③向Ca(OH)2溶液中通入过量CO2;④向CaCl2溶液中通入少量的CO2
A. ①② B. ①③④ C. ①④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的合成是人类科学技术上的一项重大突破。其原理如下:
N2( g) +3H2( g) ![]() 2NH3( g) △H= -92.4kJ/mol
2NH3( g) △H= -92.4kJ/mol
据此回答下列与NH3有关的问题:
(1)该反应的化学平衡常数表达式为K =_________ 。
(2)①500℃时,若把10molN2与20molH2置于体积为10L的密闭容器内,测得容器内压强随时间的变化关系如下表:
压强/MPa | 9.6 | 8.4 | 7.6 | 7.0 | 6.4 | 6.4 | 6.4 | 6.4 |
时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
则从反应开始到平衡这段时间内,v(H2)=_________mol/(L·min)。若达到平衡后,再充人5mol N2与10molH2,再次达到平衡时NH3的体积分数与原平衡状态相比_____(填“增大”“减小”或“不变”)。
②合成氨反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(p1、p2)下随温度变化的曲线,下列图示正确的是_____(填“A”或“B”);比较p1、p2的大小关系:_____________。

③某温度下,在恒压的某密闭容器中投入等物质的量的N2和H2,一段时间后测得H2的体积分数为40%,之后保持不变,则达到平衡时H2的转化率为________________。
(3)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料,与水在一定条件下可以生成氨气:
CO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g) △H = +133.6kJ/mol。关于该反应,下列说法正确的
2NH3(g)+CO2(g) △H = +133.6kJ/mol。关于该反应,下列说法正确的
是______(填序号)。
a.从反应开始到达到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中再加入少量CO(NH2)2,平衡正向移动
c.降低温度使尿素的转化率减小
d.恒温恒容时,向平衡体系中再充人少量氨气,平衡常数减小
(4)将氨气溶于水得到氨水,是一种弱碱。常温下,现将amol/L氨水和0.01mol/L盐酸等体积混合后,溶液中c(NH4+)=c(Cl-),则氨水的Kb=_____________。(用含a的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100ml 1mol/L的AlCl3溶液与100ml 3.5mol/L的NaOH溶液混合,得到沉淀为( )
A. 7.8g B. 0g C. 9.1 g D. 3.9g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加徳罗常数的值。下列说法中不正确的是
A. 0.1mol-NH2(氨基)中所含有的电子数为0.9NA
B. lmol D218O所含的中子数为12NA
C. 14 g聚乙烯与聚丙烯的混合物中含H原子的数目为2NA
D. —定条件下,0.2 mol SO2与足量O2充分反应,生成的SO3分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、材料是人类赖以生存和发展的重要物质基础。
(1)钢筋混凝土是重要的建筑材料,钢筋混凝土______ (填“是”或“不是”)复合材料。
(2)有机玻璃受热时会软化,易于加工成型。有机玻璃是一种_________材料(选填“硅酸盐”或“纤维”或“塑料”)。
Ⅱ.(1)我国汉代器物和秦俑彩绘用的颜料“汉紫”,直到近来人们才研究出来,其成分为紫色的硅酸铜钡(铜为+2价),它的化学式为:BaCuSi2Ox,则x的值为 _________
(2)我国新修订的《环境保护法》,使环境保护有了更严格的法律依据。
①北京和张家口市已成功申办2022年冬奥会,目前北京市政府正在全力改善空气质量,下列指标不在空气质量报告范围内的是________ (填字母)。
SO2浓度 b. CO2浓度 c. 可吸入颗粒物
②废旧电池处理不当易造成重金属污染,治理废水中的重金属污染物可用沉淀法。例如,往含铅(Pb2+)废水中加入Na2S使Pb2+转变为__________ (填化学式)沉淀而除去。
③硝酸型酸雨的形成主要是由汽车排放的尾气所致,汽车尾气中的氮氧化物可以用氨气来处理。例如,氨气与二氧化氮在催化剂作用下反应生成的均是对空气无污染的物质,请写出此时氨气与二氧化氮反应的化学方程式: ______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com