
����Ŀ����³����(���ӽṹ���ϳ���·)���п������ԣ���һ�ֺϳ�·����ͼ��
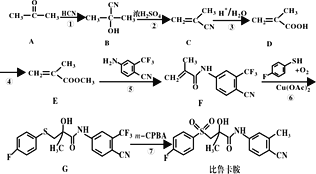
�ش���������
��1��A�Ļ�ѧ����Ϊ__��
��2��D�й����ŵ�������__��
��3����Ӧ�������Լ��������ֱ�Ϊ__��__��
��4��д���ݵķ�Ӧ����ʽ__��
��5��F�ķ���ʽΪ__��
��6��д����E��Ϊͬ���칹�壬�ҷ������������Ļ�����Ľṹ��ʽ__��
�����������������E��ͬ���ں˴Ź�������Ϊ����壬�������Ϊ1��1��6
��7���ο���³�����ϳɵ������Ϣ�������ͼ�ϳ���·(�����Լ���ѡ)___��

���𰸡���ͪ ̼̼˫�����Ȼ� �״� Ũ���ᡢ����  +CH3OH C12H9N2OF3
+CH3OH C12H9N2OF3 ![]()
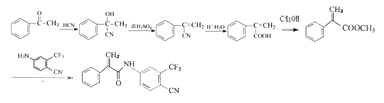
��������
A��HCN�ӳɵõ�B��-H����Oԭ���ϣ�-CN��Cԭ���ϣ�B������ȥ��Ӧ�õ�C��Cˮ��õ�D��E�ͼ״�������Ӧ�õ�E��E����ȡ����Ӧ����F��F�����ӳɡ�������Ӧ����G��G�����ɱ�³������
��1����A�Ľṹ��ʽ��֪��A�ķ���ʽΪ��C3H6O���ʴ�Ϊ��C3H6O��
��2����D�Ľṹ��ʽ��֪��D�к�̼̼˫�����Ȼ����ʴ�Ϊ��̼̼˫�����Ȼ���
��3��D�ͼ״�������Ӧ����E��������Ӧ������ΪŨ���ᡢ���ȣ��ʴ�Ϊ���״���Ũ���ᡢ���ȣ�
��4����ͼ��֪��E�е���������ȡ������F����������Hԭ�������˼״������Է����ķ�ӦΪ�� +CH3OH���ʴ�Ϊ��
+CH3OH���ʴ�Ϊ�� +CH3OH��
+CH3OH��
��5���������ˣ�F�ķ���ʽΪ��C12H9N2OF3���ʴ�Ϊ��C12H9N2OF3��
��6�����������������E��ͬ����һ����̼̼˫�����������˴Ź�������Ϊ����壬�������Ϊ1��1��6�������2������������ȷ���ֲ��ṹ��C-C=C���ڴ˻����ϣ������е��ʻ�ֻ���ܳ�����3��̼�ϣ���ô��ֻ��������һ��̼�ϣ����Է���������ֻ��һ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��7����ϱ��������ϳɲ��յڢݲ���֪��![]() ����
����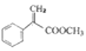 ��
��![]() �ϳɣ�
�ϳɣ�![]() ��
��![]() �ͼ״��ϳɣ�
�ͼ״��ϳɣ�![]() ��
��![]() ˮ�������
ˮ�������![]() ��
��![]() ��ȥ������
��ȥ������![]() ��
��![]() ��HCN�ӳɶ�������������
��HCN�ӳɶ������������� ���ʴ�Ϊ��
���ʴ�Ϊ��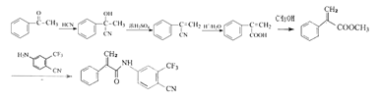 ��
��


 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ�����ʴ��˵����ȷ����(����)
A. �����ڳ�ʪ�����и�ʴ��ʵ����M��nH2O=M(OH)n��![]() H2��
H2��
B. �����Ļ�ѧ��ʴ��ʵ����M��ne��=Mn��������ֱ��ת�Ƹ�������
C. �����Ļ�ѧ��ʴ���������������½���
D. �ڳ�ʪ�Ļ����У������ĵ绯ѧ��ʴһ�������ⸯʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�����������γɵĻ������Ϊ�����������Cu9Al4��Cu5Zn8��PtNi20�ȡ�
��1��ij��������������Է��ԣ�ԭ������ά�ռ�����������������У��ý�������������___�����������������Ǿ������������־���ͷǾ�����ɿ��ķ����ǶԹ������___ʵ�顣
��2��ʵ��֤����PtCl2��NH3��2�Ľṹ�����֣�A���ػ�ɫ���п������ԣ���ˮ�е��ܽ��Ϊ0.258g��B�ʵ���ɫ���������ԣ���ˮ�е��ܽ��Ϊ0.037g�����Ʋ�PtCl2��NH3��2�Ŀռ乹����__��������������������ƽ���ı����������뻭��A�Ľṹͼʾ___��
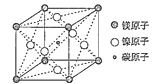
��3���ݱ���ֻ��þ������̼����Ԫ�صľ�����г����ԣ��þ���ľ����ṹ��ͼ��ʾ��д���þ���Ļ�ѧʽ__��������ÿ��þԭ����Χ�����������ԭ����__����
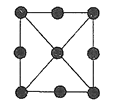
��4����������������Ķ�άͶӰͼ��ͼ��ʾ�������������ܶ�Ϊdgcm-3���谢���ӵ�������ֵΪNA��������a=__pm���г�����ʽ���ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУѧϰС���ͬѧ���ʵ�飬�Ʊ���NH4��2Fe��SO4��26H2O��̽����ֽ���ɡ�ʵ�鲽�����£�
��.��ȡ7.0g��ҵ�����۷����ձ��У������ȵ�Na2CO3��Һϴ�ӣ���ˮϴ�������
��.��ȡ6.0g��������������ۼ���25mLijŨ�������м��ȣ����ȹ����в��ϲ�������ˮ������Ӧ��֡�
��.��ȴ�����˲�ϴ�ӹ��������ۣ������������۵�������
��.��������Һ�м���������NH4��2SO4���壬������������ȫ�ܽ⣬��һϵ�в����ø��﴿���ģ�NH4��2Fe��SO4��26H2O��
V.����NH4��2Fe��SO4��26H2O��ˮ�ã�NH4��2Fe��SO4��2���������ȷֽ�ʵ�顣
��֪�ڲ�ͬ�¶���FeSO47H2O���ܽ�������
�¶ȣ��棩 | 1 | 10 | 30 | 50 |
�ܽ�ȣ�g�� | 14.0 | 17.0 | 25.0 | 33.0 |
�ش��������⣺
��1����������ȵ�Na2CO3��Һϴ�ӹ�ҵ�����۵�Ŀ����__���������������۹�������Ϊ��__�����ȷ�Ӧ�������費�ϲ�������ˮ��Ŀ����__��
��2��������г�����Ӧ��ʣ�����۵���������Ϊ��__��
��3����NH4��2Fe��SO4��2�ֽ����̬���������N2��NH3��SO2��SO3��ˮ������������װ�ü��鲿�ֲ��

�ټ�����̬�����е�SO2��SO3ʱ��װ������˳������Ϊ__�������������ң���C��ʢ�ŵ��Լ�Ϊ__��
��װ��A��������__��
�ۼ����ַֽⲢ��ȴ��Ĵ������������������Ƿ��ж����������õ����Լ�Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�ָ���ȼ�ϡ���֪�����ۼ�����(���ѻ��γ�1mol���ۼ�ʱ���ջ��ͷŵ�����)�����
N��N | O=O | N-N | N-H | O-H | |
����(KJmol��1) | 946 | 497 | 154 | 391 | 463 |
(1)N2H4(g)+O2(g)N2(g)+2H2O(l) H=________KJmol��1 ��
(2)�ܱ������н��з�Ӧ��3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g) H��0��Ӧ�Ļ�ѧƽ�����ʽΪK=________��
Fe3O4(s)+4H2(g) H��0��Ӧ�Ļ�ѧƽ�����ʽΪK=________��
(3)��֪��600��ʱ��������Ӧ��ƽ�ⳣ��K=16��������ͼ��(���º�ѹ)����ͼ��(���º���)��������
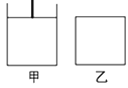
��ʼʱ���±���ʾ�ֱ��������ʣ����Ϊ2L����600��ʱ��Ӧ����һ��ʱ������ƽ�⡣
Fe | H2O(g) | Fe3O4 | H2 | |
��/mol | 2.0 | 1.0 | 2.0 | 0.5 |
��/mol | 2.0 | 2.0 | 2.0 | 1.0 |
�ٹ��ڼס������������з���ȷ����________��
A.��Ӧ��ʼʱ�������ڵ��淴Ӧ���ʣ��ף���
B.����������������ܶȲ��ٱ仯����˵����Ӧ�Ѵﵽƽ��״̬
C.���������������ѹǿ���ٱ仯����˵����Ӧ�Ѵﵽƽ��״̬
D.ƽ�������Fe3O4���������ڵ�ƽ��������ƶ�
��Ͷ�Ϻ��5min��ƽ�⣬��˶�ʱ���ڵ�ƽ����Ӧ����v(H2)=________��
��ƽ���������������ϵ�¶�ͻȻ����100����ͼ��������ȷ��ӳƽ���ƶ������������ڱ仯�������________��
A. 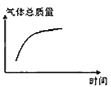 B.
B. 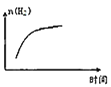 C.
C. 
(4)��ͼΪ���ݾ���������

����������Ӧ����ʼ��ƽ��ʱ�ĸ����ʵ���������
Fe | H2O(g) | Fe3O4 | H2 | |
��ʼ/mol | 3.0 | 3.0 | 0 | 0 |
ƽ��/mol | m | n | p | q |
Fe | H2O(g) | Fe3O4 | H2 | |
A/mol | 3.0 | 3.0 | 0 | 0 |
B/mol | 0 | 0 | 3.0 | 3.0 |
C/mol | m | n | p | q |
���ڴﵽƽ�����������У��ֱ�������A��B��C��������������Ӹ����ʣ����ٴδ�ƽ��ʱ����������H2�İٷֺ������ɴ�С��˳��______(��A��B��C��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǿ���ṹ�п��ظ����ֵ���С�Ľṹ��Ԫ��C60�����ṹ����ͼ��ʾ������˵����ȷ����(����)
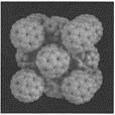
A. C60Ħ��������720
B. C60�뱽��Ϊͬ��������
C. ��C60��������14��C60����
D. ÿ��C60������Χ������������Ⱦ����C60������12��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣�����ÿһ��ŷֱ����һ��Ԫ�ء�
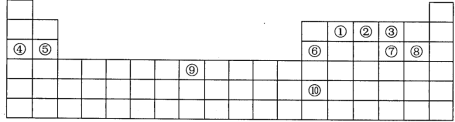
��1��Ԫ�آ�Ԫ��������__��Ԫ�آ�λ��Ԫ�����ڱ�__����
��2��Ԫ�آ�ԭ�ӵļ۵�������__��Ԫ�آ���Ԫ�����ڱ��ĵ������ڵ�__�塣
��3����Ԫ�آ١��ڡ����У��ǽ�������ǿ����__��������Ӧ��Ԫ�ط��ű�ʾ����ͬ������һ������������__��Ԫ�آۡ��ߡ���ļ����ӵİ뾶�ɴ�С��˳��Ϊ__��������ţ���Ҫ���κ����ӷ��ţ���
��4��Ԫ�آ�ĵ��ʿ��ܾ��е�������__������ĸ����
a���ܵ��絼�� b������ϡ���ᷴӦ�������� c���侧�������Ӿ���
��5����Ԫ�آܡ��ݡ�������������У��������Ե���__���ѧʽ����
��Ԫ�آ١��������������ˮ�����У�������ǿ����__���ѧʽ����
��6��Ԫ�آ�ԭ�ӵ���Χ�����Ų�Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ����ͺ���Ԫ�صĻ��ϼ����о��������ʵ�������Ҫ�ӽǣ����仯�������̬�仯Ϊ����Ķ�άת����ϵ��ͼ1��ʾ��
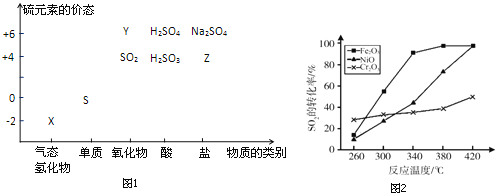
���������գ�
��1��ͼ��X�ĵ���ʽΪ__����ˮ��Һ�ڿ����з����ױ���ǣ�д����Ӧ�Ļ�ѧ����ʽ__���ñ仯˵��S�ķǽ����Ա�O__������ǿ����������������ԭ�ӽṹ�ĽǶȽ���ԭ��__��ͨ��__������������Ҳ�����ж�����������Ԫ�صķǽ�����ǿ����
��2��������������Na2S2O3�Ʊ�����������ԭ��Ӧ�ĽǶȣ��������п��ܵ���__��ѡ���ţ���
a Na2S+S b Z+S c Na2SO3+Y d NaHS+NaHSO3
��3����֪��Ӧ��Na2S2O3+H2SO4��Na2SO4+S��+SO2+H2O���о��䷴Ӧ����ʱ�����з�����������__��ѡ���ţ���
a �ⶨһ��ʱ��������SO2��������ó��÷�Ӧ������
b �о�Ũ�ȡ��¶ȵ����ضԸ÷�Ӧ���ʵ�Ӱ�죬�ȽϷ�Ӧ���ֻ��ǵ�ʱ��
c ��Na2S2O3����ֱ���Ũ��ϡ���ᷴӦ���о�Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ��
��4��������CO��SO2���̵�������Fe2O3����������CO��SO2��380��ʱת��ΪS��һ�������壮��֪��������۵㣺112.8�桢�е㣺444.6�棻�ڷ�Ӧÿ�õ�1mol�ų�270kJ��������д���������̵�����Ӧ���Ȼ�ѧ����ʽ__��
��5������������ͬ��������ͬʱ��������Ӧ��SO2��ת�����淴Ӧ�¶ȵı仯��ͼ2�������Ǵ����۸����أ�������ѡFe2O3����������Ҫԭ����__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������±�ᷴӦ���Ʊ�±��������Ҫ������ʵ�������Ʊ������飨C2H5Br��ͨ���������·���������ƿ�м�NaBr��Լ2-3g��������ˮ�������Ҵ����ټ��������Ҵ������Ũ���ᣨ1��1�������ϴ��г����ܵ����ӣ������ܵ���һ�˲���װ�б�ˮ�������Թ��У��þƾ��Ƹ�ʯ�����Է�Ӧ����ȣ���ͼ��ʾ�����ô�װ��Ҳ���Ʊ�һЩ������±�������磺1-�嶡��ȡ����ܴ��ڵĸ���Ӧ�У�����Ũ����Ĵ�������ˮ����ϩ���ѣ�Br-��Ũ��������ΪBr2�ȡ��й������б����£���ش��������⣺
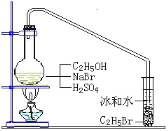
�Ҵ� | ������ | ������ | 1-�嶡�� | |
�ܶ�/gcm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
�е�/�� | 78.5 | 38.4 | 117.2 | 101.6 |
(1)д���÷����Ʊ������飨C2H5Br���Ļ�ѧ����ʽ_____
(2)ͼ�е��Թܷ����ˮ������Ŀ����_____��
(3)�Ʊ������У������Ũ����������ϡ�ͣ�Ŀ����_____��
a�����ٸ�����ϩ���ѵ����� b������Br2������
c������HBr�Ļӷ� d��ˮ�Ƿ�Ӧ�Ĵ���
(4)����ȥ������е���������Br2���������������ʺϵ���_____������ĸ����
a��NaI b��NaOH c��NaHSO3 d��KCl
(5)���Ʊ�������ʱ�����ñ߷�Ӧ����������ķ�������������_____�������Ʊ�1-�嶡��ʱȴ���ܱ߷�Ӧ�����������ԭ����_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com