
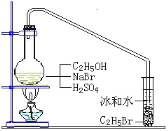
【题目】醇与氢卤酸反应是制备卤代烃的重要方法。实验室中制备溴乙烷(C2H5Br)通常采用以下方法:在烧瓶中加NaBr(约2-3g)、适量水和少量乙醇,再加两倍于乙醇体积的浓硫酸(1:1),塞上带有长导管的塞子,长导管的另一端插入装有冰水混合物的试管中,用酒精灯隔石棉网对反应物加热(如图所示)。用此装置也可制备一些其它的卤代烃,如:1-溴丁烷等。可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下,请回答下列问题:
乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
密度/gcm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
(1)写出该方法制备溴乙烷(C2H5Br)的化学方程式_____
(2)图中的试管放入冰水混合物的目的是_____。
(3)制备操作中,加入的浓硫酸必需进行稀释,目的是_____。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是_____(填字母)。
a.NaI b.NaOH c.NaHSO3 d.KCl
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于_____;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是_____。
【答案】C2H5OH+NaBr+H2SO4(浓)→ NaHSO4+C2H5Br+H2O 冷却、分离除杂 ab c 提高乙醇的利用率 1-溴丁烷与正丁醇的沸点接近
【解析】
制备溴乙烷(C2H5Br)时,浓硫酸先与NaBr反应,生成NaHSO4和HBr,HBr再与C2H5OH反应生成C2H5Br和H2O。由于浓硫酸具有强氧化性,而HBr又具有还原性,容易被浓硫酸进一步氧化为Br2,所以采用1:1的硫酸。溴乙烷的沸点在几种有机物中最低,所以可加热将其蒸出,从而提高乙醇的转化率;蒸出的溴乙烷蒸气需用冰水冷却,否则会随空气逸出,不仅造成浪费,还会污染空气。
(1)该方法中,C2H5OH、NaBr、H2SO4(浓)三者发生反应,生成溴乙烷等,化学方程式为C2H5OH+NaBr+H2SO4(浓)→NaHSO4+C2H5Br+H2O。答案为:C2H5OH+NaBr+H2SO4(浓)→NaHSO4+C2H5Br+H2O;
(2)为防溴乙烷挥发,收集溴乙烷的试管放入冰水混合物,目的是冷却、分离除杂。答案为:冷却、分离除杂;
(3)a.乙醇在浓硫酸的作用下,可以生成乙烯,也可生成乙醚,a符合题意;
b.浓硫酸能将溴化钠氧化,生成Br2,b符合题意;
c.浓硫酸与溴化钠反应生成HBr,与乙醇反应,加热会造成HBr的挥发,浓硫酸与HBr的挥发没有必然联系,c不合题意;
d.此反应为可逆反应,水对此反应不起催化作用,d不合题意;答案为:ab;
(4)a.NaI与Br2反应,生成NaBr和I2,I2溶解在溴代烷中,a不合题意;
b.NaOH不仅能吸收Br2,还会造成溴代烷的水解,b不合题意;
c.NaHSO3溶液能吸收Br2,生成Na2SO4、HBr等,c符合题意;
d.KCl与Br2不发生反应,不能吸收Br2,d不合题意;答案为:c;
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,有利于反应物不断转化为生成物,提高乙醇的利用率;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是1-溴丁烷与正丁醇的沸点接近。答案为:提高乙醇的利用率;1-溴丁烷与正丁醇的沸点接近。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】比鲁卡胺(分子结构见合成线路)是有抗癌活性,其一种合成路线如图:
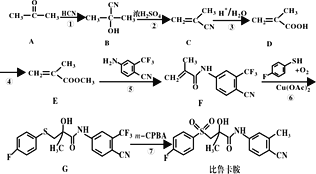
回答下列问题
(1)A的化学名称为__。
(2)D中官能团的名称是__。
(3)反应④所需试剂、条件分别为__、__。
(4)写出⑤的反应方程式__。
(5)F的分子式为__。
(6)写出与E互为同分异构体,且符合下列条件的化合物的结构简式__。
①所含官能团类别与E相同;②核磁共振氢谱为三组峰,峰面积比为1:1:6
(7)参考比鲁卡胺合成的相关信息,完成如图合成线路(其他试剂任选)___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的是可逆反应A+2B![]() 2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
2C+3D的化学反应速率随外界条件改变(先降温后加压)而变化的情况,由此可推断出( )
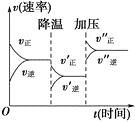
A.该反应的正反应是吸热反应
B.若A,B是气体,则D一定是纯液体或固体
C.该反应的平衡常数始终没变
D.A的转化率最终增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空
(1)打火机、运动会中的火炬一般采用丙烷(C3H8)为燃料。丙烷热值较高,污染较小,是一种优良的燃料。已知一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化如图,请写出表示丙烷燃烧热的热化学方程式:__。
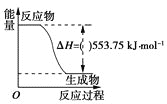
(2)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
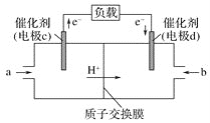
①电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极是__(填“正极”或“负极”),c电极的反应方程式为___。
②用该燃料电池电解1L饱和食盐水(足量),当燃料电池消耗0.56L(标准状况下)氧气时,溶液pH=___(不考虑溶液体积变化)。
(3)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是__,该反应能设计成原电池的原因是__。A是__(填物质名称)。
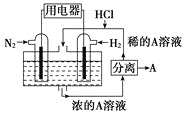
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学常用的酸碱指示剂酚酞的结构简式如图所示,下列关于酚酞的说法错误的是( )
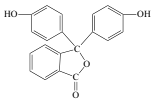
A.酚酞的分子式为C20H14O4
B.酚酞具有弱酸性,且属于芳香族化合物
C.1mol酚酞最多与2molNaOH发生反应
D.酚酞在碱性条件下能够发生水解反应,呈现红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O3是重要的化工原料,易溶于水。在中性或碱性环境中稳定。
I.制备Na2S2O35H2O
反应原理:Na2SO3(aq)+S(s)![]() Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15gNa2S2O3加入圆底烧瓶中,再加入80mL蒸馏水。另取5g研细的硫粉,用3mL乙醇润湿,加入上述溶液中。
②安装实验装置,水浴加热,微沸60分钟。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O35H2O,经过滤,洗涤,干燥,得到产品。
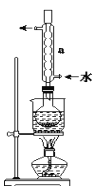
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是___。
(2)仪器a的名称是___,其作用是___。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是___,检验是否存在该杂质的方法是___。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因为___。
II.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol/L碘的标准溶液滴定,反应原理为:2S2O32-+I2=S4O62-+2I-。
(5)滴定至终点时,溶液颜色的变化为___。
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为___ mL。产品的纯度为___(设Na2S2O35H2O相对分子质量为M)。
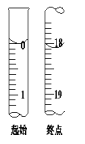
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500mL2mol/LNaOH溶液完全吸收,生成NaNO3和NaNO2的混合溶液,其中生成的NaNO3的物质的量为( )
已知NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH= NaNO3+NaNO2+H2O,
A. 0.2mol B. 0.4mol C. 0.6mol D. 0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠晶体(Na2MoO4.2H2O)是一种无公害型冷却水系统的金属缓蚀剂。工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图所示:
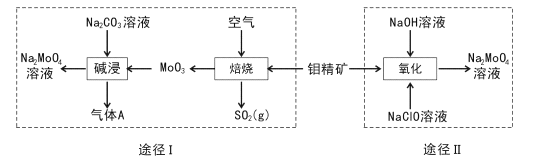
(l) Na2 MoO4![]() 2H2O中钼元素的化合价为____,NaCIO的电子式为 ___。
2H2O中钼元素的化合价为____,NaCIO的电子式为 ___。
(2)途径I为了提高钼精矿焙烧速率,可采取的措施是____(答出两条即可)。
(3)途径I焙烧过程中化学方程式为____,碱浸时气体A的化学式为____。
(4)已知途径I的钼酸钠溶液中c(MoO42-)=0. 40mol/L,c(CO32-)=0. 20mol/L。由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-。当BaMoO4开始沉淀时,CO32-的去除率是____(已知Ksp(BaCO3) =1×10-9、Ksp(BaMo04) =4.0×10-8,忽略溶液的体积变化)。
(5)途径II氧化时溶液中还有Na2SO4生成,则还原剂与氧化剂物质的量之比为_____。
(6)途径I或途径II所得的Na2MoO4溶液经结晶可得固体A后再重结晶可得固体B,其重结晶操作的目的为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨在自然界主要以钨(+6价)酸盐的形式存在。黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO4、MnWO4。黑钨矿冶炼金属钨的流程如下图(已知:钨酸是一种难溶性强酸、对热不稳定)。其中A、B、C都是钨的化合物。完成下列填空:

(1)上述从黑钨矿获得单质钨的过程中属于氧化还原反应的是(填数字序号)__________。
(2)操作①的名称为__________,得到的滤液为钨酸的钠盐,写出反应②的化学方程式______________。该过程中产品C为_________,从产品C获得纯度较高的钨的另一反应原料应该为___________。
(3)若制得的钨中含有少量金属铁,为测定其中金属钨的含量(已知金属钨不溶于盐酸),甲同学用下列装置进行测定:
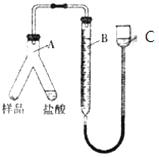
相关实验步骤:
①加好称量好的样品和盐酸,记录B的液面位置;
②检查气密性。
③待A中不再有气体产生并恢复至室温后,记录B的液面位置;
④将A中盐酸与样品混合;
正确的操作顺序是_________________(填序号)
(4)若实验用样品的质量为a g,加入20mL盐酸与之充分反应后,测得排出水的体积为VL(标准状况下),测得的H2的体积应为___________L,样品中的钨的质量分数的计算式为______________。
(5)在读取C装置液面数据时,应先____________,再平视读数,若样品中含有不溶于酸,也不与酸反应的物质,则测得钨的质量分数将_________(填“偏大”、“偏小”或“不受影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com