
【题目】下列属于强碱的是( )
A. Na2CO3B. Na2OC. NH3·H2OD. 氢氧化钙Ca(OH)2
科目:高中化学 来源: 题型:
【题目】一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高.其主要流程如下.请回答下列问题: 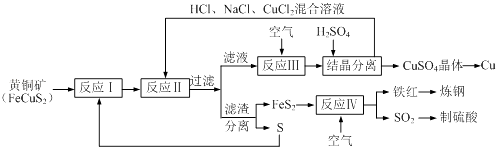
(1)反应Ⅲ的离子方程式为4CuCl2﹣+O2+4H+═4Cu2++8Cl﹣+2H2O,CuCl2﹣中铜元素的化合价为 , 该反应中的氧化剂是 .
(2)一定温度下,在反应Ⅲ所得的溶液中加入硫酸,可以析出硫酸铜晶体而不析出氯化铜晶体,其原因可能是 .
(3)炼钢时,可将铁红投入熔融的生铁中,以降低生铁的含碳量,该过程中主要反应的化学方程式是 .
(4)SO2尾气直接排放到大气中造成环境污染的后果是 .
(5)已知反应Ⅱ的离子方程式为Cu2++CuS+4Cl﹣═2CuCl2﹣+S,反应Ⅰ的产物为和 . (填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温高压下,1L密闭容器中,发生如下反应:2H2+COCH3OH.反应开始时H2的物质的量为5mol,5min时变为0.5mol,则5min内该反应的平均反应速率v(H2)(单位:molL﹣1min﹣1)为( )
A.9.0
B.0.9
C.0.45
D.4.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 已知冰的熔化热为6.0kJ·mol-1,冰中氢键键能为20kJmol-1,假设每摩尔冰中有2mol氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键
B. 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为a,Ka=(ca)2/c(1-a)。若加水稀释,,则CH3COOH![]() CH3COO-+H+向右移动,a增大,Ka不变
CH3COO-+H+向右移动,a增大,Ka不变
C. 甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1
D. 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示。

(1)在0~30小时内,CH4的平均生成速率vⅠ、vⅡ和vⅢ从大到小的顺序为________;反应开始后的12小时内,在第________种催化剂作用下,收集的CH4最多。
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g)。该反应ΔH=+206 kJ·mol-1。
CO(g)+3H2(g)。该反应ΔH=+206 kJ·mol-1。
①画出反应过程中体系能量变化图(进行必要标注)。
②将等物质的量的CH4和H2O(g)充入1 L恒容密闭反应器,某温度下反应达平衡,平衡常数K=27,此时测得CO的物质的量为0.10 mol,求得CH4的平衡转化率为____________(计算结果保留两位有效数字)。
(3)已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-802 kJ·mol-1
写出由CO2生成CO的热化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在强酸性溶液中可以大量共存的是
A. Mg2+ 、Fe3+ 、SCN-、 Cl- B. Na+、K+、NO3- Ba2+
C. Na+ 、AlO2- 、HCO3- 、SO42- D. Fe2+ 、I- 、NO3- 、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是元素周期表的一部分,根据所给的10种元素,完成以下各小题.
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | C | N | O | Ne | ||||
3 | Na | Mg | Al | Si | S | Cl |
(1)镁的原子结构示意图为 .
(2)H2SO4与HClO4中,酸性较强的是 .
(3)NaOH与Al(OH)3中,属于两性氢氧化物的是 , 它常用作治疗胃酸(含盐酸)过多的药物,该反应的化学方程式为 .
(4)碳元素形成的一种氧化物的化学式是 , 该物质中C元素与O元素的质量比为 . (相对原子质量:C﹣12 O﹣16)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列两个热化学方程式2H2(g)+O2(g)=2H2O(1) ΔH=-571.6kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2220kJmol-1
实验测得氢气和丙烷的混合气体共0.5mol,完全燃烧时放出热量723.2kJ,则混合气体中氢气和丙烷的体积比约为
A. 2:3 B. 1:3 C. 3:2 D. 3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com