
����Ŀ������Ԫ�����ڱ���һ���֣�����������10��Ԫ�أ�������¸�С�⣮
�� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
2 | C | N | O | Ne | ||||
3 | Na | Mg | Al | Si | S | Cl |
��1��þ��ԭ�ӽṹʾ��ͼΪ ��
��2��H2SO4��HClO4�У����Խ�ǿ���� ��
��3��NaOH��Al��OH��3�У�������������������� �� ������������θ�ᣨ�����ᣩ�����ҩ��÷�Ӧ�Ļ�ѧ����ʽΪ ��
��4��̼Ԫ���γɵ�һ��������Ļ�ѧʽ�� �� ��������CԪ����OԪ�ص�������Ϊ �� �����ԭ��������C��12 O��16��
���𰸡�
��1��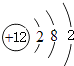
��2��HClO4
��3��Al��OH��3��Al��OH��3+3HCl�TAlCl3+3H2O
��4��CO��CO2��3��4��3��8
���������⣺��1��Mgԭ�Ӻ�����12�����ӣ���3�����Ӳ㣬���������Ϊ2��8��2��ԭ�ӽṹʾ��ͼΪ�� 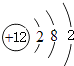 �����Դ��ǣ�
�����Դ��ǣ� 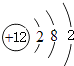 ����2��ͬ�����������Ԫ�طǽ����Լ������ʷǽ�����S��Cl��Ԫ�طǽ�����Խǿ��������������Ӧˮ���������Խǿ��������HClO4��H2SO4 ��
����2��ͬ�����������Ԫ�طǽ����Լ������ʷǽ�����S��Cl��Ԫ�طǽ�����Խǿ��������������Ӧˮ���������Խǿ��������HClO4��H2SO4 ��
���Դ��ǣ�HClO4����3�������������������������θ����Ҫ�ɷ�Ϊ���ᣬ�������������ᷴӦ�����Ȼ�����ˮ����Ӧ��ѧ����ʽΪ��Al��OH��3+3HCl�TAlCl3+3H2O��
���Դ��ǣ�Al��OH��3��Al��OH��3+3HCl�TAlCl3+3H2O����4��̼��������ΪCO��CO2 �� �ɻ�ѧʽ��֪C��OԪ������֮��=12��16=3��4��C��OԪ��֮��=12��32=3��8��
���Դ��ǣ�CO��CO2��3��4��3��8��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫϡ��ҺX�У����ܺ���������������е�ij���֡�
������ | CO |
������ | Al3����Fe3����Mg2����NH |
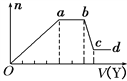
ȡ����Һ�����������м���ij�Լ�Y���������������ʵ���(n)������Լ����(V)�Ĺ�ϵ��ͼ��ʾ��
��1����Y�����ᣬ����Һ�к��е���������______ ��ab�η�����Ӧ�������ӷ���ʽΪ____________, Oa���ϱ��вμӷ�Ӧ�����ӵ����ʵ���֮��Ϊ________________________��
[Ҫ�������ӷ��ţ���n��Fe3+��]��
��2����Y��NaOH��Һ����X��һ�������ϱ��е�������________________________�����ǵ����Ӹ�����Ϊ______________________________��[����������ǰ���������ں���ǰ���ͼ��ں��˳������]��ab�η�Ӧ�����ӷ���ʽΪ______________________________�� bc�η�Ӧ�����ӷ���ʽΪ____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���������ϸ���е����õ��������������
A. ��ijЩ���ӻ��������Ҫ�ɷ�
B. ��ϸ���е���Դ����֮һ
C. ����������������
D. ��ά��ϸ������̬����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ǿ����ǣ� ��
A. Na2CO3B. Na2OC. NH3��H2OD. ��������Ca(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�����з�Ӧ����ʽ��
��1��ʵ������������
��2��������������������Һ�ķ�Ӧ��
��3��ͭ��ϡ����ķ�Ӧ��
��4��̼��Ũ����ķ�Ӧ��
��5��ͭͶ�����Ȼ�����Һ�У� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��500mL KNO3��Cu(NO3)2�Ļ����Һ��c(NO3-)=6.0mol/L����ʯī���缫������Һ����ͨ��һ��ʱ������������ռ���22.4L��������״��������Һ������仯���Բ��ƣ�����˵����ȷ����
A. ԭ�����Һ��n(K��)Ϊ2 mol B. �����������й�ת��4 mol����
C. ���õ���Cu�����ʵ���Ϊ0.5 mol D. ������Һ��c(H+)Ϊ2 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ǰЩ���ҹ����ϡ����ݵȵ��������˰��꺱���ĸɺ������ʹ���衰��ˮ�͡������鰸�ٴ������ճ̡����й���ˮ����������ȷ���� ( )
A. ���ˮ��ϸ������Ҫ��ɳɷ� B. ѪҺϸ���е�ˮ��������ˮ
C. ����ϸ���ڵ�ˮ���ǽ��ˮ D. ����ˮ�ɲ���ϸ�������ʵ�����ͻ�ѧ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�������ijЩ������˵�����ı仯��ϵ�����и������в�����ͼʾ��ϵ���ǣ� �� 
A.��ԭ��
B.��ˮ��Ӧ�ľ��ҳ̶�
C.�۵�
D.ԭ�Ӱ뾶
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������п����VmLŨ��Ϊ10%��ϡ���ᷴӦ��ȡ����������Ӧ������м����������ʣ����ڷ�Ӧ����v˵����ȷ����
A. ����Na2SO4���壬v(H2)��С B. VmLBaCl2��Һ��v(H2)����
C. ����ϸС��̼����v(H2)���� D. ����NH4HSO4���壬v(H2)����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com