
����Ŀ������Ϊһ�����˲������汻���ӣ���ԭ���ܡ�����������������Լ�ұ��ҵ�в���ȱ�ٵı�����ϡ��뼰�仯��������ж��ԡ���ͼ����һ���Ѿ�Ԥ������ĺ��������ʯ(��Ҫ����![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��)Ϊԭ����ȡ������Ĺ������̣�
��)Ϊԭ����ȡ������Ĺ������̣�
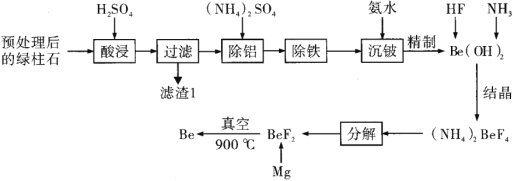
��֪��i.������Ļ�ѧ�������ƣ�
ii.�Ȼ���������̬ʱ���ѵ��룻
iii.Be(OH)2��![]() ʱ���ܽ⣻
ʱ���ܽ⣻
iV.![]() ��
��
(1)����1����Ҫ�ɷ���________��
(2)������������������������立�![]() ����ʽ��������˹�����������立��Ļ�ѧ����ʽΪ________��
����ʽ��������˹�����������立��Ļ�ѧ����ʽΪ________��
(3)������������Ҫ�������µ����ʣ������ӦΪ________��
(4)���������������У�����Ϊ���������![]() ��Һ������Ĵ�����ʽ��________(�����ӷ���)��
��Һ������Ĵ�����ʽ��________(�����ӷ���)��
(5)�����ֽ��������в�����![]() �����ᷢ����Ӧ��
�����ᷢ����Ӧ��![]() ������
������![]() ����
����![]() ���ڵ�̲�������Ӧ��������
���ڵ�̲�������Ӧ��������![]() ���ɣ���д���˷�Ӧ�Ļ�ѧ����ʽ��________��
���ɣ���д���˷�Ӧ�Ļ�ѧ����ʽ��________��
(6)�����в��÷�����þ�Ȼ�ԭ����ȡ����Ҫ��ջ�����ԭ����________���Ȼ������ε�ⷨҲ������ȡ�룬�����ڵ���������Ҫ���������![]() ������
������![]() ��������________��
��������________��
(7)��ͭ��������õĵ����ԡ������ԡ���ʴ�ԡ����ȳ�����Լ����ԡ������Զ���Ϊ��Ϊ�㷺ʹ�õ�һ����Ͻ�������ʯ��![]() �ĺ���Ϊa%����������������
�ĺ���Ϊa%����������������![]() �IJ���Ϊb%����1t����ʯ�����Ͽ���������2%Be����ͭ�Ͻ�________t��
�IJ���Ϊb%����1t����ʯ�����Ͽ���������2%Be����ͭ�Ͻ�________t��
(8)���������в����ĺ���![]() �ķ�ˮ������ʯ���к��������ᄏ�������о�������ͬ��pHֵ���¶��£�ʯ���к��������ᄏ������������Һ�е����Ũ����ͼ��ʾ����Ϊ�˼�����Ⱦ����Ӧѡ�õ�pH��Χ���¶ȷֱ���________(�����)��
�ķ�ˮ������ʯ���к��������ᄏ�������о�������ͬ��pHֵ���¶��£�ʯ���к��������ᄏ������������Һ�е����Ũ����ͼ��ʾ����Ϊ�˼�����Ⱦ����Ӧѡ�õ�pH��Χ���¶ȷֱ���________(�����)��
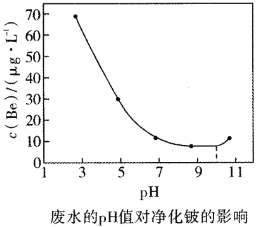
A.9~11��30�� B.7~10��30�� C.8~11��35��
���𰸡�SiO2 (NH4)2SO4+Al2(SO4)3+24H2O=2[(NH4)Al(SO4)2��12H2O] ����Һ�м�������H2O2���ټ�������ˮ������pH��3 BeO22- SiO2+4NH4HF2=SiF4��+4NH4F+2H2O ��ֹBe��Mg������ ��ǿ�����εĵ����� 1.8��10-3ab B
��������
��ϡ�����ܽ⺬�������ʯ������BeO��Al2O3��Fe2O3��FeO���������ᣬ��SiO2���������Ҳ�����ˮ�������ˣ�������ΪSiO2������Һ����Ҫ����Be2+��Al3+��Fe3+��Fe2+���������ᣬ��Һ�м���(NH4)2SO4����立�[(NH4)Al(SO4)2��12H2O]�������������˳�ȥ���ﵽ������Ŀ�ģ�������������Һ�м����������H2O2����Fe2+���ټ�������ˮ������pH��ʹ��Һ��Fe3+��ȫת��ΪFe(OH)3�������ٹ��˳�ȥ���ﵽ������Ŀ�ģ�������Һ�м��백ˮ��HF���õ�(NH4)2BeF4�����·ֽ�õ�BeF2������þ�ڸ����·�Ӧ����Be���Դ˽����⡣
(1)�ɷ���֪������1����Ҫ�ɷ���SiO2��
(2) ��Al3+����Һ�м���(NH4)2SO4����立�[(NH4)Al(SO4)2��12H2O]������������Ӧ�Ļ�ѧ����ʽΪ(NH4)2SO4+Al2(SO4)3+24H2O=2[(NH4)Al(SO4)2��12H2O]��
(3)��֪![]() ����c(Fe3+)=1��10-5mol/Lʱ��c(OH-)=
����c(Fe3+)=1��10-5mol/Lʱ��c(OH-)=![]() mol/L=1��10-11mol/L����ʱ��ҺpH=3����������������Ҫ��������Fe2+���ٵ�����ҺpH��3��ʹFe3+��ȫת��ΪFe(OH)3�������ڲ������µ����ʵ�ǰ���£���ȷ����ӦΪ����Һ�м�������H2O2���ټ�������ˮ������pH��3��
mol/L=1��10-11mol/L����ʱ��ҺpH=3����������������Ҫ��������Fe2+���ٵ�����ҺpH��3��ʹFe3+��ȫת��ΪFe(OH)3�������ڲ������µ����ʵ�ǰ���£���ȷ����ӦΪ����Һ�м�������H2O2���ټ�������ˮ������pH��3��
(4) Be(OH)2������NaOH��Һ���� �������������У������������![]() ��Һ��Be(OH)2������NaOH����NaBeO2������Ĵ�����ʽ��BeO22-��
��Һ��Be(OH)2������NaOH����NaBeO2������Ĵ�����ʽ��BeO22-��
(5) ��![]() ����
����![]() ���ڵ�̲�������SiO2����NH4HF2��Ӧ����SiF4��NH4F��������Ӧ�Ļ�ѧ����ʽΪSiO2+4NH4HF2=SiF4��+4NH4F+2H2O��
���ڵ�̲�������SiO2����NH4HF2��Ӧ����SiF4��NH4F��������Ӧ�Ļ�ѧ����ʽΪSiO2+4NH4HF2=SiF4��+4NH4F+2H2O��
(6)Be��Mg���ڿ����б���������������÷�����þ�Ȼ�ԭ����ȡ����Ҫ��ջ������ﵽ��ֹBe��Mg��������Ŀ�ģ��Ȼ���������̬ʱ���ѵ��룬�ڵ���������Ҫ���������NaCl������ǿ�����εĵ����ԣ�
(7)����ԭ���غ㣬������֪����1t������ʯ������������������2%�Ķ�̨ͭ��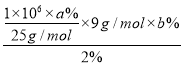 =1.8��103abg=1.8��10-3abt��
=1.8��103abg=1.8��10-3abt��
(8)����ҺpH��7~10���ҡ��¶�30��ʱ��Һ��c(Be)��ͣ�������Ч����ã��ʴ�ΪB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����ͬŨ�ȵ�NaOH��Һ�ֱ�ζ�20.00mLŨ�Ⱦ�Ϊ0.1mol��L-1�������ᣨHA��HB��HC����Һ���ζ���������ͼ��ʾ�������ж�����ȷ����
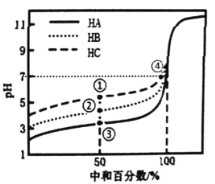
A.���кͰٷ�����50%ʱ��![]()
B.�ζ����ٵ�ʱ����Һ�У�![]()
C.���кͰٷ�����100%ʱ�����ĵ�NaOH��Һ���![]()
D.�ٺ͢���ʾ��Һ�ж��У�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ѿ��ﵽƽ��ķ�Ӧ 2X(g)+Y(g)![]() 2Z(g) ��H<0 ������˵����ȷ���ǣ� ��
2Z(g) ��H<0 ������˵����ȷ���ǣ� ��
A.��С��������������淴Ӧ���ʶ�����ƽ�����淴Ӧ�����ƶ�
B.���߷�Ӧ�¶ȣ��÷�Ӧ��ƽ�ⳣ������
C.�ı�����ʹƽ�������ƶ�����Ӧ���ת����һ��������
D.������������Խ��ͷ�Ӧ����Ļ�ܣ������ı䷴Ӧ����H
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����ʵ���Ũ������˵����ȷ����
A.����ʱ��ֱ�Ӽ�ˮ���̶��ߣ�����Һ����̶�������ʱ��ֹͣ��ˮ
B.������ƿ��ת��Һ��ǰ����ƿδ��ɣ�����õ�Ũ��ƫ��
C.����һ�����ʵ���Ũ�ȵ�����������Һ����Һʱδ��ȴ������õ�Ũ��ƫ��
D.����һ�����ʵ���Ũ�ȵ�������Һ����ȡŨ����ʱ���Ӷ���������õ�Ũ��ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2����Ȼ��̼ѭ���е���Ҫ���ʡ����й��̻����������CO2������������
A. ������� B. ��Ȼ����
C. ��ʯȼ�ϵ�ȼ�� D. ̼���εij���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���к��ȵIJⶨʵ������ͼ����
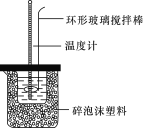
��1����ȡ��Ӧ��ʱ��ȡ50 mL 0.50 mol��L��1�����ᣬ��Ӧ������Լ���________�����������
A��50mL0.50mol��L��1NaOH��Һ
B��50mL0.55mol��L��1NaOH��Һ
C��1.0gNaOH����
��2����ʵ������У���ͬѧ��Ҫ�ⶨ����¼��ʵ��������_____________�����������
A�������Ũ��
B��������¶�
C������������Һ��Ũ��
D������������Һ���¶�
E��ˮ�ı�����
F����Һ��Ϻ������¶�
��3������50 mL 0.5 mol��L��1������Һ������������ⶨ�к��ȣ���������_____________������ƫ��������ƫС����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ���(BCl3)��һ����Ҫ�Ļ���ԭ�ϡ�ijʵ��С�����ø��������������װ��(װ�ÿ��ظ�ʹ��)�Ʊ�BCl3����֤��Ӧ����CO���ɡ�
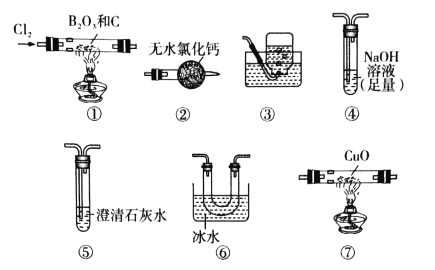
��֪��i.ʵ�����Ʊ�BCl3�Ļ�ѧ����ʽΪ��B2O3+3C+3Cl2![]() 2BCl3+3CO��
2BCl3+3CO��
ii.BCl3���۵�Ϊ-107.3�棬�е�Ϊ12.5�棬��ˮˮ������H3BO3��HCl������˵������ȷ����
A.ʵ��װ�ú���������˳��Ϊ�٢ޢܢڢߢݢ�
B.װ�â��з�����Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O
C.װ�â��������������ռ�BCl3
D.��֤��CO���ɵ�������װ�â���CuO�ɺ�ɫ��ɺ�ɫ����װ�â��г���ʯ��ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ��ԭ�Ϻͻ����Լ���������״��ϳɼ��Ĵ��������¡�����˵��������ȷ����
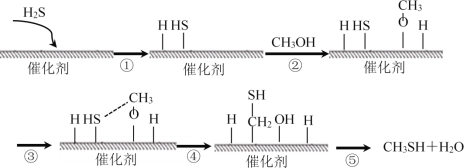
A.CH3SH��̼Ԫ�ػ��ϼ�Ϊ��2��
B.���̢��У��γ���O��H����C��H��
C.�ô�������Ч��߷�Ӧ���ƽ��ת����
D.������״��ϳɼ��ķ�Ӧ����Ϊȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��K��Al��Cu��H��C��O��S��Cl�dz����İ���Ԫ�ء�
(1)������[KAl(SO4)2��12H2O]�Ʊ� Al��K2SO4��H2SO4�Ĺ�������ͼ��ʾ��
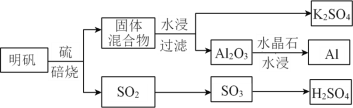
���������Ļ�ѧ����ʽΪ_________________________________________________��
(2)Kλ��Ԫ�����ڱ���________���ڵ�________�塣
(3)S�Ļ�̬ԭ�Ӻ�����________��δ�ɶԵ��ӣ�Cl�Ļ�̬ԭ�Ӻ�������Ų�ʽΪ____________��
(4)�á�����������գ�
��һ������ | ���Ӱ뾶 | �۵� | ���� |
O____S | Cl��____K�� | KCl____Al2O3 | H2SO4____HClO4 |
(5)SO2�ļ۲���ӶԸ�����________���÷���Ϊ�ṹΪ________��SO3����ԭ�Ӳ����ӻ���ʽΪ___________��
(6)���Ʊ���Cu(OH)2�ɽ���ȩ���������ᣬ��������ԭ��Cu2O������ķе����Ը�����ȩ������Ҫԭ����____________________��Cu2OΪ�뵼����ϣ��������������ڲ���4����ԭ�ӣ�������ԭ��λ�����ĺͶ��㣬��þ�������________��ͭԭ�ӡ�
(7)Al����Ϊ�����������壬�侧������a=0.405 nm����ʽ��ʾAl���ʵ��ܶ�__________g��cm��3(�г�����ʽ�ӣ����ؼ�������)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com