
| A、Ba(OH)2溶液与过量的NaHCO3溶液混合:Ba2++OH-+HCO3-=BaCO3↓+H2O |
| B、次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| C、金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| D、氯气通入水中:Cl2+H2O=Cl-+ClO-+2H+ |


科目:高中化学 来源: 题型:
| A、Fe(SCN)3溶液中存在Fe3++3SCN- Fe(SCN)3,向此溶液中加入固体KSCN后颜色变深 |
| B、用通过盛饱和食盐水的洗气瓶来除去氯气中的少量HCl气体杂质 |
| C、反应CO(g)+NO2(g)?CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
| D、合成氨:N2(g)+3H2(g)?2NH3 (g)△H<0在高温、高压和催化剂条件下进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤燃烧时将部分化学能转化为热能 |
| B、镁条燃烧时将部分化学能转化为光能 |
| C、TNT爆炸时将部分化学能转化为动能 |
| D、电解熔融Al2O3时将部分化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液与稀硫酸混合:Ba2++SO42-═BaSO4↓ |
| B、铁片插入稀硫酸溶中:2Fe+6H+═2Fe3++3H2↑ |
| C、稀盐酸滴在大理石上:CO32-+2H+═CO2↑+H2O |
| D、铁片插入硫酸铜溶液中:Fe+Cu2+═Fe2++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜与稀硝酸的反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| B、氯气与水反应:Cl2+H2O=H++Cl-+HClO |
| C、铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、钠和水反应:2Na+H2O=2Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,20 g重水(D2O)中含有的电子数为10NA |
| B、乙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |
| C、22.4 L的N2的共用电子对数为3NA |
| D、78gNa2O2固体中含有的阴离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2+Na2CO3+H2O=2NaHCO3 |
| B、Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO |
| C、2CO2+2Na2O2=2Na2CO3+O2 |
| D、SiO2+CaO=CaSiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
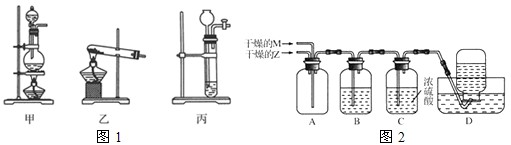
| n(Z) |
| n(M) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com