
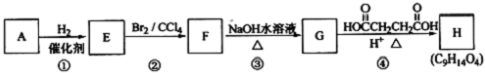
| y |
| 4 |
| 2×5+2-8 |
| 2 |
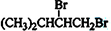 ,F和氢氧化钠的水溶液发生取代反应生成G,G的结构简式为
,F和氢氧化钠的水溶液发生取代反应生成G,G的结构简式为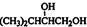 ,G和与
,G和与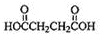 发生酯化反应生成H,结合H的分子式可知H为:
发生酯化反应生成H,结合H的分子式可知H为: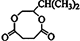 ,据此解答.
,据此解答.| y |
| 4 |
| 2×5+2-8 |
| 2 |
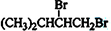 ,F和氢氧化钠的水溶液发生取代反应生成G,G的结构简式为
,F和氢氧化钠的水溶液发生取代反应生成G,G的结构简式为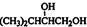 ,G和与
,G和与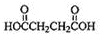 发生酯化反应生成H,结合H的分子式可知H为:
发生酯化反应生成H,结合H的分子式可知H为: ,
,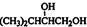 与足量的金属钠反应能生成氢气1mol,标况下氢气体积为1mol×22.4L/mol=22.4,由G转化为H的化学方程式是:
与足量的金属钠反应能生成氢气1mol,标况下氢气体积为1mol×22.4L/mol=22.4,由G转化为H的化学方程式是: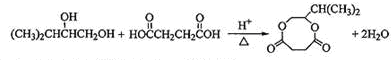 ,
,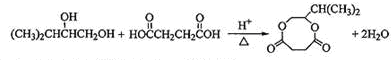 ,;
,;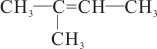 、
、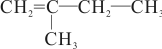 ,
,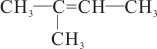 、
、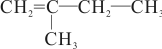 .
.


科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| H2O/H+ |
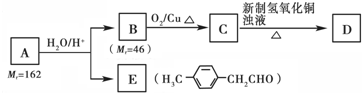
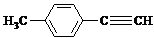 )的一条路线如下:
)的一条路线如下: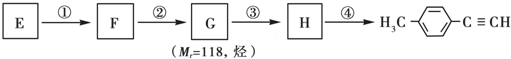
查看答案和解析>>
科目:高中化学 来源: 题型:
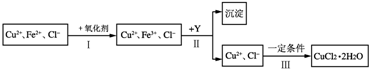
查看答案和解析>>
科目:高中化学 来源: 题型:
| n(H2O) |
| n(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 装置 | 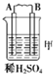 | 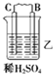 | 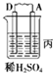 |
| 现象 | 二价金属A不断溶解 | C极质量增加 | A上有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
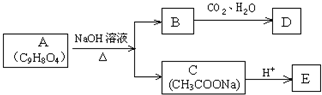
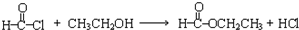 ,写出草酰氯(结构式:
,写出草酰氯(结构式: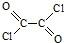 )与足量有机物D反应的化学方程式:
)与足量有机物D反应的化学方程式: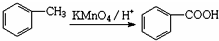 ,由邻甲基苯酚经过两步反应可生成有机物A:邻甲基苯酚→中间产物→有机物A,请写出“中间产物”的结构简式
,由邻甲基苯酚经过两步反应可生成有机物A:邻甲基苯酚→中间产物→有机物A,请写出“中间产物”的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com