
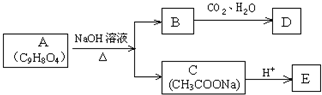
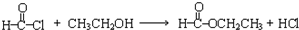 ,写出草酰氯(结构式:
,写出草酰氯(结构式: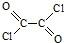 )与足量有机物D反应的化学方程式:
)与足量有机物D反应的化学方程式: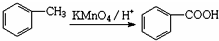 ,由邻甲基苯酚经过两步反应可生成有机物A:邻甲基苯酚→中间产物→有机物A,请写出“中间产物”的结构简式
,由邻甲基苯酚经过两步反应可生成有机物A:邻甲基苯酚→中间产物→有机物A,请写出“中间产物”的结构简式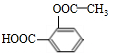 ,故B结构简式为
,故B结构简式为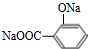 ,B溶液中通入气体CO2生成D,D不能与NaHCO3溶液反应,但能与NaOH溶液反应,则D中有酚羟基并无羧基,故D为
,B溶液中通入气体CO2生成D,D不能与NaHCO3溶液反应,但能与NaOH溶液反应,则D中有酚羟基并无羧基,故D为 ,C酸化得到E为CH3COOH,据此解答.
,C酸化得到E为CH3COOH,据此解答. ,故B结构简式为
,故B结构简式为 ,B溶液中通入气体CO2生成D,D不能与NaHCO3溶液反应,但能与NaOH溶液反应,则D中有酚羟基并无羧基,故D为
,B溶液中通入气体CO2生成D,D不能与NaHCO3溶液反应,但能与NaOH溶液反应,则D中有酚羟基并无羧基,故D为 ,C酸化得到E为CH3COOH,
,C酸化得到E为CH3COOH, ,故答案为:
,故答案为: ;
;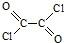 )与D中酚羟基发生取代反应会生成HCl,HCl与-COONa反应得到-COOH,故草酰氯足量有机物D反应的化学方程式为:
)与D中酚羟基发生取代反应会生成HCl,HCl与-COONa反应得到-COOH,故草酰氯足量有机物D反应的化学方程式为: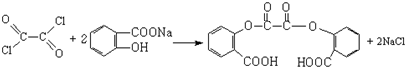 ,
, ;
;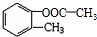 ,再用酸性高锰酸钾氧化得到A,故答案为:
,再用酸性高锰酸钾氧化得到A,故答案为: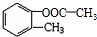 ;
;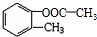 )有多种同分异构体,符合下列条件的结构简式:③能发生银镜反应,含有醛基;④含有羟基,但遇FeCl3溶液不发生显色反应,含有醇羟基,①苯环上有两个侧链; ②苯环上的一氯代物只有两种,两个侧链处于对位,符合条件的同分异构体有:
)有多种同分异构体,符合下列条件的结构简式:③能发生银镜反应,含有醛基;④含有羟基,但遇FeCl3溶液不发生显色反应,含有醇羟基,①苯环上有两个侧链; ②苯环上的一氯代物只有两种,两个侧链处于对位,符合条件的同分异构体有: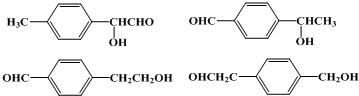 ,
,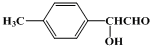 、
、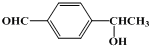 等.
等.


科目:高中化学 来源: 题型:
| A、标准状况下,20 g重水(D2O)中含有的电子数为10NA |
| B、乙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |
| C、22.4 L的N2的共用电子对数为3NA |
| D、78gNa2O2固体中含有的阴离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高价氧化物的对应水化物是一种强酸;Z的非金属性在同周期主族元素中最强.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高价氧化物的对应水化物是一种强酸;Z的非金属性在同周期主族元素中最强.查看答案和解析>>
科目:高中化学 来源: 题型:
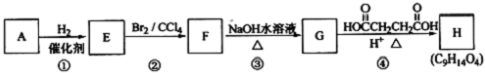
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 氯气 |
| 热空气或 |
| 水蒸气 |
| 碱液 |
| 吸收 |
| 酸化 |
| 蒸馏 |
| 煅烧 |
| 水 |
| 海水 |
| 过滤 |
| 灼烧 |
| 熔化 |
| 电解 |
| 放电 |
| 水 |
| 吸收 |
| 一定 |
| 条件下 |
| 合成塔 |
| 过量氮气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
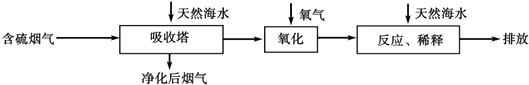
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | 最高价氧化物对应的水化物化学式为H2XO3 |
| Y | 最外层电子数是次外层的3倍 |
| Z | 短周期元素中原子半径最大的主族元素 |
| W | 一种核素的质量数为28,中子数为14 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com