
【题目】合成气(CO+H2)可利用甲烷与水蒸气重整反应制得。
(1)已知:①H2(g)+![]() O2(g)=H2O(g) △H1=-242kJmol-1
O2(g)=H2O(g) △H1=-242kJmol-1
②2CO(g)+O2(g)=2CO2(g) △H2=-576kJmol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3=-802.6KJmo1-1
则甲烷和水蒸气重整反应CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H4=____。该反应的活化能E1=240.1kJmol-1,则逆反应的活化能E2=____。
CO(g)+3H2(g)△H4=____。该反应的活化能E1=240.1kJmol-1,则逆反应的活化能E2=____。
(2)重整反应中CH4的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图1所示。
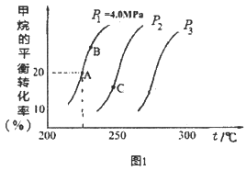
①图中A点的平衡常数KP=___(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),比较A、B、C三点的平衡常数Kp(A)、KP(B)、KP(C)由大到小的顺序为___。
②图中压强P1、P2、P3由大到小的顺序为___,理由是____。
(3)在恒容密闭容器中充入2mol的CH4和H2O(曲混合气体,且CH4和H2O(g)的物质的量之比为x,相同温度下测得H2平衡产率与x的关系如图2所示。请比较a、b两点CH4的转化率a点___b点(填“>”、“<”、“=”下同),a点c(CH4)___b点c[H2O(g)]。当x=1时,下列叙述正确的是____(填序号)。
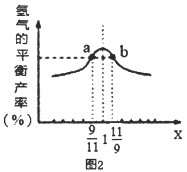
A.平衡常数K最大 B.CH4的转化率最大
C.氢气的产率最大 D.合成气的浓度最大
【答案】+211.4kJmol-1 28.7kJmol-1 ![]() Kp(C)>Kp(B)>Kp(A) P3>P2>P1 其他条件不变时,压强增大,平衡左移,甲烷的转化率减小 > = CD
Kp(C)>Kp(B)>Kp(A) P3>P2>P1 其他条件不变时,压强增大,平衡左移,甲烷的转化率减小 > = CD
【解析】
(1)根据盖斯定律计算;正反应为吸热反应,正反应活化能等于逆反应活化能与反应热之和;
(2)用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,平衡常数Kp等于生成物分压幂之积与反应物分压幂之积比值;
反应CH4(g)+H2O(g)CO(g)+3H2(g)为放热反应,温度越高,平衡常数越大;
②CH4(g)+H2O(g)CO(g)+3H2(g)是气体体积增大的反应,由图知温度不变时压强P1、P2、P3下甲烷转化率逐渐减小;
(3)两种反应物存在,增加其中一种反应物的量,能使另一种反应物的转化率提高。
(1)(1)已知:①H2(g)+O2(g)=H2O(g)△H1=-242kJmol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-576kJmol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H3=-802.6KJmo1-1
由③-①×3-②×得CH4(g)+H2O(g)CO(g)+3H2(g)△H4=△H3-△H1×3-△H2×=+211.4kJmol-1。
正反应活化能等于逆反应活化能与反应热之和,逆反应的活化能E2=E1-△H4=240.1kJmol-1-211.4kJmol-1=28.7kJmol-1,故答案为:+211.4kJmol-1;28.7kJmol-1;
(2)①假设甲烷有1mol,水蒸气有1mol,则

平衡后混合气体的总量:(0.8+0.8+0.2+0.6)mol=2.4mol,P(CH4)=P(H2O)=![]() ×4.0MPa=
×4.0MPa=![]() Mpa,P(CO)=
Mpa,P(CO)=![]() ×4.0MPa=
×4.0MPa=![]() Mpa,P(H2)=
Mpa,P(H2)=![]() ×4.0MPa=1Mpa,A点的平衡常数Kp=
×4.0MPa=1Mpa,A点的平衡常数Kp=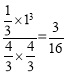 ;
;
反应CH4(g)+H2O(g)CO(g)+3H2(g)为放热反应,温度升高,平衡右移,平衡常数增大,由图知,ABC三点温度依次升高,故平衡常数大小关系为Kp(C)>Kp(B)>Kp(A),
故答案为:![]() ;Kp(C)>Kp(B)>Kp(A);
;Kp(C)>Kp(B)>Kp(A);
②CH4(g)+H2O(g)CO(g)+3H2(g)是气体体积增大的反应,增大压强,平衡左移,甲烷转化率减小,由图知温度不变时压强P1、P2、P3下甲烷转化率逐渐减小,所以压强P1、P2、P3由大到小的顺序为P3>P2>P1,故答案为:P3>P2>P1;其他条件不变时,压强增大,平衡左移,甲烷的转化率减小;
(3)两种反应物存在,增加其中一种反应物的量,能使另一种反应物的转化率提高,a点H2O的含量相对较大,所以a点CH4的转化率更高;根据反应方程式分析,CH4和H2O是按照1:1反应的,a点CH4和
A.平衡常数K只与温度有关,温度不变,K不变,故A错误;
B.H2O(g)浓度越大,X越小,CH4的转化率越大,故C错误;
C.由图知当x=1时,氢气的产率最大,故C正确;
D.当x=1时,合成气的浓度最大,故D正确。故答案为:>;=;CD。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】轻质碳酸钙(CaCO3)是一种重要的化工产品,广泛应用于油漆、塑料、橡胶和造纸等工业。一种以低品位石灰石(含CaCO3、MnCO3、Fe2O3及A12O3)为原料生产高纯度轻质碳酸钙的循环工艺流程如图:

回答下列问题:
(1)气体A为:______,滤渣的主要成分是______。
(2)“沉钙”过程中发生的化学反应方程式为______。
(3)在NH4C1尾液中加入氧化镁并加热,发生反应的离子方程式为______。
(4)“系列操作”包含有:______。
(5)氧化镁可以在尾液处理中循环使用,______和_______可循环使用于石灰石制备轻质碳酸钙的过程中。
(6)轻质碳酸钙的工业生产还可以使用“石灰碳化法”:用高品位石灰石焙烧制得生石灰,生石灰消化制得氢氧化钙,再通入二氧化碳制得碳酸钙;本题工艺流程与“石灰碳化法,相比,优点是:______,______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸 | CH3COOH | H2CO3 |
电离平衡常数(常温) | Ka=1.8×10-5 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则c(CH3COOH)/c(CH3COO-)=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(C1O2)易溶于水,是一种处理水的高效安全消毒剂。实验室以NH4C1、盐酸、NaClO2为原料制备C1O2的流程如下。已知NCl3晶体在95℃就会发生爆炸性分解,在热水中易分解,在空气中易挥发。下列说法错误的是( )

A.除去C1O2中的NH3可选用饱和食盐水
B.电解时,发生反应的化学方程式为NH4C1+2HCl![]() 3H2↑+NCl3
3H2↑+NCl3
C.X溶液中大量存在的离子是Na+、C1-、H+
D.为保证实验的安全,在电解时要控制好反应温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A.pH=5的H2S溶液中,c(H+)= c(HS-)=1×10-5 mol·L-1
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H2CO3溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HCO3-)+c( CO32-)
D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+
B.由水电离的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
C.![]() =1012的溶液中:NH4+、Al3+、NO3-、Cl-
=1012的溶液中:NH4+、Al3+、NO3-、Cl-
D.NaHS溶液中:K+、S2-、SO42-、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,它可由冰醋酸与过氧化氢在一定条件下制得;它可以迅速杀灭多种微生物,包括多种病毒(如:SARS病毒、禽流感病毒)、细菌、真菌及芽孢。下面是市售过氧乙酸商品标签:

有关资料:H2O2是极弱的电解质,在酸性介质中才能稳定存在,是一种强氧化剂。过氧乙酸消毒液是由H2O2、H2O、CH3COOH及少量H2SO4混合后,反应生成过氧乙酸(CH3COOOH)。CH3COOOH容易放出氧原子,它与空气中微生物机体作用,达到灭菌目的,是消毒液的主要成分。
(1)某研究性学习小组为了弄清配制过氧乙酸消毒液的甲、乙溶液的主要成分各是什么?进行以下科学探究,请你完成下列相关内容:
①提出假设:甲溶液的主要成分为_________,乙溶液的主要成分为_________。
②实验验证:取甲、乙两种溶液少许,分别加入几滴_________试液,若①中假设正确,则甲溶液的现象为_____________________,乙溶液的现象为__________。
(2)有关过氧乙酸的叙述正确的是_________ (填编号)
A.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
B.过氧乙酸与苯酚混合使用可增强消毒效果
C.过氧乙酸与乙酸属于同系物
D.氧元素的化合价为-2价
(3)实验室制备少量过氧乙酸,可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
①在三颈烧瓶中加入一定量冰醋酸与浓H2SO4的混合液体,再缓缓加入适量30%的双氧水。
②不断搅拌并控制B中混合液的温度为20~30℃至反应结束。
③接入冷凝管和抽气泵,在锥形瓶中收集得到产品。
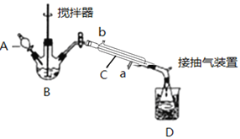
请回答下列问题:
①仪器C的名称是_______________;
②为更好地控制反应温度,应采用方法是_________________;
③生成过氧乙酸的化学方程式为________________________________________;
④碘量法取2.00mL过氧乙酸试样稀释成100mL,从中取出5.00mL,滴加酸性KMnO4溶液至恰好粉红色以除去残余H2O2,再加入10mL 10%KI溶液和几滴淀粉溶液,摇匀,反应完全后再用0.1000mol/L的Na2S2O3标准液滴定至终点(反应方程式为2Na2S2O3+I2=Na2S4O6+2NaI),共消耗14.30mL Na2S2O3标准液。该样品中过氧乙酸的物质的量浓度是_____mol/L。(结果保留小数点后两位)(提示:CH3COOOH+2I+2H+ =I2+CH3COOH +H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应中的能量变化,下列说法中不正确的是( )
A. 燃烧反应都是放热反应
B. 对于可逆反应:aA(g)+bB(g)![]() bC(g)+dD(g),如果正反应放热,逆反应一定吸热
bC(g)+dD(g),如果正反应放热,逆反应一定吸热
C. 氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量
D. 只有放热的氧化还原反应才可以设计为原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近来,郑州大学药学院某研究小组合成出具有抗肿瘤活性的化合物X,其合成路线如下图所示:
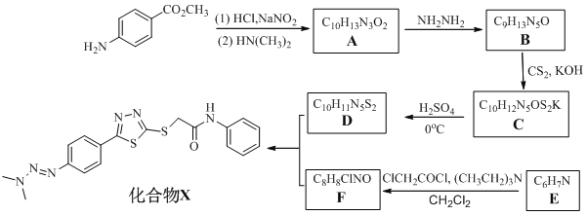
已知:
a.R-SH+R’Cl→RS-R’
b 
c 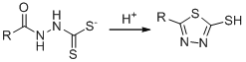
请回答:
(1)化合物F的结构简式_________________,推测E和ClCH2COCl反应得到化合物F的过程中, 二氯甲烷(CH2Cl2)是反应的溶剂,那(CH3CH2)3N的作用是_________________。
(2)下列说法正确的是___________________。
A. 化合物D可与钠反应
B. 上述生成B、F、化合物X的反应均为取代反应
C. 1 mol 化合物B可以与5 mol H2发生加成反应
D. 化合物X分子式为C18H18N6OS2
(3)A→B的化学方程式为__________________________________。
(4)写出同时符合下列条件的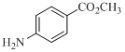 的同分异构体的结构简式:______________。
的同分异构体的结构简式:______________。
①红外光谱显示分子中含有一个甲基,1H-NMR谱图显示苯环上有两种化学环境的氢;
②分子能水解,且能发生银镜反应
(5)设计以甲苯、甲醇为原料合成化合物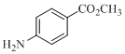 (用流程图表示,无机试剂任选)________________________________。
(用流程图表示,无机试剂任选)________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com