
【题目】填空
(1)![]() 的名称是 ______ ;
的名称是 ______ ;
(2) 的名称是 ______ ;
的名称是 ______ ;
(3) 的含氧官能团的名称___________________________________
的含氧官能团的名称___________________________________
(4)实验测定某有机物元素质量组成为C:69% H:4.6% N:8.0%,其余是O,该有机物的实验式为________
科目:高中化学 来源: 题型:
【题目】下列说法或表示法正确的是( )
A.CO(g)的燃烧热是283.0kJ·mol-1,则表示CO(g)的燃烧热的热化学方程式为:2CO(g)+O2(g)=2CO2(g) △H=-283.0kJ·mol-1
B.当反应物的总能量比生成物的总能量高时,为吸热反应;当生成物的总能量比反应物的总能量高时,则为放热反应
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含lmolNaOH的溶液混合,放出的热量等于57.3kJ
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO﹣)﹣c(Na+)=________(填准确数值)。
(2)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为___________________________________。
(3)写出使用泡沫灭火器时发生反应的离子方程式_________________________________。
(4)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈_______(填“酸性”,“中性”或“碱性”),溶液中c(Na+) _______c(CH3COO-)(填“ >” 或 “=”或“<”)。
(5)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈_______(填“酸性”,“中性”或“碱性”)。
(6)25℃时,体积为Va、pH=a的某一元强酸溶液与体积为Vb、pH=b的某一元强碱溶液均匀混合后,溶液的pH=7,已知b=2a,Va<Vb,则a的取值范围为________。
(7)今有a·盐酸 b·硫酸 c·醋酸三种酸:完全中和含等物质的量的NaOH的溶液,消耗相同pH的上述三种酸溶液的体积由大到小的顺序是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是
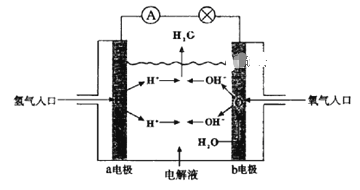
A. a电极是负极
B. 氢氧燃料电池是一种具有应用前景的绿色电源
C. b电极的电极反应为:4OH--4e-=2H2O+O2↑
D. 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al、Cu、Fe及其化合物常用于制备溴苯、乙醛反应的催化剂,也可以与CO、CN-、SCN-、N3-、NO2-、NH3、H2O等形成配合物。回答下列问题:
(1)Cu+基态核外电子排布式为________。
(2)Mg、Al、Si原子的第一电离能由大到小的顺序为________。
(3)CO、H2O、 CN-、SCN-、N3-、NH3中,有________对等电子体。
(4)乙醛分子中C原子轨道杂化的类型是________。等物质的量的溴苯和乙醛所包含的σ键的数目之比为________。
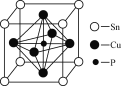
(5)磷青铜的晶胞结构如图所示,该晶体中铜、锡、磷三种原子的数目之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. lmol 该有机物( )最多能与4mol 氢气加成
)最多能与4mol 氢气加成
B. 乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C. 乳酸薄荷醇酯( )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
D.  分子中至少有9个碳原子处于同一平面上
分子中至少有9个碳原子处于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是二元弱酸,KHC2O4溶液呈酸性。向10mL 0.01mol·L-1的H2C2O4溶液滴加0.01mol·L-1KOH溶液V(mL),回答下列问题。
(1)当V<10mL时,反应的离子方程式为___。
(2)当V=10mL时,溶液中HC2O4-、C2O42-、H2C2O4、H+的浓度从大到小的顺序为___。
(3)当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+(HC2O4-);当V=b mL时,溶液中离子浓度有如下关系:c(K+)= c(C2O42-)+c(HC2O4-)+c(H2C2O4);则a___b(填“<”“=”或“>”)。
(4)当V=20mL时,再滴入NaOH溶液,则溶液中![]() 的值将___(填“变大”“变小”或“不变”)。
的值将___(填“变大”“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X为中学化学常见物质,A、B、C含有相同元素甲,可以发生如下转化(水参与的反应,水未标出)。
![]()
下列说法不正确的是
A.若A、B、C的焰色反应呈黄色、水溶液均呈碱性,则X可以是CO2
B.若C为红棕色气体,则A一定为空气中含量最高的气体
C.若B为FeCl3,则X一定是Fe
D.A可以是碳单质,也可以是O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下表所示为元素周期表的一部分,参照元素①~⑦在表中的位置,请回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(1)③④⑦的原子半径由大到小的顺序为____(用元素符号表示)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为____(用酸的化学式表示)。
(3)②④两种元素按原子个数之比为1:1组成的化合物的电子式____。
(4)①②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式___。
(5)表中⑤的单质和④的最高价氧化物水化物反应的化学方程式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com