
����Ŀ���л���G��һ��ҽҩ�м��塣��ϳ�·�����£�

(1)B�к�������������Ϊ________��________��
(2)B��C��Ӧ����Ϊ________��
(3)D�ķ���ʽΪC10H11OCl��д��D�Ľṹ��ʽ��________��
(4)д����������������F��һ��ͬ���칹��Ľṹ��ʽ��________��
�ٷ����к���1���������ܷ���������Ӧ��
�ڷ�������4�ֲ�ͬ��ѧ�������⡣
(5)����![]() ��
��![]() ��
��![]() Ϊԭ���Ʊ�
Ϊԭ���Ʊ�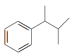 ��д����Ӧ�ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)________��
��д����Ӧ�ĺϳ�·������ͼ(���Լ����ã��ϳ�·������ͼʾ�����������)________��
���𰸡��ʻ� �Ȼ� ��ԭ��Ӧ 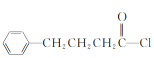
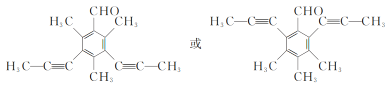
��������
A��![]() ��AlCl3�����·���ȡ����Ӧ����
��AlCl3�����·���ȡ����Ӧ����![]() ��
��![]() ��HCl�ڴ��������·������ԭ��Ӧ����
��HCl�ڴ��������·������ԭ��Ӧ����![]() ��
��![]() ��SOCl2����ȡ����Ӧ����D��D��AlCl3�����·���ȡ����Ӧ����
��SOCl2����ȡ����Ӧ����D��D��AlCl3�����·���ȡ����Ӧ����![]() �������������֪��DΪ
�������������֪��DΪ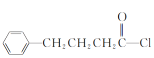 ���ݴ˷�������
���ݴ˷�������
��1��BΪ![]() �����к�������������Ϊ�ʻ����Ȼ���
�����к�������������Ϊ�ʻ����Ȼ���
��2��B��C�Ĺ����У��ʻ�ת��Ϊ�Ǽ������ڻ�ԭ��Ӧ��
��3��![]() ��SOCl2����ȡ����Ӧ����D��D�ķ���ʽΪC10H11OCl����֪DΪ��
��SOCl2����ȡ����Ӧ����D��D�ķ���ʽΪC10H11OCl����֪DΪ��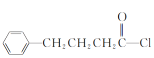 ��
��
��4��F�ķ���ʽΪC16H16O���䲻���Ͷ�=![]() =9���ٷ����к���1���������ܷ���������Ӧ����˵�������ں�ȩ�����ڷ�������4�ֲ�ͬ��ѧ�������⣬�����Ϊ�Գƽṹ����������������ͬ���칹��Ϊ��
=9���ٷ����к���1���������ܷ���������Ӧ����˵�������ں�ȩ�����ڷ�������4�ֲ�ͬ��ѧ�������⣬�����Ϊ�Գƽṹ����������������ͬ���칹��Ϊ��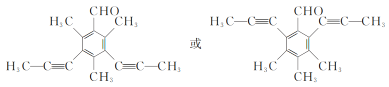 ��
��
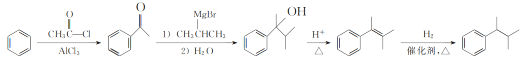
��5�����������ϳ�·�ߣ���������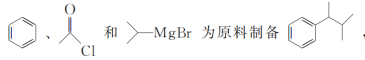 �����Ƚ�����AlCl3��������CH3COCl���з�Ӧ�����������ɵ�
�����Ƚ�����AlCl3��������CH3COCl���з�Ӧ�����������ɵ�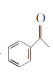 ��
��![]() �Լ�ˮ���з�Ӧ�Ʊ�
�Լ�ˮ���з�Ӧ�Ʊ�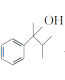 ��������ϳɷ��������Ŀ����ֻҪ��
��������ϳɷ��������Ŀ����ֻҪ�� ���������¼��ȿ�����
���������¼��ȿ�����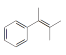 ������������ӳɼ��ɵõ�
������������ӳɼ��ɵõ�![]() ������ϳ�·��Ϊ��
������ϳ�·��Ϊ�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�������[(CH3O)2CO]��һ�־��з�չǰ��������ɫ��������Ʒ���绯ѧ���ϳ�̼��������Ĺ���ԭ����ͼ��ʾ������˵���������
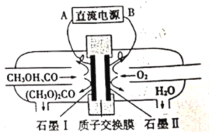
A.ʯīI��ֱ����Դ��������
B.H����ʯīIIͨ�����ӽ���Ĥ��ʯīI�ƶ�
C.ʯīI�Ϸ����ĵ缫��ӦΪ2CH3OH��CO��2e����(CH3O)2CO��2H��
D.�������У�����������������������ʵ���֮��Ϊ1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA�ǰ����ӵ�������ֵ������˵����ȷ���ǣ� ��
A.1molK2Cr2O7����ԭΪCr3+ת�Ƶĵ�����Ϊ3NA
B.0.1molCH4��Cl2�ڹ����·�Ӧ���ɵ�CH3Cl������Ϊ0.1NA
C.���³�ѹ�£�124gP4������P��P����Ŀ4NA
D.��״���£�22.4L�������������ۼ���ĿΪ10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��Ϊ����������Ԫ�أ�����Ԫ��λ��ͬһ���ڣ�
��Ϊ����������Ԫ�أ�����Ԫ��λ��ͬһ���ڣ�![]() ��Ԫ�ص�����������֮����Z��������������ȣ�Y���������������ڲ��������3��������˵����ȷ����( )
��Ԫ�ص�����������֮����Z��������������ȣ�Y���������������ڲ��������3��������˵����ȷ����( )
A.ԭ�Ӱ뾶��![]() B.����⻯������ȶ��ԣ�
B.����⻯������ȶ��ԣ�![]()
C.XZΪ���ۻ�����D.![]() �ĵ��ʾ�������ˮ������Ӧ
�ĵ��ʾ�������ˮ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H��һ�ָ�Ч���ݼ�����ϳ�·������ͼ��ͼ��
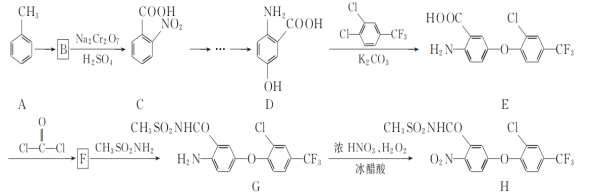
��1��E�к�������������Ϊ____��____��
��2��A��B�ķ�Ӧ����Ϊ____��
��3��д��ͬʱ��������������D��һ��ͬ���칹��Ľṹ��ʽ��____��
�ٲ��ܷ���ˮ�ⷴӦ������FeCl3��Һ������ɫ��Ӧ��
�ڷ�������4�ֲ�ͬ��ѧ�������⡣
��4��F�ķ���ʽΪC15H7ClF3NO4������Ԫ�ӻ�����д��F�Ľṹ��ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г������ʵ�ת����ϵ���������ʺͷ�Ӧ������ȥ��
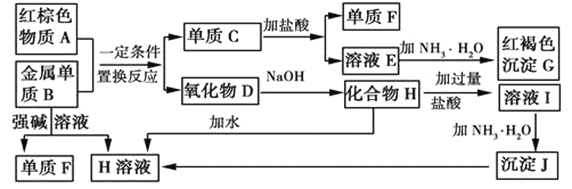
��1������F�Ļ�ѧʽ��___��
��2��д���ɳ���J���� H��Һ�����ӷ���ʽ__��
��3����ҺE�м��백ˮʱ�������ɰ�ɫ����L��д������L�����ӷ���ʽ��__����ɫ����L���ձ�Ϊ���ɫ����G��д��L��ΪG�Ļ�ѧ��Ӧ����ʽ__��
��4����ҺI����������������__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ������й㷺��;����̼��������FeCO3������Ϊ��Ѫ�������죨Fe2O3������Ϊ���ϡ�����ij���᳧��������������Ҫ��FeCO3��FeO������һ������SiO2���Ʊ�̼��������������ͼ��
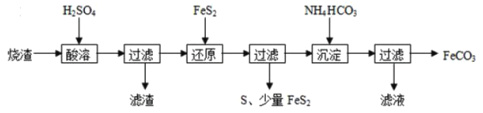
��1�������ܡ�ʱ�ӿ췴Ӧ���ʵķ�����____��д��һ�֣���
��2���١���ԭ��ʱ��FeS2��H2SO4����Ӧ��Fe3+ͨ��������Ӧ����ԭ������һ����Ӧ���£�FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+������һ����Ӧ�����ӷ���ʽΪ��___��
��FeS2��ԭ����Fe3+�Ƿ�Ӧ��ȫ�ķ�����___��
��3���١�������ʱ�������pH���˹��ߣ��������ɵ�FeCO3�п��ܻ���___���ʣ�
���ܷ�NH4HCO3����(NH4)2CO3___��
��4��FeCO3��Һ��ʱ�䱩¶�ڿ����У����в��ֹ�������Ϊ���ɫ��ͬʱ�ͷų�CO2������FeCO3��Ӧ������Ϊ___���ѧʽ����
��5��FeCO3�ڿ�������������Fe2O3ʱ��Ҳ������FeO��������34.8g��FeCO3���õ�Fe2O3��FeO�Ļ����23.76g����Fe2O3������Ϊ___g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д��ȷ���ǣ� ��
A.����������Һ�м����������ữ�Ĺ���������Һ��Fe2����2H����H2O2=Fe3����2H2O
B.������ˮ��Ӧ��Cl2 + H2O![]() 2H+ + Cl- + ClO-
2H+ + Cl- + ClO-
C.̼����������Һ��Ӧ��CaCO3��2H��=Ca2����CO2����H2O
D.��A12(SO4)3��Һ�м�������İ�ˮ��A13++3NH3��H2O=A1(OH)3��+3NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2��һ���������壬����������滷���������Ӱ�죬ά�ִ�����CO2��ƽ�����̬��������������Ҫ���塣
��1��CO2����ϳɵ�̼ϩ����������Ч����CO2���Ժϳ�C2H4Ϊ������ת����Ϊ�������У�
��һ����CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H1=+41.3kJ/mol
CO(g)+H2O(g) ��H1=+41.3kJ/mol
�ڶ�����2CO(g)+4H2(g)![]() C2H4(g)+2H2O(g) ��H2=-210.5kJ/mol
C2H4(g)+2H2O(g) ��H2=-210.5kJ/mol
CO2����ϳ���ϩ���Ȼ�ѧ����ʽΪ__��
��2������CO2��H2�ϳɼ״�����һ����Ч����CO2��;������Ӧ���£�CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H3
CH3OH(g)+H2O(g) ��H3
�����ݻ�Ϊ2L�ĺ����ܱ������У�ͨ��2molCO2��3molH2����������Ӧ������˵���ܹ������ÿ��淴Ӧ�ﵽƽ��״̬����__������ĸ��
a.����1.5molH2ʱ����0.5molCH3OH����
b.ת��3mol����ʱ������11.2L����״���£�CO2
c.��ϵ��������ܶȲ���
d.ˮ����������������ֲ���
e.��λʱ��������H2������H2O�����ʵ���֮��Ϊ3��1
���о��¶ȶԸ÷�Ӧ�״����ʵ�Ӱ�졣��210�桫290�棬����ԭ������CO2��H2��Ͷ�ϱȲ��䣬��һ�����ٷ���������Ӧ���õ��״�ƽ��������¶ȵĹ�ϵ��ͼ��ʾ����H3__0�����������=�����������ж�������__��
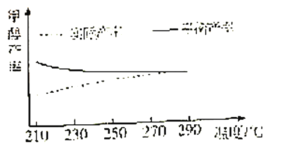
����һ�̶��ݻ����ܱ������з���������Ӧ����Ҫ���ƽ��ʱCH3OH���ʣ�����Բ�ȡ�Ĵ�ʩ��__������ĸ����
a.���� b.������� c.����CO2��Ũ�� d.����H2��ѹ e.����������� f.������״�
��3����һ���¶Ⱥʹ��������£�Ҳ�ɽ�CO2ת��Ϊȼ��CH4����Ӧ����ʽΪCO2(g)+4H2(g)![]() CH4(g)+2H2O(g)����30��ʱ��һ������CO2��H2����������ݻ�Ϊ1L�ĺ����ܱ������з���������Ӧ��5min��ﵽ��⣬��ʱ�����ʵ�Ũ�����±���
CH4(g)+2H2O(g)����30��ʱ��һ������CO2��H2����������ݻ�Ϊ1L�ĺ����ܱ������з���������Ӧ��5min��ﵽ��⣬��ʱ�����ʵ�Ũ�����±���
���� | CO2(g) | H2(g) | CH4(g) | H2O(g) |
Ũ��/mol��L-1 | 0.2 | 0. | a | 1.6 |
��a=__���÷�Ӧƽ�ⳣ��K=__��
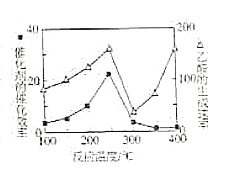
��4����TiO2/Cu2Al2O4Ϊ����������CH4���Խ�CO2ֱ��ת�������ᡣ�ڲ�ͬ�¶��´����Ĵ�Ч����������������ʵĹ�ϵ��ͼ��ʾ�����������������Ҫȡ�����¶�Ӱ��ķ�Χ��__��250��300��ʱ���¶����߶�������������ʽ��͵�ԭ����__��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com