
【题目】FeS2焙烧产生的SO2可用于制硫酸.已知25℃、101kPa时: 2SO2(g)+O2(g) ![]() 2SO3(g)△H1=﹣197kJmol﹣1;
2SO3(g)△H1=﹣197kJmol﹣1;
H2O(g)═H2O(l)△H2=﹣44kJmol﹣1;
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=﹣545kJmol﹣1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是 .
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O据此,下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O据此,下列说法不正确的是( )
A. KClO3发生还原反应
B. H2C2O4在反应中被氧化
C. H2C2O4的氧化性强于C1O2的氧化性
D. 每1mol C1O2生成,该反应转移的电子数约为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一个有机物的核磁共振氢谱图,请你观察图谱,分析其可能是下列物质中的( ) 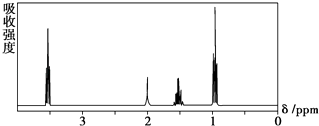
A.CH3CH2CH2CH3
B.(CH3)2CHCH3
C.CH3CH2CH2OH
D.CH3CH2COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(1)在光照条件下,氯气和氢气反应过程如下: ①Cl2→Cl+Cl
②Cl+H2→HCl+H
③H+Cl2→HCl+Cl
…
反应②中形成的化合物的电子式为;反应③中被破坏的化学键属于键(填“极性”或“非极性”).
(2)已知在短周期主族元素中,元素a与氯元素相邻且属同一周期,元素b也与氯元素相邻且属于同一主族,那么比较元素a、b以及氯元素三者的原子半径由大到小的顺序是(用元素符号表示).与氯元素同周期且金属性最强的元素位于周期表的第周期族.
(3)卤素单质及化合物在许多性质上都存在着递变规律.下列有关说法错误的是(填字母).
A.卤素单质的熔沸点按F2、Cl、Br2、I2的顺序由低到高
B.原子半径按
C.Cl、Br、I的顺序由大到小
D.卤化氢的稳定性按的H
E.HCl、HBr、HI的顺序由强到弱
F.卤素单质与氢气化合按的F2、Cl2、Br2、I2顺序由难变易
(4)碘单质及其化合物具有重要应用.下列说法正确的是(填字母). a. ![]() I与
I与 ![]() I互为同位素
I互为同位素
b.加碘食盐能使淀粉溶液变蓝
c.从海带中提取I2的过程只发生化学变化
d.提纯含泥沙的粗碘可用升华法.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组用打磨过的铝片进行如下实验,下列分析不合理的是

A. ①中铝片发生了钝化
B. ②中产生的气泡可能是氮氧化合物
C. ③中沉淀溶解的离子方程式是Al(OH)3+ OH-=AlO2- + 2H2O
D. ②中加水稀释过程中,仅发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20.其中A为非金属元素;A和E属同一族,它们原子最外层电子排布为ns1 . B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题:
(1)A是 , B是 , C是 , D是 , E是 .
(2)由这五种元素组成的一种化合物是(写化学式) .
(3)写出C元素基态原子的电子排布式: .
(4)用电子排布图表示D元素原子的价电子排布为 .
(5)元素B与D的电负性的大小关系是BD,C与E的第一电离能的大小关系是CE.(填“>”、“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com